Clear Sky Science · sv
Säker öppning av blod‑hjärnbarriären med fokuserad ultraljudsbehandling drivs främst av tillfällig omorganisering av täta fogar
Varför det spelar roll att öppna hjärnans grind
Många av de mest lovande behandlingarna för Alzheimers sjukdom, hjärntumörer och andra neurologiska tillstånd når aldrig sina mål eftersom hjärnan skyddas av en mikroskopisk grindvakt kallad blod‑hjärnbarriären. Denna barriär skyddar den känsliga nervvävnaden från skadliga ämnen i blodet, men blockerar också de flesta nyttiga läkemedel. Studien som sammanfattas här utforskar ett icke‑invasivt sätt att tillfälligt öppna barriären med fokuserade ljudvågor och visar vad som händer i hjärnans blodkärl när metoden används försiktigt respektive för aggressivt.
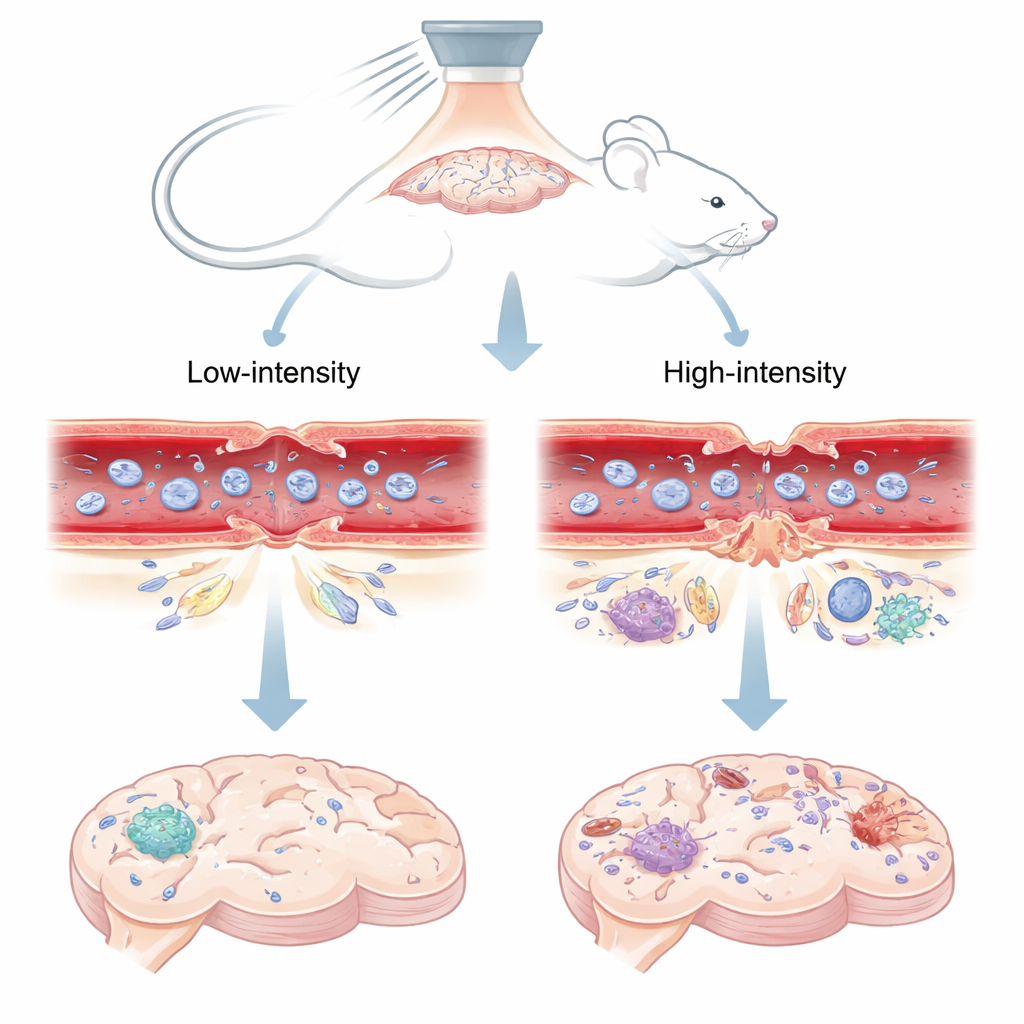
En ljuddriven dörr in i hjärnan
Forskare använde fokuserat ultraljud – koncentrerade ljudvågor från utsidan av skallen – i kombination med små gasfyllda bubblor som injicerades i blodet. När ljudvågorna träffar dessa mikrobubblor i hjärnans blodkärl vibrerar bubblorna. Vid lägre ljudtryck svänger bubblorna kontrollerat; vid högre tryck kan de kollapsa våldsamt. Teamet testade två nivåer i möss: en “låg” inställning känd från tidigare arbete för att öppna barriären säkert och kortvarigt, och en “hög” inställning som förknippas med längrevarig läcka och vävnadsskada. De följde sedan hur en fluorescerande färg och ett MR‑kontrastämne spreds in i hjärnan, vilket visade när och var barriären öppnades och när den tillslöts igen.
Mikroskopiska grindar som förskjuts eller krossas
Blod‑hjärnbarriären bildas huvudsakligen av täta fogar – protein‑“blixtlås” som tätar intilliggande celler som bekläder hjärnans blodkärl. I speciella möss där dessa täta fogar lyser under mikroskop kunde forskarna iaktta hur blixtlåsen ändrade form efter ultraljudet. Vid det säkra, låga ljudtrycket visade fogarna små, tillfälliga glipor i både de minsta kapillärerna och något större arterioler. Inom ungefär tre dagar hade dessa glipor till stor del slutits och mönstret av fogar liknade i hög grad den orörda sidan av hjärnan, i linje med att färg och MR‑kontrast inte längre läckte in. Vid det högre trycket var fogarna däremot inte bara glipande utan ibland helt försvunna, särskilt i större kärl. Dessa allvarliga brott bestod i minst 72 timmar och åtföljdes av fortsatt läckage av spårmolekyler.
Hjärnans immunceller och blodproteiner blir en del av bilden
Öppning av barriären tillåter också blodproteiner att komma in i hjärnvävnaden. Ett sådant protein, fibrinogen, är involverat i koagulering och inflammation och har kopplats till skada i flera hjärnsjukdomar. Kort efter ultraljud vid båda trycknivåerna syntes fibrinogen nära läckande kärl tillsammans med aktiverade mikroglia, hjärnans egna immunceller. Mikroglian förändrade form från ett vilande, förgrenat utseende till en rundare, “alarmbered” form. Vid 72 timmar var fibrinogen inte längre detekterbart för någon av trycknivåerna, vilket tyder på att även när fogskadorna bestod vid den högre inställningen hade vissa aspekter av läckaget avtagit. Forskarnas försök med möss utan caveolae, små fickor i kärlväggen som kan transportera molekyler genom celler, visade att barriärens öppning vid det säkra trycket inte påverkades avsaknaden av dessa strukturer. Detta pekar på omorganisering av täta fogar – inte en ökad transcellulär transportväg – som huvudmekanism för kontrollerad öppning.
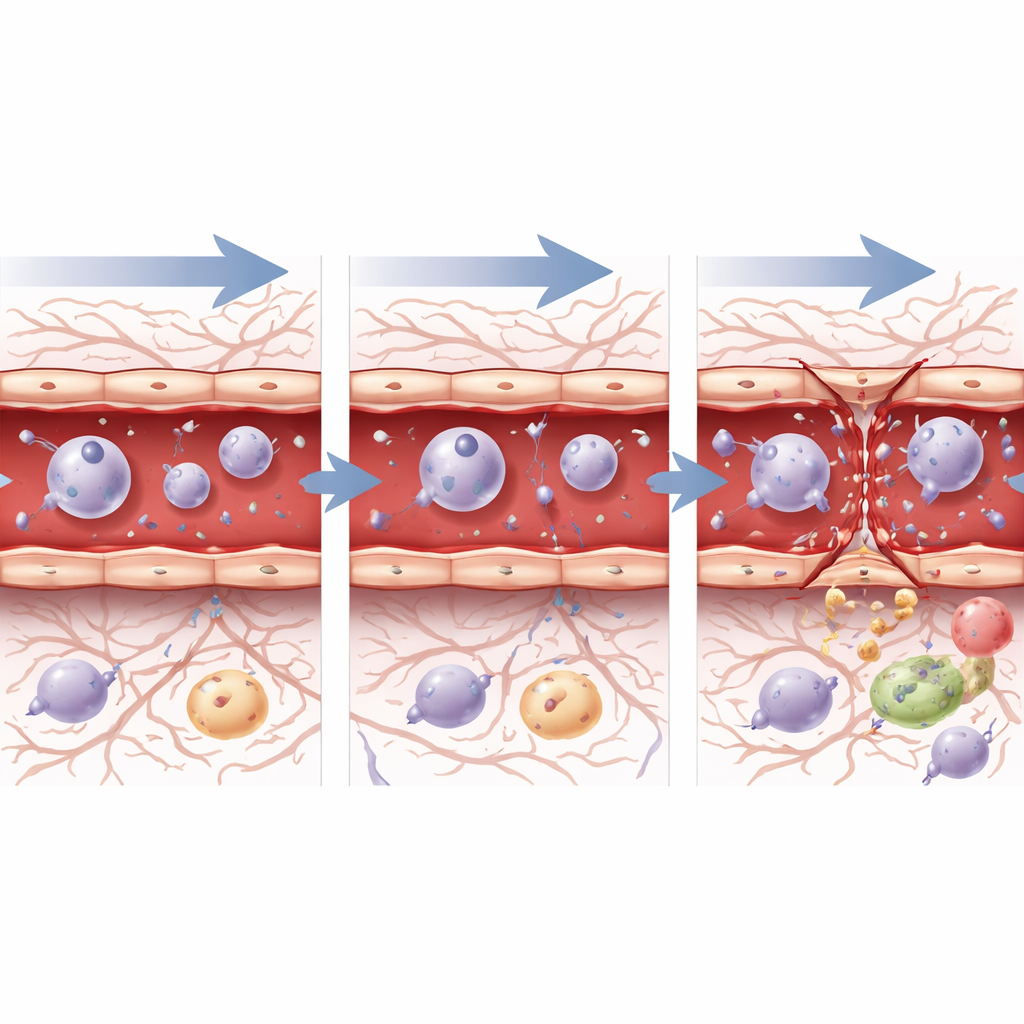
Hur kärlcellernas inre svar ser ut
För att se hur enskilda kärlceller reagerar på gen-nivå isolerade teamet tusentals endotelceller – cellerna som bekläder artärer, kapillärer och vener – och utförde enskildcells‑RNA‑sekvensering. Inom en timme efter ultraljud ökade dessa celler, oberoende av tryck, uttrycket av gener kopplade till stress, celldöd, inflammation och reparation, vilket signalerar att de kände både skada och behovet av återhämtning. Efter 72 timmar skilde sig bilden åt. Efter det säkra, låga trycket visade cellerna genaktivitet som stämde överens med sårläkning, kontrollerad celldelning och en gradvis återgång mot ett stabilt barriärtillstånd. Efter det högre trycket uttryckte cellerna fortsatt starkt stress‑ och “sårsvar”‑program, och nyckelgener för uppbyggnad av fogar förblev dämpade, i linje med den fortgående strukturella skadan som sågs i mikroskopet. Signaleringsvägar som styr kärltillväxt och barriärbildning, såsom TGF‑beta, Notch och Wnt, ändrade över tiden i riktningar som antydde aktiv men ofullständig reparation, särskilt efter den mer aggressiva inställningen.
Vad detta betyder för framtida hjärnbehandlingar
För dem som hoppas på bättre behandlingar för hjärnan klargör detta arbete en central säkerhetsfråga: hur kan vi öppna blod‑hjärnbarriären tillräckligt för att släppa in läkemedel utan att orsaka bestående skada? Studien visar att vid noggrant utvalda, lägre ultraljudstryck öppnas barriären framför allt eftersom dess protein‑“blixtlås” tillfälligt slappnar av och sedan omorganiserar sig, medan kärlceller aktiverar reparationsprogram som stänger gliporna inom dagar. Att trycka systemet hårdare krossar dessa blixtlås istället för att bara förskjuta dem, vilket lämnar långvariga läckor och utdragen cellär stress. I praktiska termer stöder fynden användning av konservativa ultraljudsinställningar och noggrann övervakning i kliniska tillämpningar och förstärker idén att säker läkemedelsleverans till hjärnan beror på tillfällig omorganisering – inte förstörelse – av hjärnans mikroskopiska grindar.
Citering: Noel, R.L., Kugelman, T., Karakatsani, M.E. et al. Safe focused ultrasound-mediated blood-brain barrier opening is driven primarily by transient reorganization of tight junctions. Commun Eng 5, 58 (2026). https://doi.org/10.1038/s44172-026-00597-5
Nyckelord: fokuserat ultraljud, blod‑hjärnbarriär, Läkemedelsleverans, hjärnans blodkärl, mikrobubblor