Clear Sky Science · de
Sichere, fokussierte Ultraschall-vermittelte Öffnung der Blut-Hirn-Schranke beruht vor allem auf vorübergehender Umorganisation der Tight Junctions
Warum das Öffnen des Hirntors wichtig ist
Viele der vielversprechendsten Behandlungen für Alzheimer, Hirntumore und andere neurologische Erkrankungen erreichen ihre Ziele nicht, weil das Gehirn durch einen mikroskopischen Torwächter geschützt ist: die Blut‑Hirn‑Schranke. Diese Schranke schützt empfindliches Nervengewebe vor schädlichen Substanzen im Blut, blockiert aber gleichzeitig die meisten nützlichen Medikamente. Die hier zusammengefasste Studie untersucht eine nichtinvasive Methode, diese Schranke kurzzeitig mit fokussierten Schallwellen zu öffnen, und zeigt, was mit den Hirnblutgefäßen geschieht, wenn die Methode schonend gegenüber aggressiv angewendet wird.
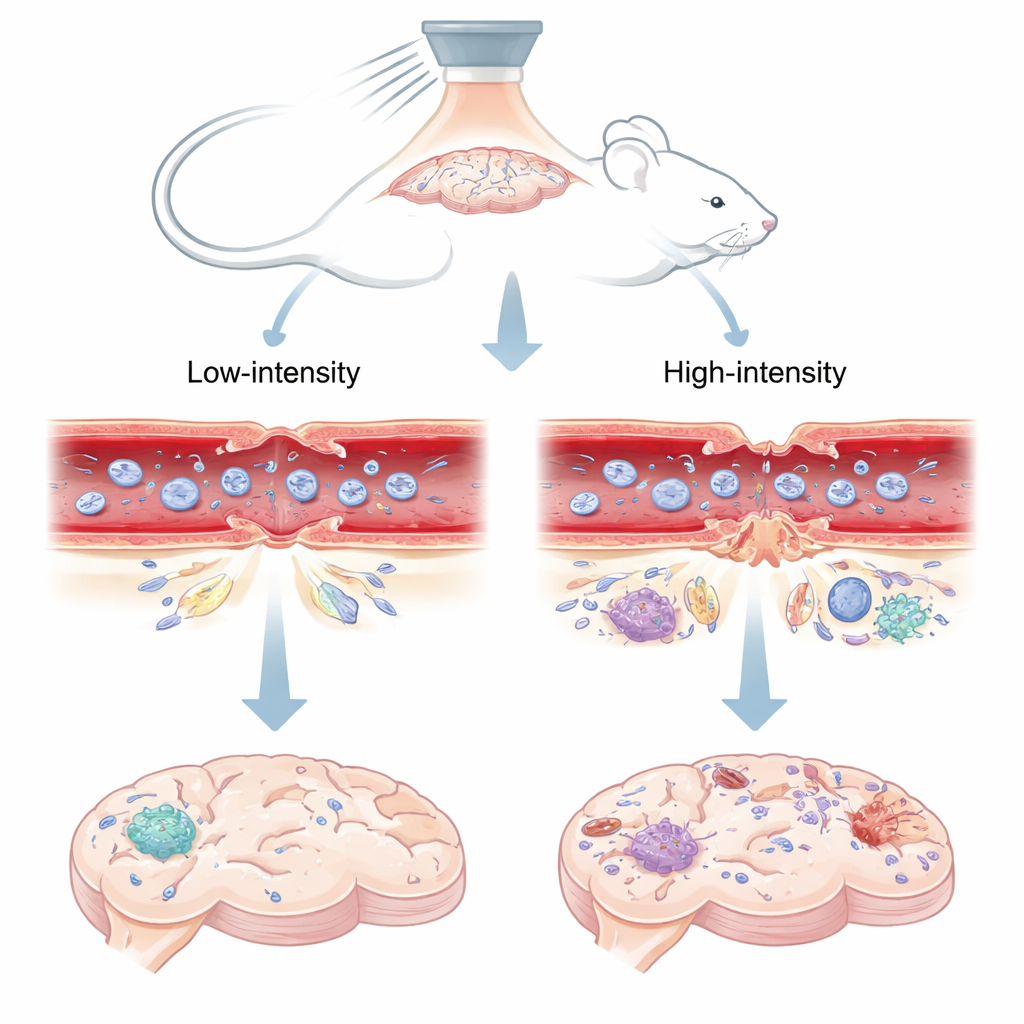
Eine schallbetriebene Tür ins Gehirn
Die Forschenden setzten fokussierten Ultraschall ein – von außen gebündelte Schallwellen – kombiniert mit winzigen, mit Gas gefüllten Bläschen, die in den Blutkreislauf injiziert wurden. Treffen die Schallwellen auf diese Mikroblasen in den Hirngefäßen, beginnen die Bläschen zu vibrieren. Bei niedrigeren Schalldrücken schwanken sie kontrolliert; bei höheren Drücken können sie heftig kollabieren. Das Team testete zwei Pegel an Mäusen: eine „niedrige“ Einstellung, die aus früheren Arbeiten dafür bekannt ist, die Schranke sicher und kurzzeitig zu öffnen, und eine „hohe“ Einstellung, die mit länger anhaltendem Austritt und Gewebeschäden in Verbindung gebracht wird. Anschließend verfolgten die Forschenden, wie ein fluoreszierender Farbstoff und ein MRT‑Kontrastmittel ins Gehirn eindrangen, was zeigte, wann und wo die Schranke geöffnet war und wann sie sich wieder verschloss.
Mikroskopische Tore, die sich verschieben oder zerbrechen
Die Blut‑Hirn‑Schranke wird hauptsächlich durch Tight Junctions gebildet – proteinartige „Reißverschlüsse“, die benachbarte Zellen auskleidender Hirngefäße abdichten. In speziellen Mäusen, bei denen diese Tight Junctions unter dem Mikroskop leuchten, konnten die Wissenschaftler beobachten, wie sich diese Reißverschlüsse nach Ultraschall veränderten. Beim sicheren, niedrigen Schalldruck traten in Kapillaren und etwas größeren Arteriolen kleine, vorübergehende Lücken auf. Innerhalb von etwa drei Tagen schlossen sich diese Lücken größtenteils wieder und das Muster der Junctions ähnelte stark der unbehandelten Hirnhälfte, was mit dem Verschwinden von Farbstoff‑ und Kontrastmittelaustritt übereinstimmt. Bei höherem Druck waren die Junctions jedoch nicht nur aufgeweitet, sondern teilweise ganz fehlend, besonders in größeren Gefäßen. Diese schweren Schäden hielten mindestens 72 Stunden an und gingen mit anhaltendem Austreten von Marker‑Molekülen einher.
Hirn‑Immunzellen und Blutproteine als Teil der Geschichte
Das Öffnen der Schranke lässt auch Blutproteine ins Hirngewebe gelangen. Ein solches Protein, Fibrinogen, ist an Gerinnung und Entzündung beteiligt und steht in Zusammenhang mit Schäden bei mehreren Hirnerkrankungen. Kurz nach dem Ultraschall trat Fibrinogen bei beiden Drücken in der Nähe undichter Gefäße auf, zusammen mit aktivierten Mikroglia, den residenten Immunzellen des Gehirns. Die Mikroglia veränderten ihr Aussehen von ruhend und verzweigt zu rundlicheren, „alarmierten“ Formen. Nach 72 Stunden war Fibrinogen bei beiden Druckstufen nicht mehr nachweisbar, was darauf hindeutet, dass selbst wenn Junction‑Schäden bei der höheren Einstellung anhielten, einige Aspekte des Lecks bereits aufgeklärt waren. Die Forschenden testeten außerdem Mäuse ohne Caveolae, winzige Einstülpungen in der Gefäßwand, die Moleküle über Zellen transportieren können. Das Öffnen der Schranke bei sicherem Druck war ohne diese Strukturen unverändert, was darauf hinweist, dass die Umorganisation der Tight Junctions – und nicht eine Zunahme dieses Transportroutings – der Haupmechanismus für die kontrollierte Öffnung ist.
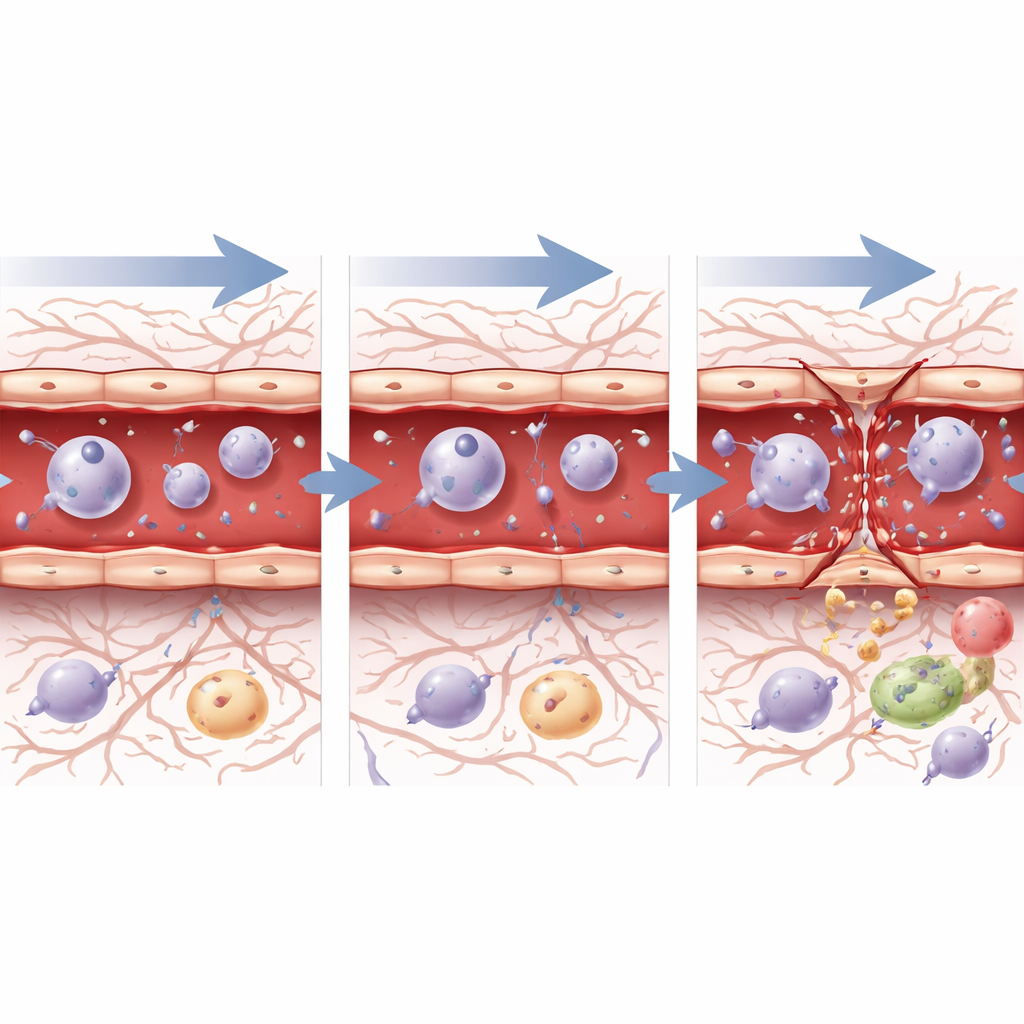
Wie Gefäßzellen von innen reagieren
Um zu sehen, wie einzelne Gefäßzellen auf genetischer Ebene reagieren, isolierte das Team Tausende von Endothelzellen – die Zellen, die Arterien, Kapillaren und Venen auskleiden – und führte Einzelzell‑RNA‑Sequenzierungen durch. Innerhalb einer Stunde nach dem Ultraschall erhöhten diese Zellen unabhängig vom Druck die Aktivität von Genen, die mit Stress, Zelltod, Entzündung und Reparatur verbunden sind, was signalisiert, dass sie sowohl Verletzung als auch Bedarf an Wiederherstellung wahrnehmen. Nach 72 Stunden divergierte das Bild. Nach sicherem, niedrigem Druck zeigten die Zellen Genaktivität, die mit Wundheilung, kontrolliertem Zellwachstum und einer allmählichen Rückkehr zu einem stabilen Schranken‑Zustand vereinbar ist. Nach dem höheren Druck dagegen exprimierten die Zellen weiterhin stark Stress‑ und „Wundantwort“‑Programme, und Schlüsselgene zum Aufbau von Junctions blieben unterdrückt, was mit den anhaltenden strukturellen Schäden unter dem Mikroskop übereinstimmt. Pfade, die Gefäßwachstum und Schrankenbildung steuern, wie TGF‑beta-, Notch‑ und Wnt‑Signalwege, veränderten sich im Zeitverlauf in einer Weise, die auf aktive, aber unvollständige Reparatur hinweist, besonders nach der aggressiveren Einstellung.
Was das für künftige Hirnbehandlungen bedeutet
Für Menschen, die auf bessere Hirntherapien hoffen, klärt diese Arbeit eine zentrale Sicherheitsfrage: Wie können wir die Blut‑Hirn‑Schranke so öffnen, dass Wirkstoffe eindringen können, ohne bleibenden Schaden zu verursachen? Die Studie zeigt, dass bei sorgfältig gewählten, niedrigeren Ultraschallpegeln die Schranke vorwiegend dadurch geöffnet wird, dass ihre proteinartigen „Reißverschlüsse“ sich kurz lockern und danach umorganisieren, wobei Gefäßzellen Reparaturprogramme aktivieren, die die Lücken innerhalb von Tagen schließen. Ein stärkeres Vorgehen zerschlägt diese Reißverschlüsse statt sie nur zu verschieben, bleibt mit länger anhaltenden Lecks und anhaltendem zellulärem Stress verbunden. Praktisch gesprochen unterstützen die Ergebnisse den Einsatz konservativer Ultraschall‑Einstellungen und sorgfältiger Überwachung in klinischen Anwendungen und untermauern die Idee, dass sichere Arzneistoffabgabe ins Gehirn von vorübergehender Umorganisation – nicht Zerstörung – der mikroskopischen Tore des Gehirns abhängt.
Zitation: Noel, R.L., Kugelman, T., Karakatsani, M.E. et al. Safe focused ultrasound-mediated blood-brain barrier opening is driven primarily by transient reorganization of tight junctions. Commun Eng 5, 58 (2026). https://doi.org/10.1038/s44172-026-00597-5
Schlüsselwörter: fokussierter Ultraschall, Blut-Hirn-Schranke, Arzneimittelabgabe, Hirnblutgefäße, Mikroblasen