Clear Sky Science · pt
Abertura segura da barreira hematoencefálica mediada por ultrassom focado é impulsionada principalmente pela reorganização transitória das junções de oclusão
Por que abrir o portão do cérebro importa
Muitos dos tratamentos mais promissores para Alzheimer, cânceres cerebrais e outras condições neurológicas nunca chegam aos seus alvos porque o cérebro é protegido por um guardião microscópico chamado barreira hematoencefálica. Essa barreira protege o tecido nervoso delicado de substâncias nocivas no sangue, mas também bloqueia a maioria dos medicamentos úteis. O estudo resumido aqui explora uma forma não invasiva de abrir essa barreira brevemente com ondas sonoras focalizadas, revelando o que acontece com os vasos sanguíneos do cérebro quando a abordagem é usada de forma suave versus excessivamente agressiva.
Uma porta para o cérebro movida por som
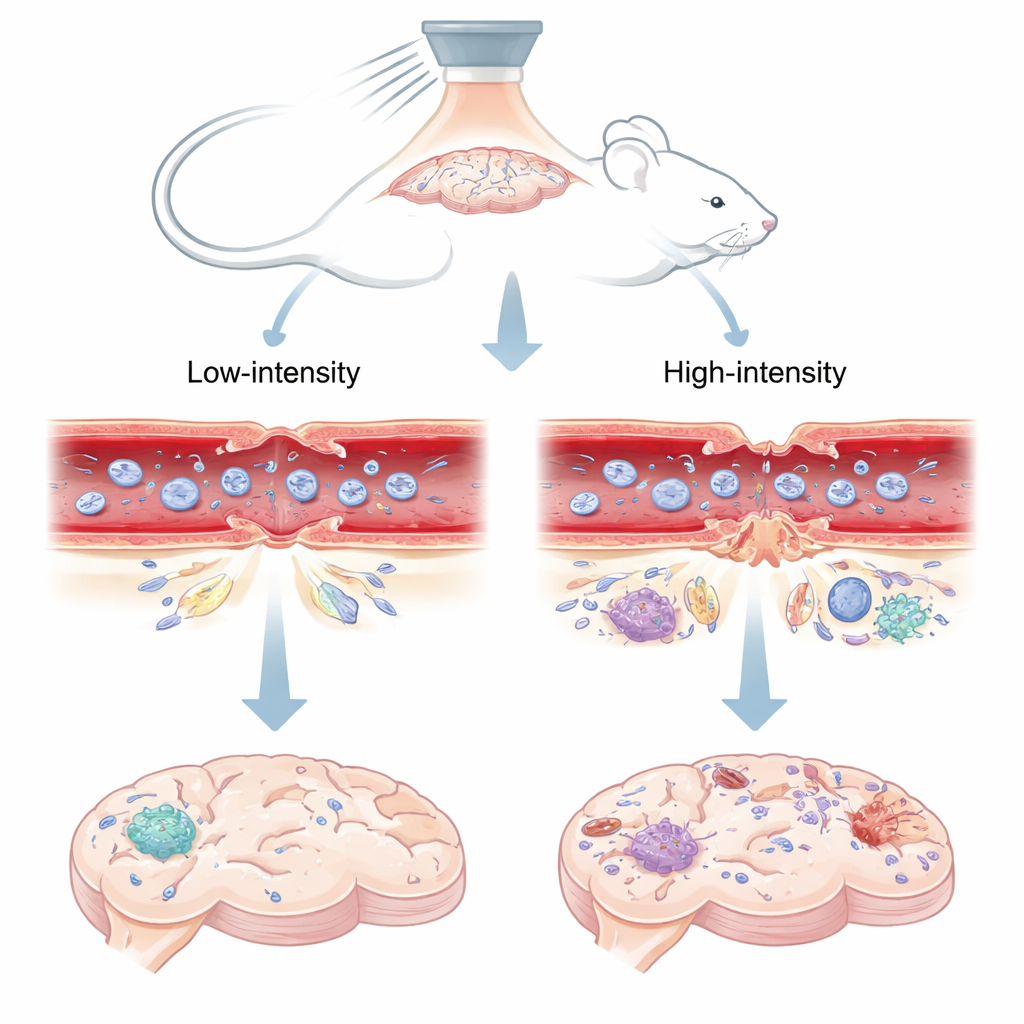
Os pesquisadores usaram ultrassom focalizado – ondas sonoras concentradas vindas de fora do crânio – combinado com microbolhas minúsculas preenchidas com gás injetadas na corrente sanguínea. Quando as ondas sonoras atingem essas microbolhas dentro dos vasos sanguíneos cerebrais, as bolhas vibram. Em pressões sonoras mais baixas, as bolhas oscilam de forma controlada; em pressões mais altas, podem entrar em colapso violento. A equipe testou dois níveis em camundongos: uma configuração “baixa” conhecida por trabalhos anteriores por abrir a barreira de forma segura e temporária, e uma configuração “alta” associada a vazamentos de maior duração e dano tecidual. Em seguida, observaram como um corante fluorescente e um agente de contraste por Ressonância Magnética se espalharam pelo cérebro, o que revelou quando e onde a barreira havia aberto e quando ela se selou novamente.
Portões microscópicos que mudam ou se rompem
A barreira hematoencefálica é formada principalmente por junções de oclusão – “zippers” proteicos que selam as células vizinhas que revestem os vasos sanguíneos cerebrais. Em camundongos especiais cujas junções de oclusão brilham ao microscópio, os cientistas puderam observar esses zippers mudarem de forma após o ultrassom. Na pressão sonora segura e baixa, as junções apresentaram pequenas lacunas temporárias tanto em capilares minúsculos quanto em arteríolas ligeiramente maiores. Em cerca de três dias, essas lacunas em grande parte se fecharam e o padrão das junções parecia muito semelhante ao do lado não tratado do cérebro, coincidindo com o fato de que o corante e o contraste por RM não vazavam mais. Na pressão mais alta, contudo, as junções não estavam apenas com lacunas, mas às vezes completamente ausentes, especialmente em vasos maiores. Essas rupturas severas persistiram por pelo menos 72 horas e foram acompanhadas por vazamento contínuo de moléculas rastreadoras.
Células imunes do cérebro e proteínas sanguíneas entram na história
A abertura da barreira também permite que proteínas sanguíneas entrem no tecido cerebral. Uma dessas proteínas, a fibrinogênio, atua na coagulação e na inflamação e está ligada a danos em várias doenças cerebrais. Logo após o ultrassom em ambas as pressões, o fibrinogênio apareceu próximo a vasos permeáveis junto com microglia ativada, as células imunes residentes do cérebro. As microglias mudaram de uma aparência ramificada e repousante para uma forma mais arredondada, de “alerta”. Em 72 horas, o fibrinogênio não era mais detectável em nenhuma das pressões, sugerindo que mesmo quando o dano às junções persistia na configuração mais alta, alguns aspectos do vazamento haviam sido resolvidos. Os pesquisadores também testaram camundongos sem cavernas (caveolas), pequenas invaginações na parede vascular que podem transportar moléculas através das células. A abertura da barreira na pressão segura não foi alterada sem essas estruturas, indicando que a reorganização das junções de oclusão – e não um aumento dessa via de transporte – é o principal mecanismo para a abertura controlada.
Como as células dos vasos respondem por dentro
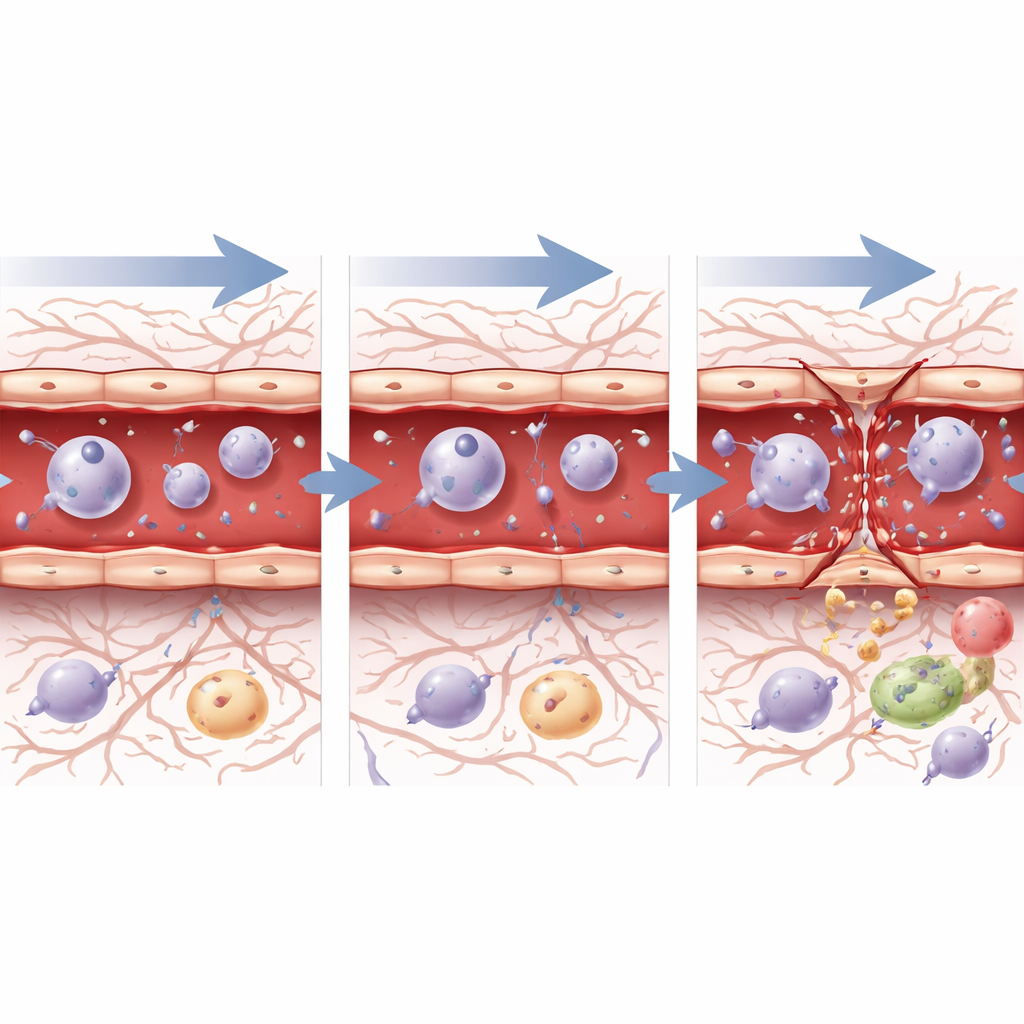
Para ver como células individuais dos vasos sanguíneos reagem ao nível genético, a equipe isolou milhares de células endoteliais – as células que revestem artérias, capilares e veias – e realizou sequenciamento de RNA de célula única. Dentro de uma hora após o ultrassom, independentemente da pressão, essas células aumentaram a expressão de genes ligados ao estresse, morte celular, inflamação e reparo, sinalizando que perceberam tanto lesão quanto a necessidade de recuperação. Em 72 horas, o quadro divergiu. Após a pressão baixa e segura, as células mostraram atividade gênica consistente com cicatrização, crescimento celular controlado e retorno gradual a um estado de barreira estável. Após a pressão mais alta, porém, as células ainda expressavam fortemente programas de estresse e resposta a ferimentos, e genes-chave para a construção das junções permaneceram suprimidos, em consonância com o dano estrutural contínuo observado ao microscópio. Vias que orientam o crescimento de vasos sanguíneos e a formação da barreira, como as sinalizações TGF-beta, Notch e Wnt, mudaram ao longo do tempo de maneiras que sugerem reparo ativo, porém incompleto, especialmente após a configuração mais agressiva.
O que isso significa para tratamentos cerebrais futuros
Para quem busca melhores terapias cerebrais, este trabalho esclarece uma questão central de segurança: como podemos abrir a barreira hematoencefálica o suficiente para permitir a entrada de medicamentos sem causar danos duradouros? O estudo mostra que, em pressões de ultrassom cuidadosamente escolhidas e mais baixas, a barreira se abre principalmente porque seus “zippers” proteicos afrouxam brevemente e então se reorganizam, com as células dos vasos sanguíneos ativando programas de reparo que fecham as lacunas em dias. Forçar o sistema mais intensamente quebra esses zippers em vez de apenas deslocá‑los, deixando vazamentos prolongados e estresse celular prolongado. Em termos práticos, as descobertas apoiam o uso de configurações conservadoras de ultrassom e monitoramento cuidadoso em aplicações clínicas, reforçando a ideia de que a entrega segura de fármacos ao cérebro depende da reorganização transitória – não da destruição – dos portões microscópicos do cérebro.
Citação: Noel, R.L., Kugelman, T., Karakatsani, M.E. et al. Safe focused ultrasound-mediated blood-brain barrier opening is driven primarily by transient reorganization of tight junctions. Commun Eng 5, 58 (2026). https://doi.org/10.1038/s44172-026-00597-5
Palavras-chave: ultrassom focalizado, barreira hematoencefálica, entrega de fármacos, vasos sanguíneos cerebrais, microbolhas