Clear Sky Science · pl
Bezpieczne otwieranie bariery krew–mózg przy użyciu ukierunkowanego ultradźwięku jest napędzane przede wszystkim przez przejściową reorganizację połączeń zamykających
Dlaczego otwarcie „bramy” mózgu ma znaczenie
Wiele z najbardziej obiecujących terapii choroby Alzheimera, nowotworów mózgu i innych schorzeń neurologicznych nigdy nie dociera do swoich celów, ponieważ mózg chroniony jest przez mikroskopijnego strażnika zwanego barierą krew–mózg. Ta bariera chroni delikatną tkankę nerwową przed szkodliwymi substancjami we krwi, ale także blokuje większość przydatnych leków. Opisane badanie bada nieinwazyjny sposób krótkotrwałego otwarcia tej bariery za pomocą skoncentrowanych fal dźwiękowych i pokazuje, co dzieje się z naczyniami mózgowymi, gdy podejście stosuje się łagodnie w porównaniu z nadmiernie agresywnym.
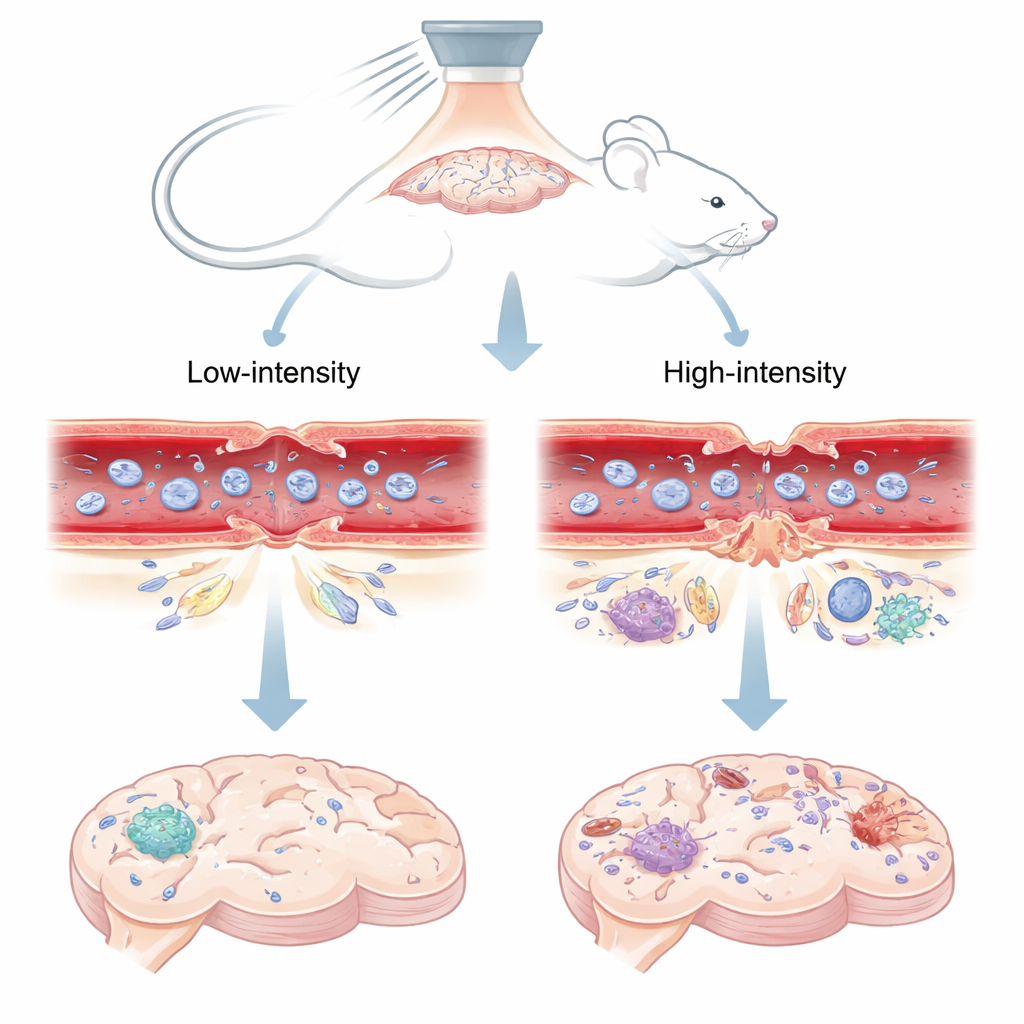
Dźwiękowe drzwi do mózgu
Naukowcy użyli ukierunkowanego ultradźwięku – skoncentrowanych fal dźwiękowych z zewnątrz czaszki – w połączeniu z drobnymi, wypełnionymi gazem pęcherzykami wstrzykniętymi do krwiobiegu. Gdy fale dźwiękowe trafiają w te mikropęcherzyki wewnątrz naczyń mózgowych, pęcherzyki wibrują. Przy niższych ciśnieniach dźwięku pęcherzyki kołyszą się w kontrolowany sposób; przy wyższych ciśnieniach mogą gwałtownie zawalić się. Zespół przetestował dwa poziomy u myszy: ustawienie „niskie” znane z wcześniejszych prac jako bezpieczne i krótkotrwałe otwierające barierę oraz ustawienie „wysokie” związane z dłużej utrzymującymi się przeciekami i uszkodzeniem tkanki. Następnie obserwowano, jak barwnik fluorescencyjny i kontrast do MRI rozprzestrzeniają się w mózgu, co ujawniło, kiedy i gdzie bariera została otwarta i kiedy się ponownie zamknęła.
Mikroskopijne zamki, które przesuwają się lub kruszą
Bariera krew–mózg jest w głównej mierze tworzona przez połączenia typu tight junction – białkowe „zameczki” uszczelniające sąsiednie komórki wyściełające naczynia mózgowe. U specjalnych myszy, których te połączenia świecą pod mikroskopem, naukowcy mogli obserwować, jak te zameczki zmieniają kształt po ekspozycji na ultradźwięki. Przy bezpiecznym, niskim ciśnieniu dźwięku połączenia ujawniały małe, przejściowe szczeliny zarówno w drobnych kapilarach, jak i w nieco większych arterioleach. W ciągu około trzech dni te szczeliny w dużej mierze się zamykały, a układ połączeń wyglądał bardzo podobnie do nieleczonej strony mózgu, co odpowiadało temu, że barwnik i kontrast MRI przestały przenikać. Przy wyższym ciśnieniu jednak połączenia nie tylko były rozdzielone, lecz czasami całkowicie brakowało ich fragmentów, zwłaszcza w większych naczyniach. Te poważne przerwy utrzymywały się przez co najmniej 72 godziny i towarzyszyło im dalsze wyciekanie cząsteczek znacznikowych.
W komórkach odpornościowych mózgu i białkach krwi także pojawia się odpowiedź
Otwieranie bariery pozwala również białkom krwi wnikać do tkanki mózgowej. Jedno z takich białek, fibrynogen, bierze udział w krzepnięciu i zapaleniu i wiąże się ze szkodami w kilku chorobach mózgu. Krótko po ultradźwiękach przy obu ciśnieniach fibrynogen pojawiał się w pobliżu nieszczelnych naczyń wraz z aktywowanymi mikroglejem, rezydentnymi komórkami odpornościowymi mózgu. Mikroglej zmieniał wygląd z wypoczętego, rozgałęzionego na bardziej okrągły, „w trybie czujności”. Po 72 godzinach fibrynogen nie był już wykrywalny przy żadnym z ciśnień, co sugeruje, że nawet gdy uszkodzenia połączeń utrzymywały się przy wyższym ustawieniu, niektóre aspekty przecieku uległy rozwiązaniu. Naukowcy badali także myszy pozbawione kaweloi – maleńkich kieszonek w ścianie naczynia, które mogą transportować cząsteczki przez komórki. Otwarcie bariery przy bezpiecznym ciśnieniu nie zmieniło się w ich braku, co wskazuje, że głównym mechanizmem kontrolowanego otwarcia była reorganizacja połączeń zamykających, a nie zwiększenie tego szlaku transportowego.
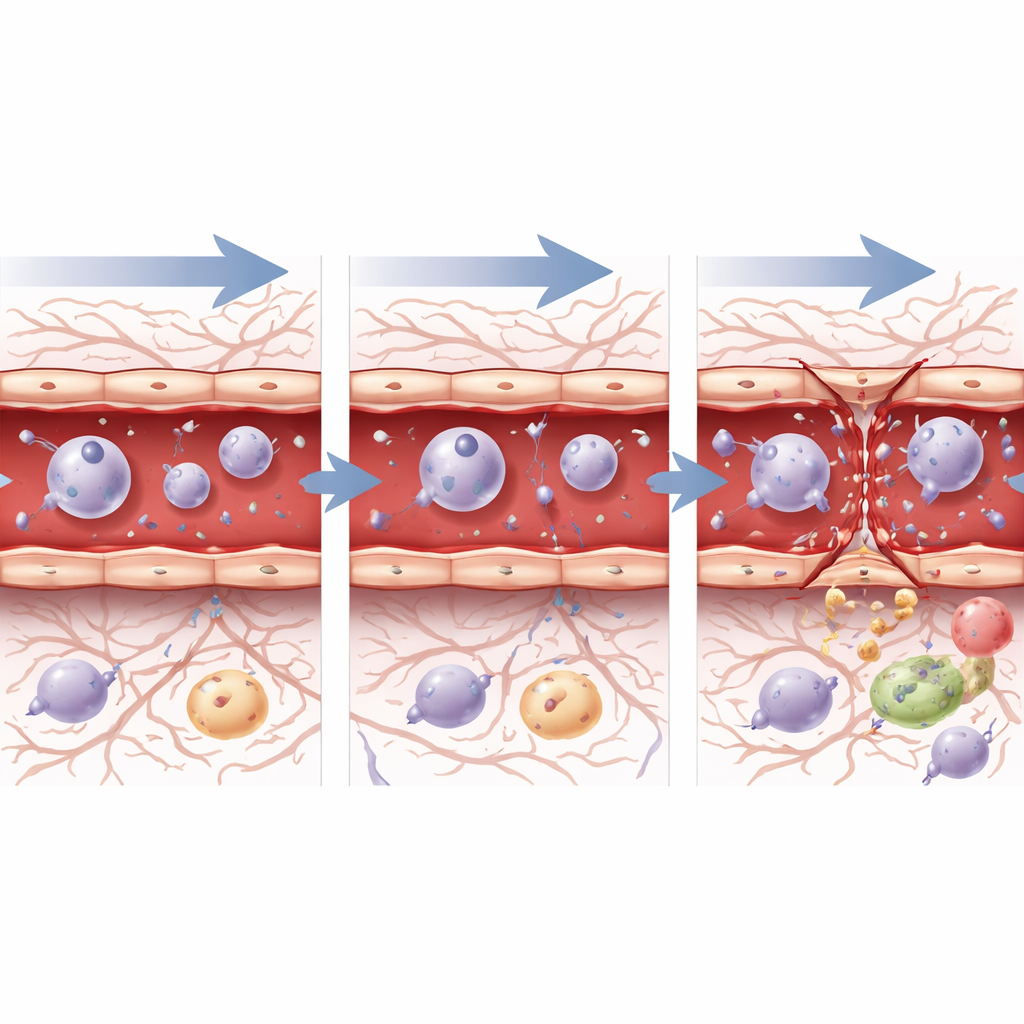
Jak komórki naczyń krwionośnych reagują od środka
Aby zobaczyć, jak pojedyncze komórki naczyń reagują na poziomie genetycznym, zespół izolował tysiące komórek śródbłonka – komórek wyściełających tętnice, kapilary i żyły – i przeprowadził sekwencjonowanie RNA pojedynczych komórek. W ciągu godziny od ultradźwięków, niezależnie od ciśnienia, komórki te zwiększyły aktywność genów związanych ze stresem, śmiercią komórkową, zapaleniem i naprawą, sygnalizując, że rozpoznały zarówno uraz, jak i potrzebę odzyskania równowagi. Po 72 godzinach obraz się rozszedł. Po bezpiecznym, niskim ciśnieniu komórki wykazywały aktywność genów zgodną z gojeniem się ran, kontrolowanym wzrostem komórek i stopniowym powrotem do stabilnego stanu bariery. Po wyższym ciśnieniu komórki nadal silnie wyrażały programy związane ze stresem i reakcją na uraz, a kluczowe geny budujące połączenia pozostawały stłumione, co zgadza się z trwającymi uszkodzeniami strukturalnymi obserwowanymi pod mikroskopem. Szlaki kierujące wzrostem naczyń i formowaniem bariery, takie jak sygnalizacja TGF-beta, Notch i Wnt, zmieniały się w czasie w sposób sugerujący aktywną, lecz niepełną naprawę, szczególnie po bardziej agresywnym ustawieniu.
Co to oznacza dla przyszłych terapii mózgu
Dla osób liczących na lepsze terapie mózgowe ta praca wyjaśnia kluczowe pytanie dotyczące bezpieczeństwa: jak otworzyć barierę krew–mózg wystarczająco, by wpuścić leki, nie powodując trwałych szkód? Badanie pokazuje, że przy starannie dobranych, niższych ciśnieniach ultradźwięku bariera otwiera się głównie dlatego, że jej białkowe „zameczki” chwilowo poluzowują się, a następnie reorganizują, przy czym komórki naczyniowe uruchamiają programy naprawcze, które zamykają szczeliny w ciągu dni. Silniejsze działanie rozbija te zameczki zamiast je przesunąć, powodując przedłużone przecieki i długotrwały stres komórkowy. W praktycznym wymiarze wyniki te wspierają stosowanie zachowawczych ustawień ultradźwięku i uważne monitorowanie w zastosowaniach klinicznych, wzmacniając ideę, że bezpieczne dostarczanie leków do mózgu zależy od przejściowej reorganizacji – a nie niszczenia – mikroskopijnych bram mózgu.
Cytowanie: Noel, R.L., Kugelman, T., Karakatsani, M.E. et al. Safe focused ultrasound-mediated blood-brain barrier opening is driven primarily by transient reorganization of tight junctions. Commun Eng 5, 58 (2026). https://doi.org/10.1038/s44172-026-00597-5
Słowa kluczowe: ukierunkowany ultradźwięk, bariera krew–mózg, dostarczanie leków, naczynia krwionośne mózgu, mikropęcherzyki