Clear Sky Science · es
Apertura segura de la barrera hematoencefálica mediada por ultrasonidos focalizados se debe principalmente a la reorganización transitoria de las uniones estrechas
Por qué importa abrir la puerta del cerebro
Muchos de los tratamientos más prometedores para la enfermedad de Alzheimer, los tumores cerebrales y otras afecciones neurológicas nunca alcanzan sus objetivos porque el cerebro está protegido por un guardián microscópico llamado barrera hematoencefálica. Esta barrera protege el delicado tejido nervioso de sustancias nocivas en la sangre, pero también bloquea la mayoría de los medicamentos útiles. El estudio resumido aquí explora una forma no invasiva de abrir brevemente esa barrera con ondas sonoras concentradas, revelando qué ocurre en los vasos sanguíneos cerebrales cuando el método se aplica con calma frente a cuando se aplica de forma demasiado agresiva.
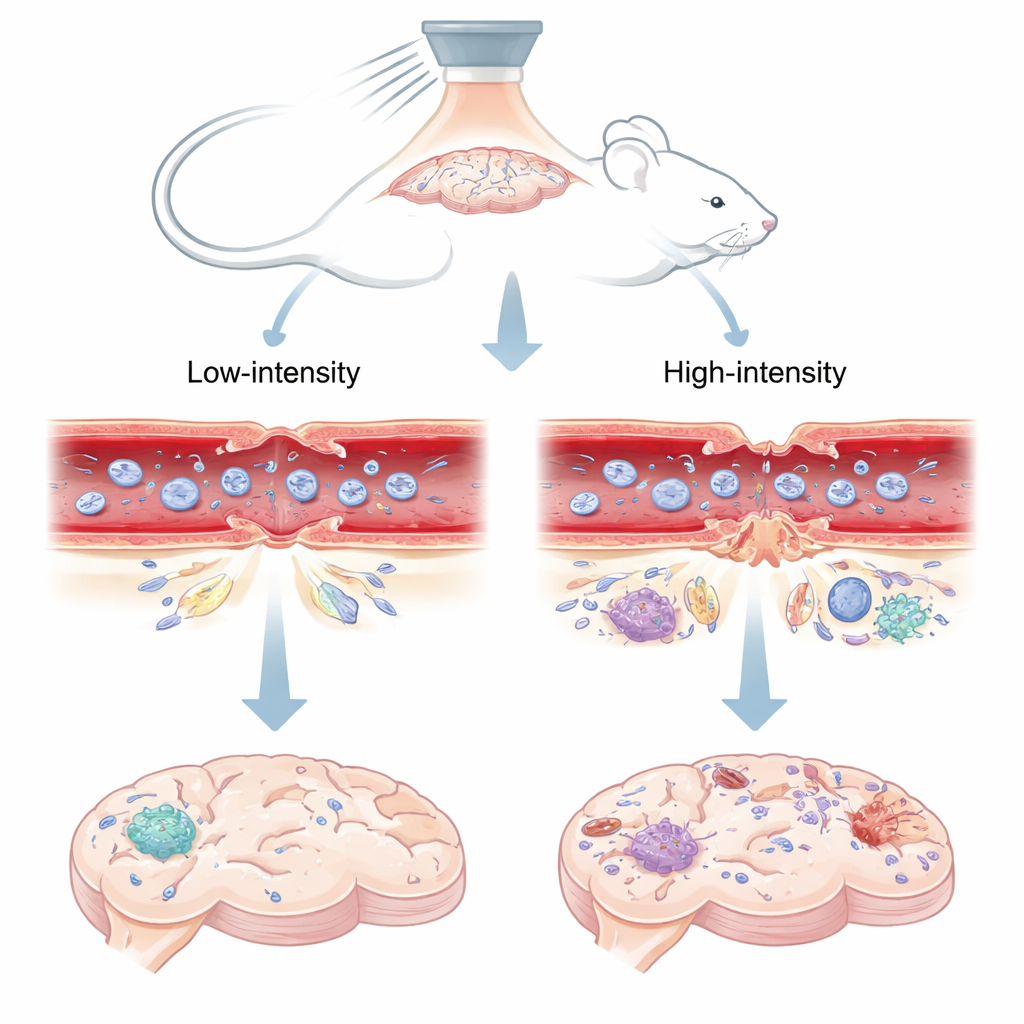
Una puerta al cerebro impulsada por sonido
Los investigadores emplearon ultrasonidos focalizados: ondas sonoras concentradas desde fuera del cráneo, combinados con diminutas burbujas rellenas de gas inyectadas en el torrente sanguíneo. Cuando las ondas sonoras alcanzan estas microburbujas dentro de los vasos cerebrales, las burbujas vibran. A presiones sonoras más bajas, las burbujas oscilan de forma controlada; a presiones más altas pueden colapsar violentamente. El equipo probó dos niveles en ratones: un ajuste “bajo” conocido por trabajos previos que abre la barrera de forma segura y breve, y un ajuste “alto” asociado con fugas más duraderas y daño tisular. Luego observaron cómo se difundían un tinte fluorescente y un agente de contraste para resonancia magnética en el cerebro, lo que reveló cuándo y dónde la barrera se había abierto y cuándo se volvió a sellar.
Portones microscópicos que se desplazan o se rompen
La barrera hematoencefálica se forma principalmente por uniones estrechas: “cierres” proteicos que sellan las células vecinas que recubren los vasos sanguíneos cerebrales. En ratones especiales cuyas uniones estrechas brillan bajo el microscopio, los científicos pudieron observar estos cierres cambiar de forma tras la aplicación de ultrasonidos. A la presión sonora segura y baja, las uniones mostraron pequeñas brechas temporales tanto en capilares diminutos como en arteriolas algo mayores. En alrededor de tres días, esas brechas se cerraron en gran medida y el patrón de las uniones se parecía mucho al lado intacto del cerebro, lo que coincidía con el hecho de que el tinte y el contraste de la RM ya no se filtraban. Sin embargo, a la presión más alta, las uniones no solo presentaban huecos, sino que a veces faltaban por completo, especialmente en vasos de mayor calibre. Estas rupturas graves persistieron al menos 72 horas y estuvieron acompañadas de filtración continuada de moléculas trazadoras.
Las células inmunitarias cerebrales y las proteínas sanguíneas se suman al relato
Abrir la barrera también permite que proteínas sanguíneas entren en el tejido cerebral. Una de ellas, la fibrinógeno, participa en la coagulación y la inflamación y se asocia con daño en varias enfermedades cerebrales. Poco después de aplicar ultrasonidos a ambas presiones, la fibrinógeno apareció cerca de vasos permeables junto con microglía activada, las células inmunitarias residentes del cerebro. Las microglías pasaron de una apariencia ramificada y en reposo a una forma más redondeada, “en alerta”. A las 72 horas, la fibrinógeno ya no era detectable en ninguno de los dos ajustes, lo que sugiere que incluso cuando el daño en las uniones persistía con la presión más alta, algunos aspectos de la fuga se habían resuelto. Los investigadores también evaluaron ratones sin caveolas, diminutos bolsillos en la pared vascular que pueden transportar moléculas a través de las células. La apertura de la barrera a la presión segura no cambió en ausencia de estas estructuras, lo que apunta a la reorganización de las uniones estrechas —no a un aumento de esta vía de transporte— como el mecanismo principal de una apertura controlada.
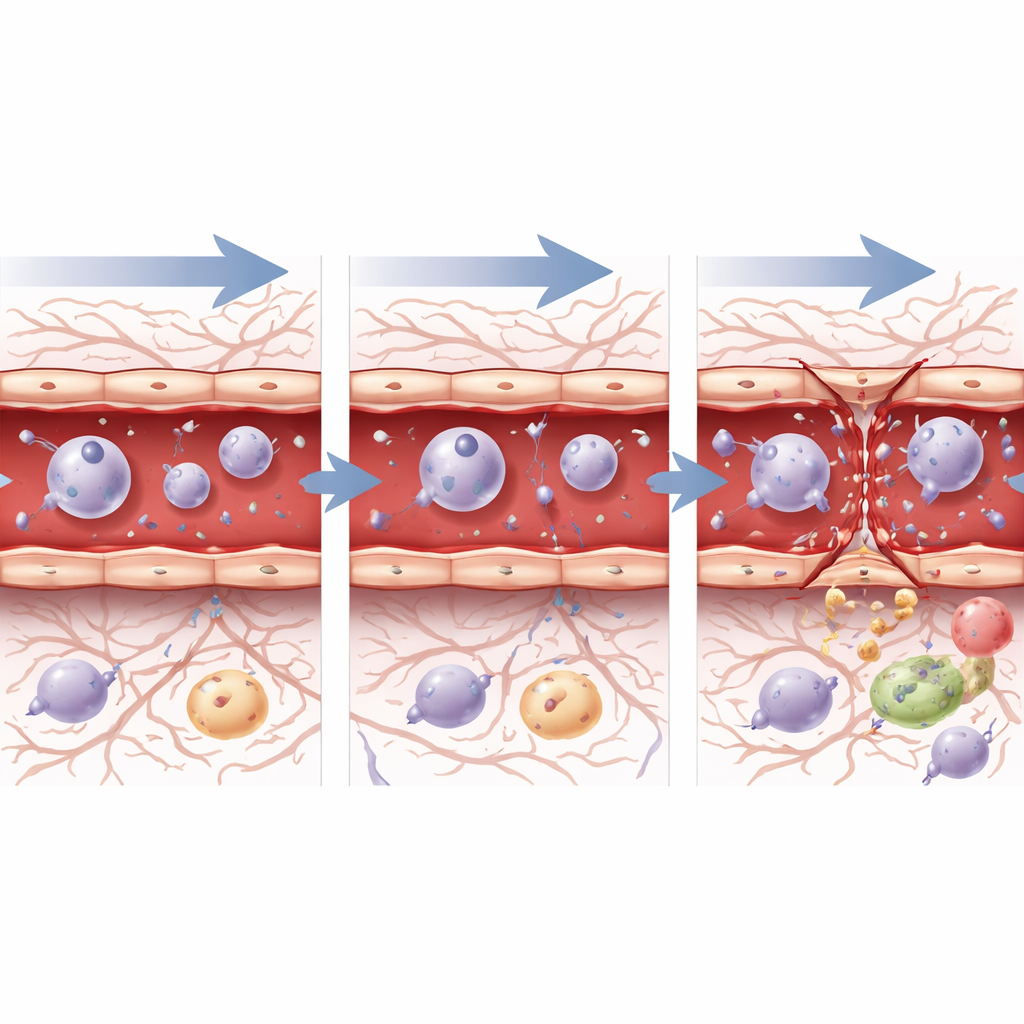
Cómo responden desde dentro las células de los vasos
Para ver cómo reaccionan a nivel genético las células individuales de los vasos sanguíneos, el equipo aisló miles de células endoteliales —las que recubren arterias, capilares y venas— y realizó secuenciación de ARN de célula única. En la primera hora tras los ultrasonidos, independientemente de la presión, estas células aumentaron la expresión de genes ligados al estrés, la muerte celular, la inflamación y la reparación, lo que indica que percibían tanto daño como la necesidad de recuperación. A las 72 horas, el panorama divergia. Tras la presión segura y baja, las células mostraron actividad génica consistente con la cicatrización, el control del crecimiento celular y un retorno gradual hacia un estado de barrera estable. Tras la presión más alta, sin embargo, las células seguían expresando con fuerza programas de estrés y de respuesta a heridas, y genes clave para formar uniones permanecían reprimidos, en línea con el daño estructural persistente observado al microscopio. Vías que guían el crecimiento vascular y la formación de la barrera, como TGF-beta, Notch y la señalización Wnt, cambiaron con el tiempo de maneras que sugerían reparación activa pero incompleta, especialmente tras el ajuste más agresivo.
Qué significa esto para futuros tratamientos cerebrales
Para quienes esperan mejores terapias cerebrales, este trabajo aclara una cuestión central de seguridad: ¿cómo podemos abrir la barrera hematoencefálica lo suficiente para dejar pasar fármacos sin causar daño duradero? El estudio muestra que con presiones de ultrasonido cuidadosamente elegidas y menores, la barrera se abre principalmente porque sus “cierres” proteicos se aflojan brevemente y luego se reorganizan, con células vasculares que activan programas de reparación que cierran las brechas en días. Forzar el sistema con mayor intensidad rompe esos cierres en vez de desplazarlos, dejando fugas prolongadas y sufrimiento celular sostenido. En términos prácticos, los hallazgos respaldan el uso de ajustes conservadores de ultrasonido y un monitoreo cuidadoso en aplicaciones clínicas, reforzando la idea de que la administración segura de fármacos al cerebro depende de la reorganización transitoria —no de la destrucción— de las puertas microscópicas del cerebro.
Cita: Noel, R.L., Kugelman, T., Karakatsani, M.E. et al. Safe focused ultrasound-mediated blood-brain barrier opening is driven primarily by transient reorganization of tight junctions. Commun Eng 5, 58 (2026). https://doi.org/10.1038/s44172-026-00597-5
Palabras clave: ultrasonidos focalizados, barrera hematoencefálica, administración de fármacos, vasos sanguíneos cerebrales, microburbujas