Clear Sky Science · it
Una chiusura sicura della barriera emato-encefalica mediata da ultrasuoni focalizzati è guidata principalmente da una riorganizzazione transitoria delle giunzioni strette
Perché aprire la porta del cervello è importante
Molti dei trattamenti più promettenti per l’alzheimer, i tumori cerebrali e altre condizioni neurologiche non raggiungono mai i loro bersagli, perché il cervello è protetto da un guardiano microscopico chiamato barriera emato-encefalica. Questa barriera protegge il delicato tessuto nervoso da sostanze nocive nel sangue, ma blocca anche la maggior parte dei farmaci utili. Lo studio riassunto qui esplora un modo non invasivo per aprire temporaneamente questa barriera con onde sonore focalizzate, rivelando cosa succede ai vasi sanguigni cerebrali quando l’approccio viene usato con cautela rispetto a quando è troppo aggressivo.
Una porta nel cervello alimentata dal suono
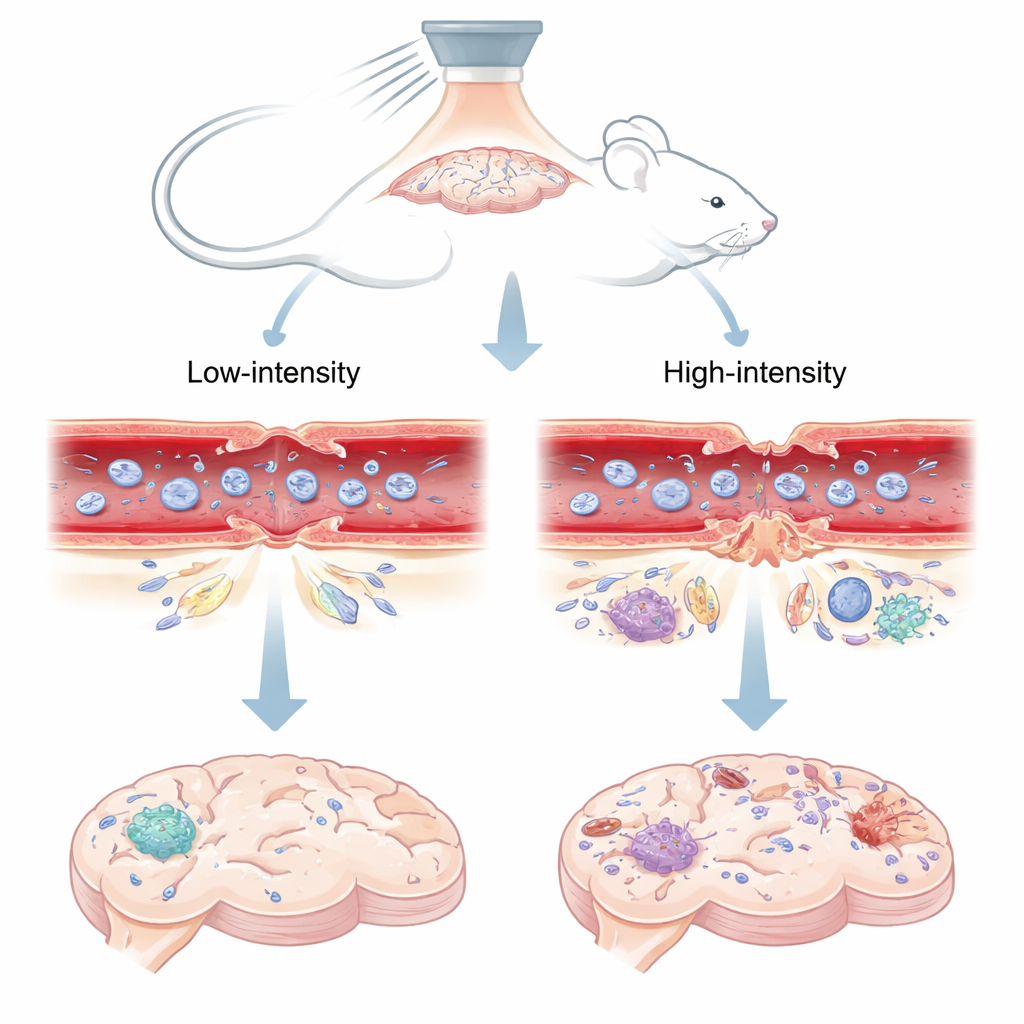
I ricercatori hanno usato ultrasuoni focalizzati — onde sonore concentrate dall’esterno del cranio — combinati con piccolissime bolle di gas iniettate nel flusso sanguigno. Quando le onde sonore colpiscono queste microbolle all’interno dei vasi cerebrali, le bolle vibrano. A pressioni sonore più basse le bolle oscillano in modo controllato; a pressioni più alte possono collassare violentemente. Il team ha testato due livelli nei topi: un’impostazione “bassa” nota da lavori precedenti per aprire la barriera in modo sicuro e temporaneo, e un’impostazione “alta” associata a perdite più durature e a danni al tessuto. Hanno quindi osservato come un colorante fluorescente e un agente di contrasto per risonanza magnetica si diffondevano nel cervello, il che ha rivelato quando e dove la barriera si era aperta e quando si era richiusa.
Gate microscopici che si spostano o si frantumano
La barriera emato-encefalica è formata principalmente da giunzioni strette — “cerniere” proteiche che sigillano le cellule adiacenti che rivestono i vasi sanguigni cerebrali. In topi speciali le cui giunzioni strette brillano al microscopio, gli scienziati hanno potuto osservare queste cerniere cambiare forma dopo l’ultrasuono. Alla pressione sonora bassa e sicura, le giunzioni mostravano piccole lacune temporanee sia nei capillari minuscoli sia nelle arteriole leggermente più grandi. Entro circa tre giorni quelle lacune si richiudevano in gran parte e il pattern delle giunzioni appariva molto simile al lato non trattato del cervello, corrispondendo al fatto che il colorante e il contrasto per risonanza magnetica non fuoriuscivano più. Alla pressione più alta, invece, le giunzioni non erano soltanto separate ma talvolta completamente assenti, specialmente nei vasi più grandi. Queste rotture gravi persistevano per almeno 72 ore ed erano accompagnate da una continua fuoriuscita di molecole traccianti.
Cellule immunitarie cerebrali e proteine del sangue entrano in scena
L’apertura della barriera permette anche alle proteine del sangue di entrare nel tessuto cerebrale. Una di queste proteine, la fibrinogeno, ha ruoli nella coagulazione e nell’infiammazione ed è collegata a danni in varie patologie cerebrali. Poco dopo l’ultrasuono a entrambe le pressioni, il fibrinogeno compariva vicino ai vasi che perdevano insieme a microglia attivata, le cellule immunitarie residenti del cervello. Le microglia passavano da un aspetto ramificato e quiescente a una forma più arrotondata e “in allerta”. Dopo 72 ore, il fibrinogeno non era più rilevabile per entrambe le pressioni, suggerendo che anche quando il danno alle giunzioni persisteva all’impostazione più alta, alcuni aspetti della perdita si erano risolti. I ricercatori hanno anche testato topi privi di caveole, piccole tasche nella parete vascolare che possono trasportare molecole attraverso le cellule. L’apertura della barriera alla pressione sicura non è cambiata in assenza di queste strutture, indicando che la riorganizzazione delle giunzioni strette — non un aumento di questa via di trasporto — è il principale meccanismo per un’apertura controllata.
Come rispondono dall’interno le cellule dei vasi sanguigni
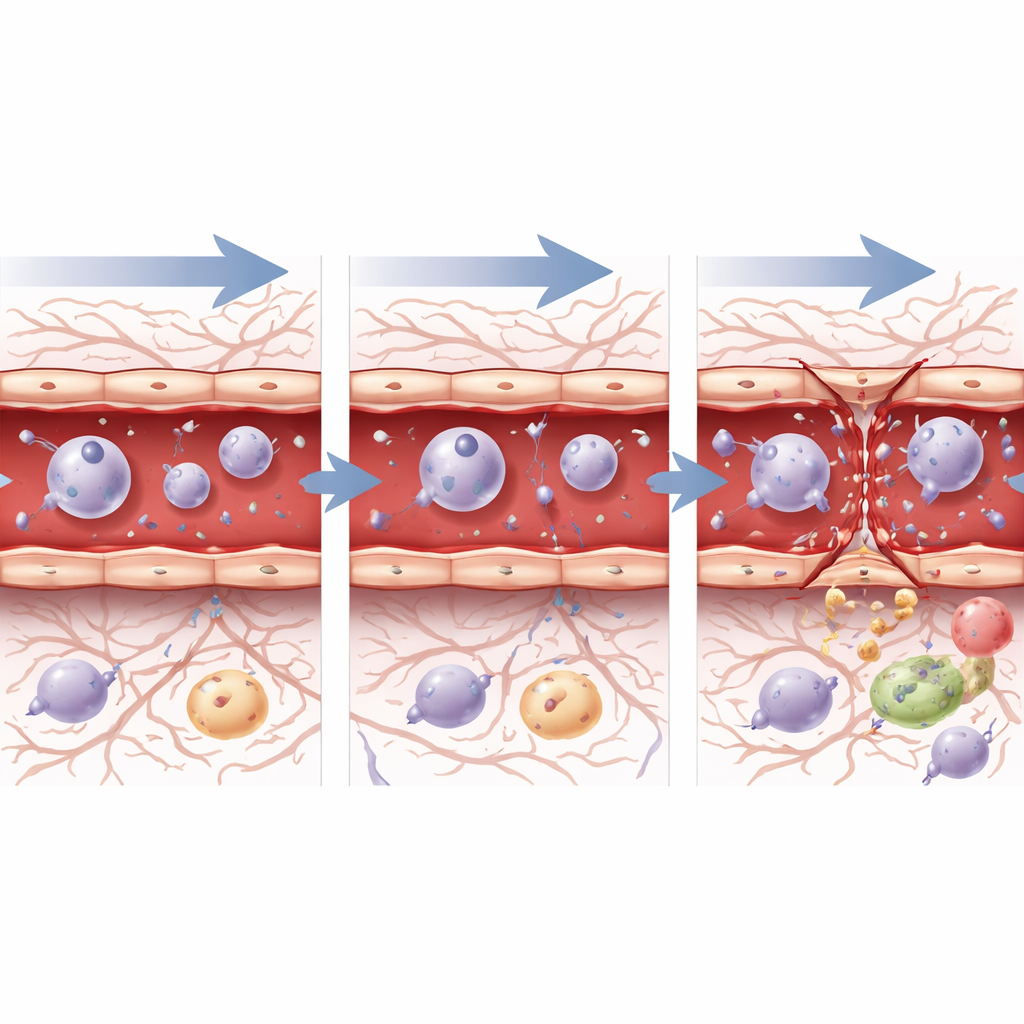
Per vedere come le singole cellule vascolari reagiscono a livello genetico, il team ha isolato migliaia di cellule endoteliali — le cellule che rivestono arterie, capillari e vene — e ha effettuato il sequenziamento dell’RNA a singola cellula. Entro un’ora dall’ultrasuono, indipendentemente dalla pressione, queste cellule hanno aumentato l’attività genica legata allo stress, alla morte cellulare, all’infiammazione e alla riparazione, segnalando che percepivano sia un danno sia la necessità di recupero. Dopo 72 ore, il quadro è divergente. Dopo la pressione bassa e sicura, le cellule mostravano attività genica coerente con la guarigione delle ferite, una crescita cellulare controllata e un graduale ritorno verso uno stato di barriera stabile. Dopo la pressione più alta, invece, le cellule esprimevano ancora fortemente programmi di stress e risposta alle ferite, e i geni chiave per la costruzione delle giunzioni restavano soppressi, in accordo con il danno strutturale persistente osservato al microscopio. Le vie che guidano la crescita dei vasi e la formazione della barriera, come la segnalazione TGF-beta, Notch e Wnt, si sono modificate nel tempo in modo coerente con una riparazione attiva ma incompleta, specialmente dopo l’impostazione più aggressiva.
Cosa significa per i futuri trattamenti cerebrali
Per chi spera in terapie cerebrali migliori, questo lavoro chiarisce una domanda centrale di sicurezza: come possiamo aprire la barriera emato-encefalica a sufficienza per far entrare i farmaci, senza causare danni duraturi? Lo studio mostra che a pressioni ultrasoniche basse e scelte con cura, la barriera si apre principalmente perché le sue “cerniere” proteiche si allentano brevemente e poi si riorganizzano, con le cellule vascolari che attivano programmi di riparazione che chiudono le lacune entro giorni. Spingere il sistema oltre rompe quelle cerniere invece di spostarle, lasciando perdite prolungate e disagio cellulare prolungato. In termini pratici, i risultati supportano l’uso di impostazioni ultrasoniche conservative e un monitoraggio accurato nelle applicazioni cliniche, rafforzando l’idea che una somministrazione sicura di farmaci al cervello dipende dalla riorganizzazione transitoria — non dalla distruzione — delle porte microscopiche del cervello.
Citazione: Noel, R.L., Kugelman, T., Karakatsani, M.E. et al. Safe focused ultrasound-mediated blood-brain barrier opening is driven primarily by transient reorganization of tight junctions. Commun Eng 5, 58 (2026). https://doi.org/10.1038/s44172-026-00597-5
Parole chiave: ultrasuoni focalizzati, barriera emato-encefalica, somministrazione di farmaci, vasi sanguigni cerebrali, microbolle