Clear Sky Science · nl
Veilige, via gefocuste ultrageluid gemedieerde opening van de bloed‑hersenbarrière wordt voornamelijk veroorzaakt door tijdelijke reorganisatie van tight junctions
Waarom het openen van de poort van de hersenen ertoe doet
Veel van de veelbelovende behandelingen voor de ziekte van Alzheimer, hersentumoren en andere neurologische aandoeningen bereiken hun doel niet, omdat de hersenen worden beschermd door een microscopische poortwachter genaamd de bloed‑hersenbarrière. Deze barrière beschermt kwetsbaar zenuwweefsel tegen schadelijke stoffen in het bloed, maar blokkeert ook de meeste behulpzame medicijnen. De hier samengevatte studie onderzoekt een niet‑invasieve manier om deze barrière kortstondig te openen met gefocuste geluidsgolven, en toont wat er met de hersenbloedvaten gebeurt wanneer de benadering voorzichtig wordt toegepast versus te agressief.
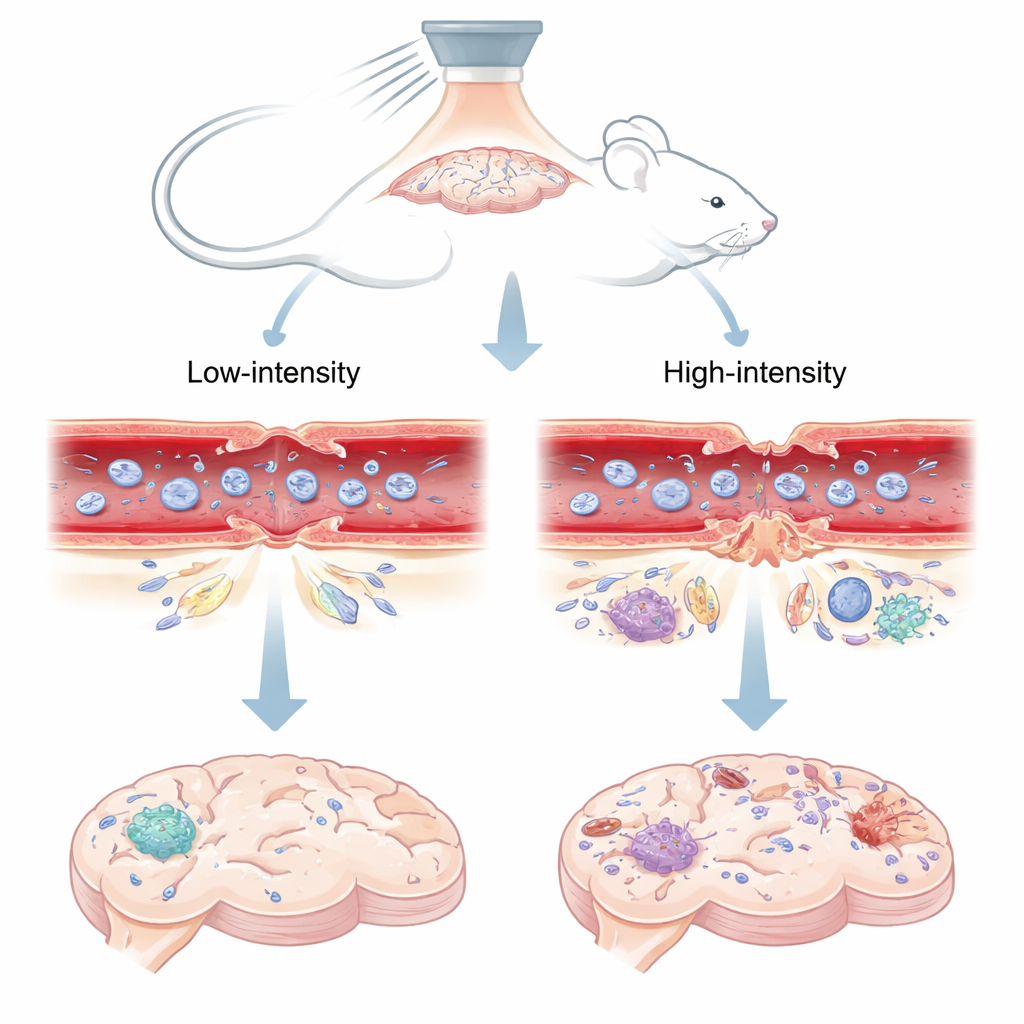
Een door geluid aangedreven deur naar de hersenen
Onderzoekers gebruikten gefocust ultrageluid – geconcentreerde geluidsgolven van buiten de schedel – gecombineerd met piepkleine met gas gevulde belletjes die in de bloedbaan werden geïnjecteerd. Wanneer de geluidsgolven deze microbellen in de hersenbloedvaten raken, gaan de belletjes trillen. Bij lagere geluidsdrukken wiebelen de belletjes op gecontroleerde wijze; bij hogere drukken kunnen ze heftig imploderen. Het team testte twee niveaus bij muizen: een "laag" niveau dat uit eerder werk bekend is als veilig en kortdurend in het openen van de barrière, en een "hoog" niveau dat geassocieerd wordt met langduriger lekkage en weefselschade. Vervolgens volgden ze hoe een fluorescente kleurstof en een MRI‑contrastmiddel in de hersenen verspreidden, wat onthulde wanneer en waar de barrière geopend was en wanneer ze weer sloot.
Microscopische poorten die verschuiven of verbrijzelen
De bloed‑hersenbarrière wordt voornamelijk gevormd door tight junctions – eiwit‑"ritsen" die naburige cellen bekleden die de bloedvaten in de hersenen bedekken afdichten. In speciale muizen waarvan de tight junctions oplichten onder het microscoop, konden de wetenschappers deze ritsen zien veranderen van vorm na ultrageluid. Bij de veilige, lage geluidsdruk toonden de junctions kleine, tijdelijke openingen in zowel kleine capillairen als iets grotere arteriolen. Binnen ongeveer drie dagen sloten die openingen grotendeels en leek het patroon van junctions sterk op de onaangetaste zijde van de hersenen, wat overeenkomt met het feit dat kleurstof en MRI‑contrast niet langer lekte. Bij de hogere druk waren de junctions echter niet alleen geopend maar soms volledig verdwenen, vooral in grotere vaten. Deze ernstige breuken hielden ten minste 72 uur aan en gingen gepaard met aanhoudende lekkage van tracer‑moleculen.
Hersenimmuuncellen en bloedproteïnen voegen zich bij het verhaal
Het openen van de barrière laat ook bloedproteïnen het hersenweefsel binnendringen. Één zo’n eiwit, fibrinogeen, speelt een rol bij stolling en ontsteking en wordt in verband gebracht met schade bij verschillende hersenziekten. Kort na ultrageluid bij beide drukken verscheen fibrinogeen nabij lekkende vaten, samen met geactiveerde microgliacellen, de residentiële immuuncellen van de hersenen. De microglia veranderden van een rustende, vertakte verschijning naar een ronder, "waakzaam" uiterlijk. Na 72 uur was fibrinogeen voor beide drukken niet langer detecteerbaar, wat suggereert dat zelfs wanneer junction‑schade bij de hogere instelling aanhield, sommige aspecten van de lekkage waren opgelost. De onderzoekers testten ook muizen zonder caveolae, kleine zakjes in de vaatwand die moleculen door cellen kunnen vervoeren. Het openen van de barrière bij de veilige druk veranderde niet zonder deze structuren, wat wijst op reorganisatie van tight junctions — niet een toename van dit transportpad — als het belangrijkste mechanisme voor gecontroleerde opening.
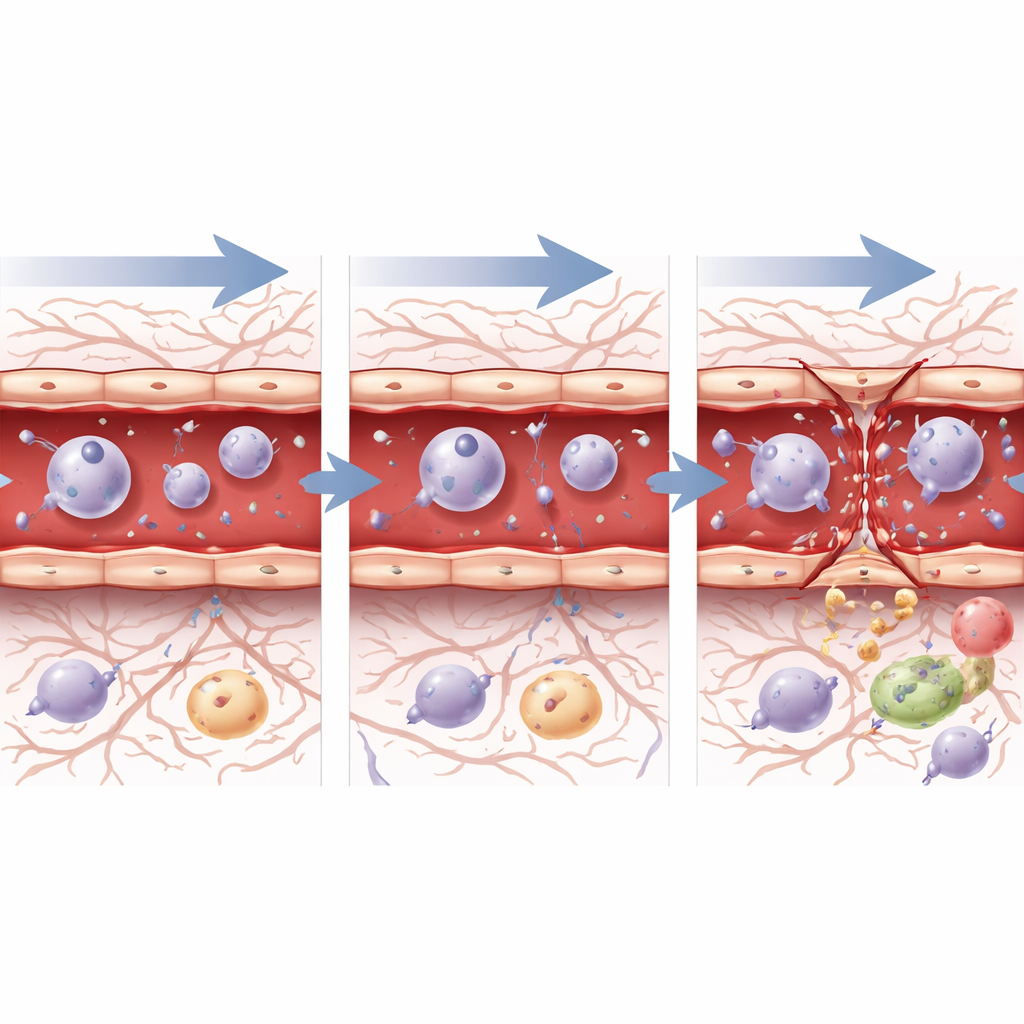
Hoe vatencellen van binnenuit reageren
Om te zien hoe individuele vatencellen op genetisch niveau reageren, is het team duizenden endotheelcellen — de cellen die arteriën, capillairen en venen bekleden —ole geïsoleerd en onderwierp men ze aan single‑cell RNA‑sequencing. Binnen een uur na ultrageluid, ongeacht de druk, zetten deze cellen genen aan die verband houden met stress, celdood, ontsteking en herstel, wat aangeeft dat ze zowel letsel voelden als het noodzaak tot herstel signaleerden. Na 72 uur splitste het beeld zich. Na de veilige, lage druk vertoonden cellen genactiviteit die consistent was met wondgenezing, gecontroleerde celgroei en een geleidelijke terugkeer naar een stabiele barrière‑toestand. Na de hogere druk echter, bleven cellen sterk stress‑ en "wondrespons" programma’s tot expressie brengen, en bleven sleutelgenen voor het bouwen van junctions onderdrukt, wat overeenkomt met de aanhoudende structurele schade die onder de microscoop werd gezien. Pathways die de groei van bloedvaten en barrièrevorming sturen, zoals TGF‑beta, Notch en Wnt‑signaleringsroutes, verschoven in de loop van de tijd op manieren die wezen op actief maar onvolledig herstel, vooral na de agressievere instelling.
Wat dit betekent voor toekomstige hersenbehandelingen
Voor mensen die hopen op betere hersentherapieën verduidelijkt dit werk een centrale veiligheidvraag: hoe kunnen we de bloed‑hersenbarrière voldoende openen om medicijnen binnen te laten, zonder blijvende schade toe te brengen? De studie toont aan dat bij zorgvuldig gekozen, lagere ultrageluiddrukken de barrière voornamelijk opent omdat de eiwit‑"ritsen" tijdelijk losser worden en zich vervolgens reorganiseren, waarbij vatencellen herstelprogramma’s activeren die de openingen binnen enkele dagen sluiten. Het harder pushen van het systeem verbrijzelt die ritsen in plaats van ze slechts te verschuiven, waardoor langdurige lekkages en aanhoudende cellulaire stress ontstaan. In praktische zin ondersteunen de bevindingen het gebruik van conservatieve ultrageluidinstellingen en zorgvuldige monitoring in klinische toepassingen, en versterken ze het idee dat veilige levering van geneesmiddelen aan de hersenen afhangt van tijdelijke reorganisatie — niet vernietiging — van de microscopische poorten van de hersenen.
Bronvermelding: Noel, R.L., Kugelman, T., Karakatsani, M.E. et al. Safe focused ultrasound-mediated blood-brain barrier opening is driven primarily by transient reorganization of tight junctions. Commun Eng 5, 58 (2026). https://doi.org/10.1038/s44172-026-00597-5
Trefwoorden: gefocusseerd ultrageluid, bloed‑hersenbarrière, geneesmiddelbezorging, hersenbloedvaten, microbellen