Clear Sky Science · fr
Une ouverture sûre de la barrière hémato‑encéphalique par ultrasons focalisés repose principalement sur une réorganisation transitoire des jonctions serrées
Pourquoi il est important d’ouvrir la porte du cerveau
De nombreux traitements les plus prometteurs contre la maladie d’Alzheimer, les cancers cérébraux et d’autres affections neurologiques n’atteignent jamais leurs cibles, car le cerveau est protégé par un gardien microscopique appelé barrière hémato‑encéphalique. Cette barrière protège les tissus nerveux fragiles des substances nuisibles présentes dans le sang, mais elle bloque également la plupart des médicaments utiles. L’étude résumée ici explore une méthode non invasive pour ouvrir brièvement cette barrière à l’aide d’ondes sonores focalisées, dévoilant ce qui arrive aux vaisseaux sanguins cérébraux lorsque l’approche est utilisée de manière douce plutôt que trop agressive.
Une porte vers le cerveau actionnée par le son
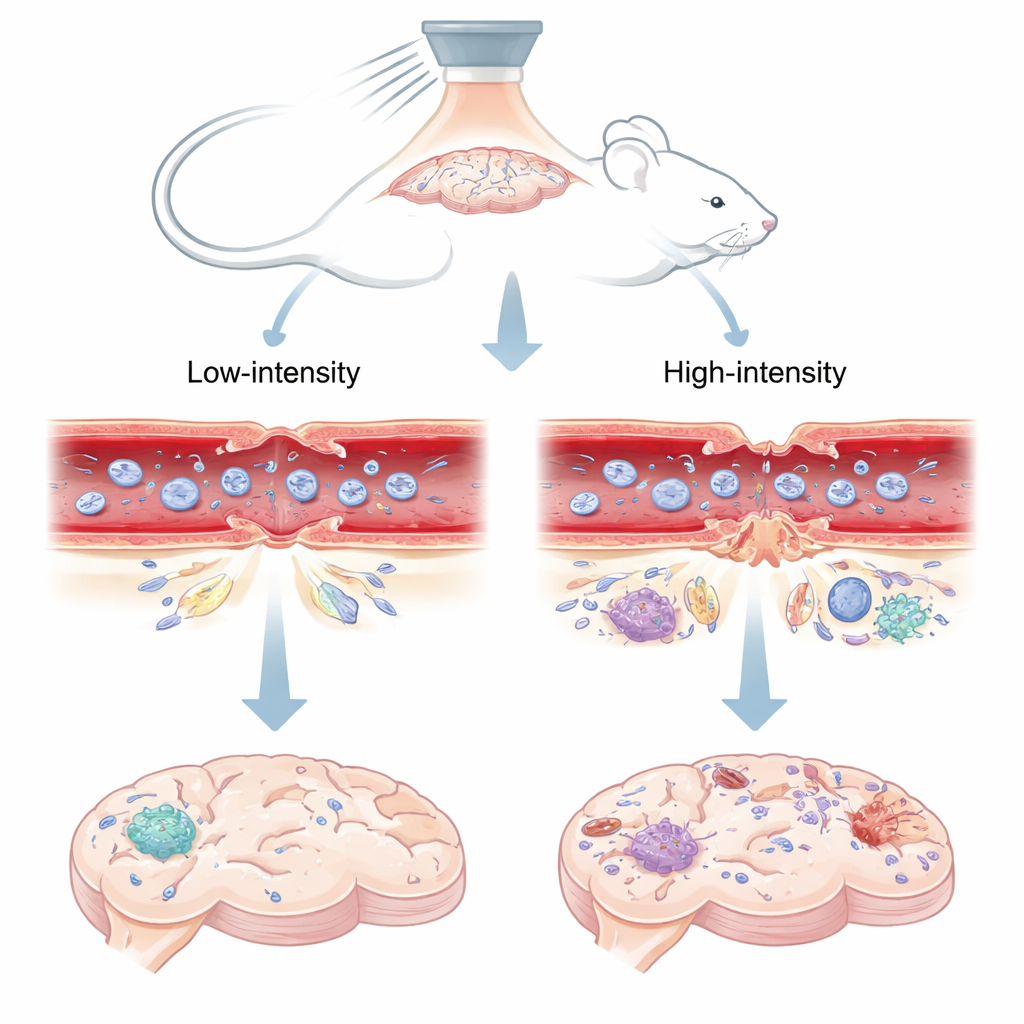
Les chercheurs ont utilisé des ultrasons focalisés – des ondes sonores concentrées provenant de l’extérieur du crâne – combinés à de minuscules bulles remplies de gaz injectées dans la circulation sanguine. Lorsque les ondes sonores frappent ces microbulles dans les vaisseaux cérébraux, les bulles vibrent. À faibles pressions sonores, les bulles oscillent de façon contrôlée ; à des pressions plus élevées, elles peuvent s’effondrer violemment. L’équipe a testé deux niveaux chez la souris : un réglage « bas » connu d’études antérieures pour ouvrir la barrière de façon sûre et brève, et un réglage « élevé » associé à une fuite plus longue et à des lésions tissulaires. Ils ont ensuite observé comment un colorant fluorescent et un produit de contraste IRM se propageaient dans le cerveau, ce qui a révélé quand et où la barrière s’était ouverte et quand elle s’était refermée.
Des portes microscopiques qui se déplacent ou se brisent
La barrière hémato‑encéphalique est principalement formée par des jonctions serrées – des « fermetures éclair » protéiques qui scellent les cellules voisines qui tapissent les vaisseaux cérébraux. Chez des souris spéciales dont les jonctions serrées brillent au microscope, les scientifiques ont pu observer ces fermetures changer de forme après l’exposition aux ultrasons. À la faible pression sûre, les jonctions présentaient de petites lacunes temporaires à la fois dans les capillaires minuscules et dans des artérioles légèrement plus larges. En l’espace d’environ trois jours, ces lacunes se refermaient largement et le motif des jonctions ressemblait beaucoup à celui du côté non traité du cerveau, ce qui correspondait au fait que le colorant et le produit de contraste IRM ne fuyaient plus. À la pression plus élevée, toutefois, les jonctions n’étaient pas seulement entrouvertes mais parfois complètement absentes, en particulier dans les plus gros vaisseaux. Ces ruptures sévères ont persisté pendant au moins 72 heures et s’accompagnaient d’une fuite continue des molécules traceuses.
Les cellules immunitaires cérébrales et les protéines sanguines prennent part à l’histoire
L’ouverture de la barrière permet aussi aux protéines sanguines de pénétrer dans le tissu cérébral. L’une de ces protéines, la fibrinogène, joue un rôle dans la coagulation et l’inflammation et est liée à des dommages dans plusieurs maladies cérébrales. Peu après l’exposition aux ultrasons, pour les deux niveaux de pression, de la fibrinogène est apparue près des vaisseaux perméables, parallèlement à des microglies activées, les cellules immunitaires résidentes du cerveau. Les microglies sont passées d’une apparence ramifiée et au repos à une forme plus ronde, « en alerte ». Au bout de 72 heures, la fibrinogène n’était plus détectable pour les deux pressions, ce qui suggère que même lorsque des dommages aux jonctions persistaient à la pression élevée, certains aspects de la fuite s’étaient résorbés. Les chercheurs ont également testé des souris dépourvues de cavéoles, de petites invaginations de la paroi vasculaire qui peuvent transporter des molécules à travers les cellules. L’ouverture de la barrière à la pression sûre n’a pas été modifiée en l’absence de ces structures, ce qui indique que la réorganisation des jonctions serrées – et non une augmentation de ce mode de transport – est le principal mécanisme d’une ouverture contrôlée.
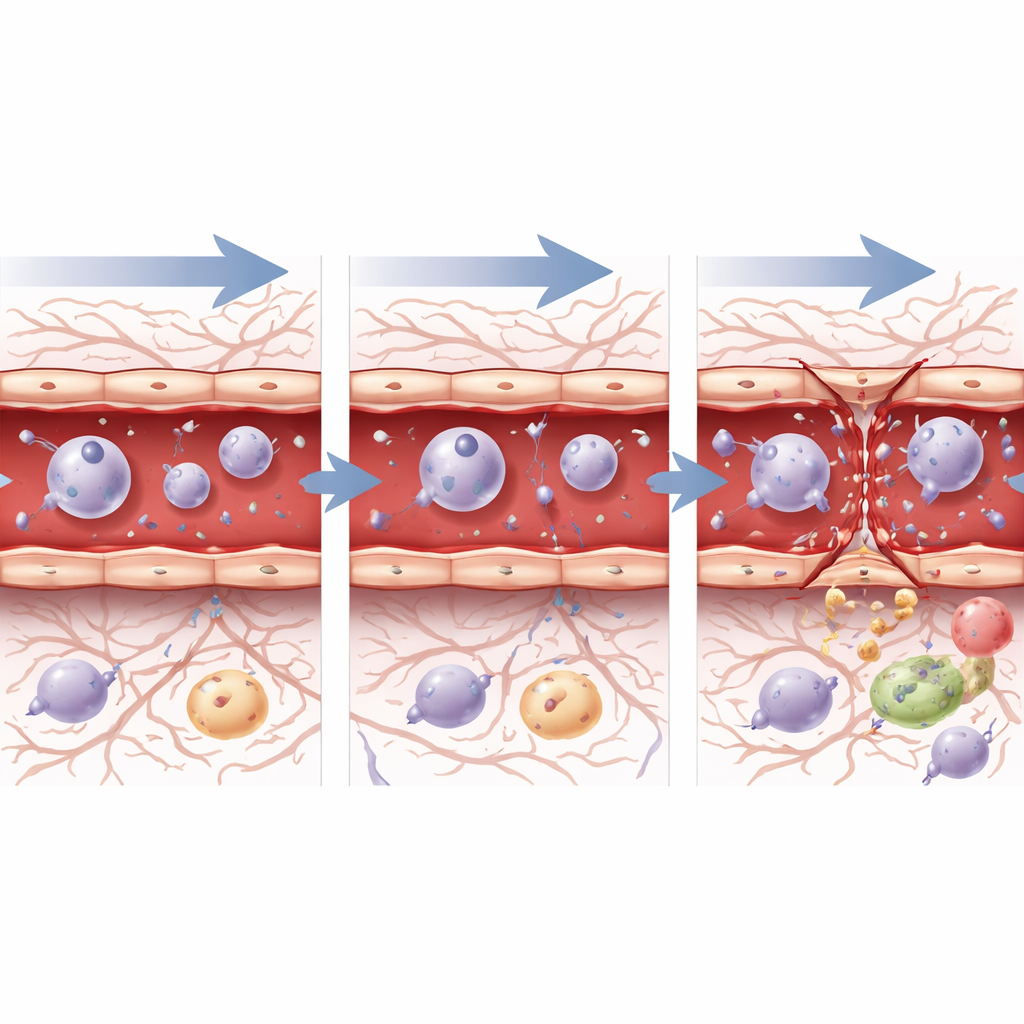
Comment les cellules des vaisseaux sanguins réagissent de l’intérieur
Pour voir comment les cellules individuelles des vaisseaux réagissaient au niveau génétique, l’équipe a isolé des milliers de cellules endothéliales – les cellules tapissant artères, capillaires et veines – et a réalisé un séquençage de l’ARN à cellule unique. Une heure après les ultrasons, quel que soit le niveau de pression, ces cellules ont augmenté l’expression de gènes associés au stress, à la mort cellulaire, à l’inflammation et à la réparation, signalant qu’elles percevaient à la fois une lésion et la nécessité de récupérer. Au bout de 72 heures, les trajectoires ont divergé. Après la pression sûre et basse, les cellules présentaient une activité génique compatible avec la cicatrisation, une croissance cellulaire contrôlée et un retour progressif vers un état de barrière stable. Après la pression élevée, en revanche, les cellules exprimaient encore fortement des programmes de stress et de « réponse aux blessures », et les gènes clés impliqués dans la constitution des jonctions restaient supprimés, en accord avec les dommages structurels persistants observés au microscope. Les voies qui guident la croissance vasculaire et la formation de la barrière, telles que les voies TGF‑bêta, Notch et Wnt, évoluaient dans le temps de manière suggérant une réparation active mais incomplète, en particulier après le réglage le plus agressif.
Ce que cela signifie pour les traitements cérébraux futurs
Pour ceux qui espèrent de meilleures thérapies cérébrales, ce travail clarifie une question centrale de sécurité : comment ouvrir suffisamment la barrière hémato‑encéphalique pour laisser passer les médicaments, sans provoquer de dommages durables ? L’étude montre qu’à des pressions d’ultrasons soigneusement choisies et plus faibles, la barrière s’ouvre principalement parce que ses « fermetures éclair » protéiques se desserrent brièvement puis se réorganisent, avec des cellules vasculaires mobilisant des programmes de réparation qui referment les lacunes en quelques jours. Pousser le système plus fort détruit ces fermetures plutôt que de simplement les déplacer, entraînant des fuites prolongées et une souffrance cellulaire durable. En termes pratiques, ces résultats soutiennent l’utilisation de réglages ultrasons conservateurs et d’une surveillance attentive en pratique clinique, renforçant l’idée que l’administration sûre de médicaments au cerveau repose sur une réorganisation transitoire – et non sur la destruction – des portes microscopiques du cerveau.
Citation: Noel, R.L., Kugelman, T., Karakatsani, M.E. et al. Safe focused ultrasound-mediated blood-brain barrier opening is driven primarily by transient reorganization of tight junctions. Commun Eng 5, 58 (2026). https://doi.org/10.1038/s44172-026-00597-5
Mots-clés: ultrasons focalisés, barrière hémato‑encéphalique, administration de médicaments, vaisseaux sanguins cérébraux, microbulles