Clear Sky Science · sv
Riboswitch‑styrd lipidomvandling möjliggör funktionell membranasymmetri i artificiella celler
Varför det spelar roll att bygga konstgjorda celler
Varje levande cell omformar ständigt sin yttre hud — membranet — för att känna av omgivningen, skicka signaler och överleva. Men de flesta artificiella celler som görs i labbet har frusna, oföränderliga membran, vilket begränsar hur livlika de kan vara. Denna artikel beskriver ett sätt att ge artificiella celler en slags ”programmerbar hud” som kan ändra sin sammansättning som respons på ett enkelt kemiskt signalämne. Denna förmåga skulle en dag kunna göra att små syntetiska celler känner av sjukdomar, frigör läkemedel på begäran eller hjälper forskare att undersöka hur riktiga celler fungerar från utsidan och in.
En strömbrytare som lyssnar på ett enkelt salt
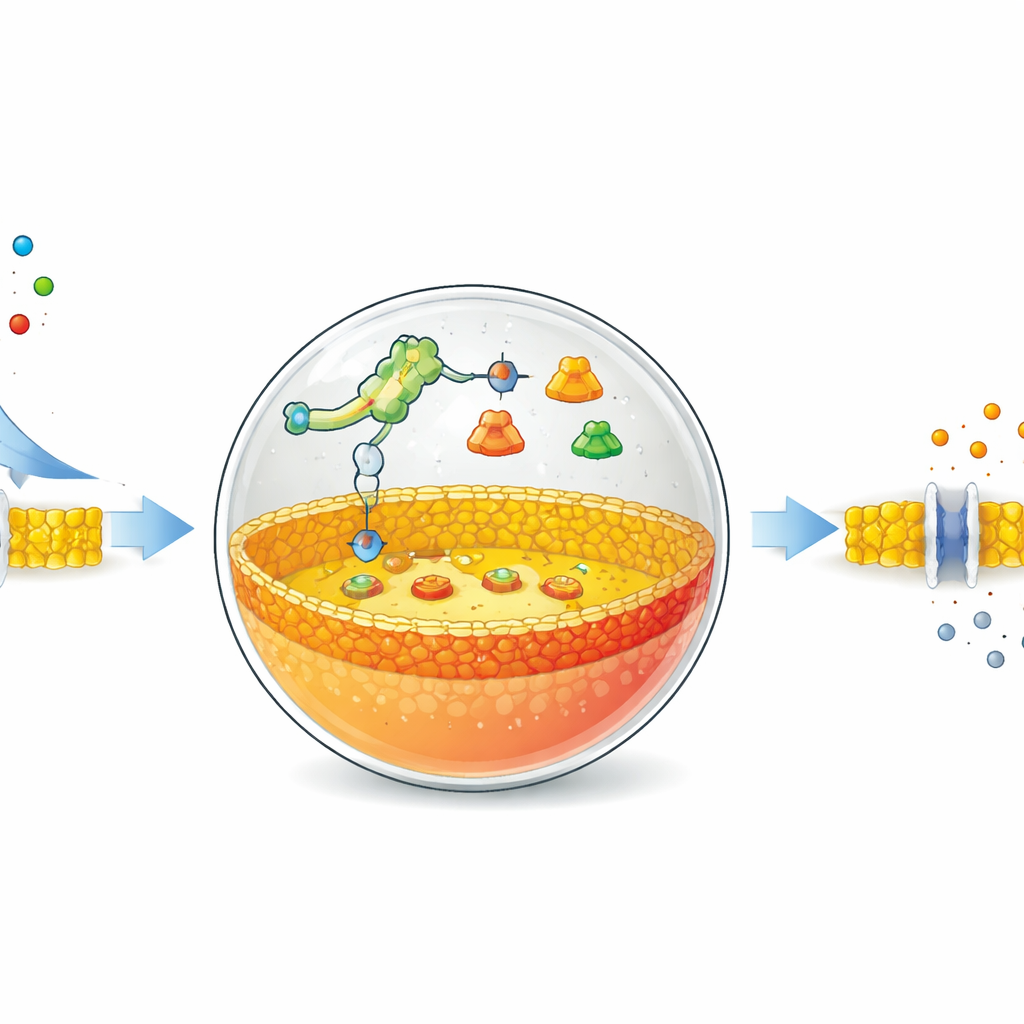
Författarna börjar med ihåliga bubblor gjorda av fettmolekyler, liknande de som bildar naturliga cellmembran. Inuti dessa bubblor placerar de ett avskalat proteinsyntessystem och särskilda DNA‑instruktioner. Centralt i deras konstruktion finns en riboswitch — ett RNA‑segment som ändrar form när det binder ett visst småmolekylärt ämne och därigenom slår på eller av proteinproduktion. Här är riboswitchen inställd för att reagera på vanliga fluoridjoner, till exempel från natriumfluorid. När fluorid smiter igenom membranet in i bubblan aktiveras riboswitchen DNA‑programmet och beställer fram produktion av ett specifikt enzym.
Att skriva om membranet inifrån
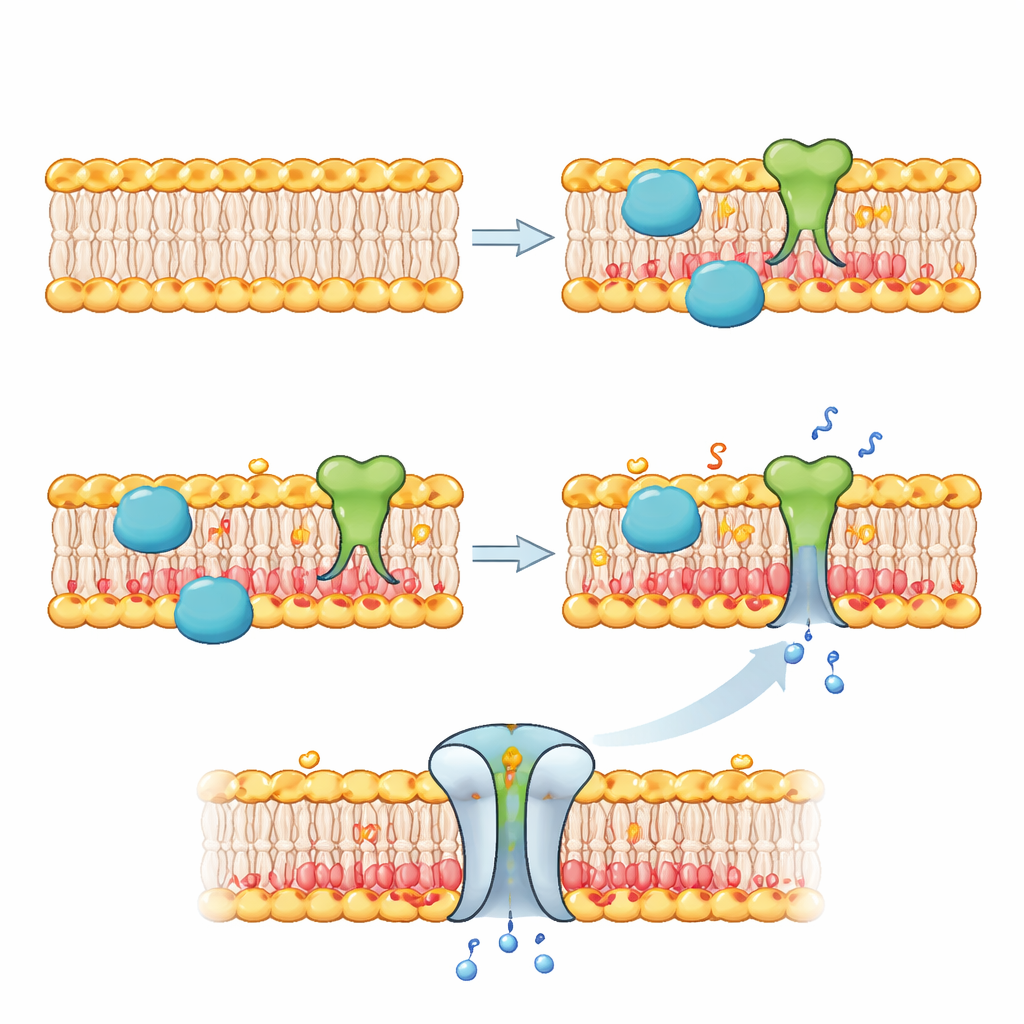
Det valda enzymet är fosfolipas D, ett protein som klipper och redigerar fettmolekyler. I dessa artificiella celler består startmembranet mestadels av en neutral fettmolekyl kallad fosfatidylkolin. Nyproducerad fosfolipas D arbetar bara på den inre halvan av membranet och omvandlar en del av dessa neutrala fetter till negativt laddade sådana, kallade fosfatidsyra. Som ett resultat blir membranet asymmetriskt: insidan blir mer negativt laddad än utsidan. Med fluorescerande prober som binder fosfatidsyra följde teamet denna förändring över tid. De visade att genom att ställa in mängden DNA och fluorid kunde de kontrollera hur snabbt och hur kraftigt det inre membranet omformas, med märkbara förändringar efter ungefär en timme.
Att hålla obalansen på plats
I mjuka, flytande membran driver fettmolekyler långsamt över från ena sidan till den andra, vilket skulle radera den noggrant skapade obalansen. För att motverka detta tillsatte forskarna kolesterol, en styv komponent som också är riklig i humana cellmembran. Med kolesterol närvarande stannade de nybildade negativa lipiderna till största delen på insidan i minst 90 minuter, medan mycket mindre läckte ut till utsidan. Genom att jämföra bubblor med och utan kolesterol och uppskatta hur många modifierade lipider som framträdde på varje sida visade de att kolesterol hämmar flip‑flop‑rörelsen hos dessa molekyler och hjälper till att bevara långlivad asymmetri — en viktig egenskap hos riktiga cellmembran.
Förankring av proteiner och öppning av portar
När de kunde skriva om det inre membranet använde författarna denna nya kemi för att kontrollera vad som händer vid gränsytan på den artificiella cellen. I en serie experiment använde de en variant av samma enzymaktivitet för att fästa ”klickbara” handtag på lipider i innerbladet, och förankrade sedan ett fluorescerande protein vid dessa handtag. Först när fluorid tillsattes samlades proteinerna längs membranet, vilket visar stimulusstyrd proteinrekrytering. I ett annat viktigt test tillsatte de ett naturligt portprotein kallat MscL till membranet. Denna kanal tenderar att öppna när den känner av negativa lipider och spänning. När fosfolipas D byggde upp negativa lipider på insidan efter fluoridtillsats öppnade MscL‑porerna och tillät små färgämnesmolekyler att flöda in i bubblorna, vilket gjorde dem synligt ljusa — tydligt bevis för att membranomformning kan växla ett membranprotein från ett inaktivt till ett aktivt tillstånd.
Från programmerbara skinn till smarta syntetiska celler
För en icke‑specialist är kärnbudskapet att forskarna har kopplat ihop en kemisk sensor, en genetisk brytare och ett membranredigerande enzym inuti små fettbubblor. En enkel yttre signal — en skvätt fluorid — får den artificiella cellen att ändra laddningsmönstret i sitt membran inifrån, vilket i sin tur styr vilka proteiner som fäster vid ytan och om inbyggda portar öppnas eller stängs. Denna metod förvandlar annars passiva bubblor till responsiva, ställbara objekt som liknar levande celler i högre grad. Framåtblickande skulle liknande upplägg göra det möjligt för artificiella celler att känna av signaler från tumörer, omforma sina membran och utlösa kaskader av reaktioner eller läkemedelsfrisättning, och därigenom erbjuda en kraftfull ny väg till miljömedvetna, programmerbara mikroskopiska enheter.
Citering: Kamiya, K., Lee, S. & Baba, K. Riboswitch-controlled lipid conversion enables functional membrane asymmetry in artificial cells. Commun Biol 9, 580 (2026). https://doi.org/10.1038/s42003-026-09890-7
Nyckelord: artificiella celler, riboswitch, lipidmembran, membranasymmetri, syntetisk biologi