Clear Sky Science · pt
Conversão lipídica controlada por riboswitch permite assimetria funcional de membrana em células artificiais
Por que Construir Células Falsas Importa
Toda célula viva remodela constantemente sua pele externa — a membrana — para perceber o ambiente, enviar sinais e permanecer viva. Ainda assim, a maioria das células artificiais produzidas em laboratório tem membranas congeladas e imutáveis, o que limita o quão parecidas com organismos reais elas podem ser. Este artigo descreve uma forma de dar às células artificiais uma espécie de “pele programável” que pode mudar sua composição em resposta a um sinal químico simples. Essa capacidade poderia, no futuro, permitir que minúsculas células sintéticas detectem doenças, liberem medicamentos sob demanda ou ajudem cientistas a investigar como células reais funcionam de fora para dentro.
Um Interruptor que Escuta um Sal Simples
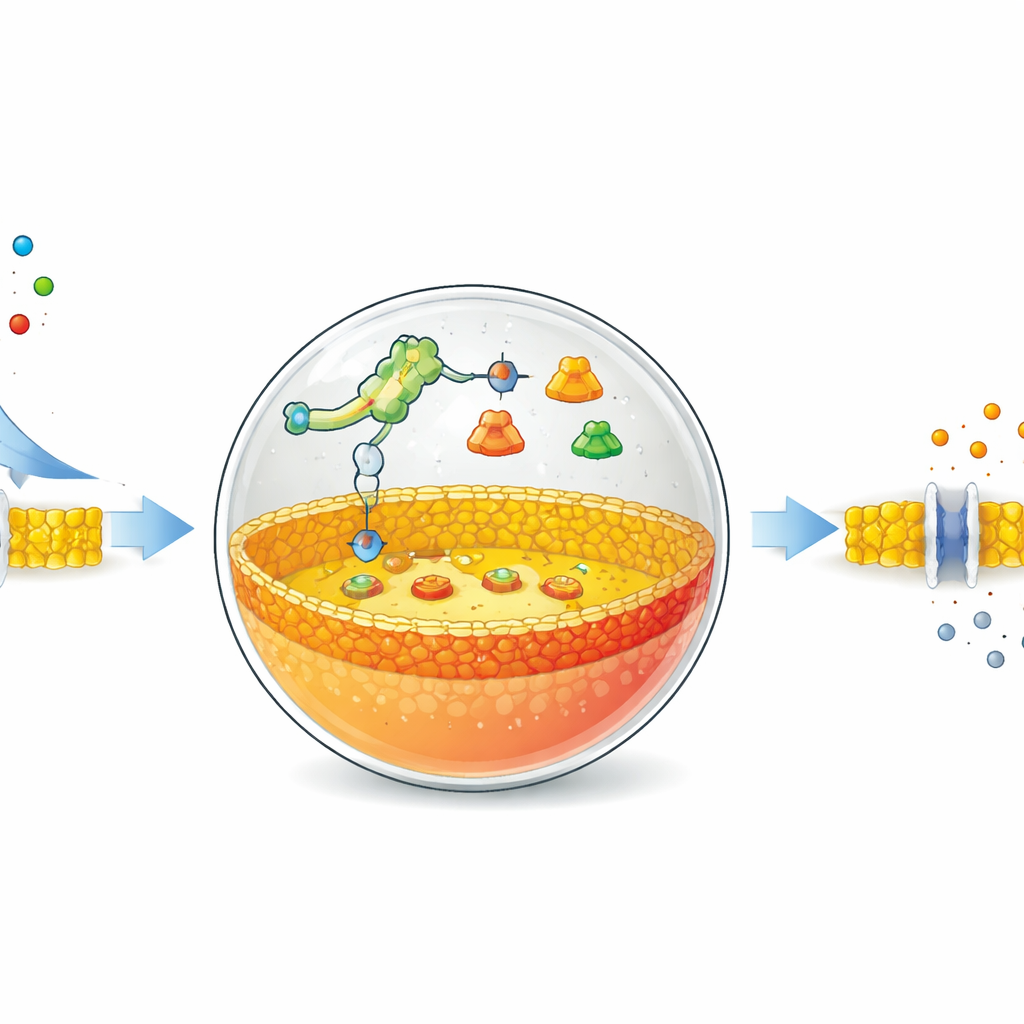
Os autores começam com bolhas ocas feitas de moléculas gordurosas, semelhantes às que formam membranas celulares naturais. Dentro dessas bolhas eles colocam um sistema reduzido de síntese proteica e instruções de DNA especiais. O elemento central do projeto é um riboswitch — um segmento de RNA que muda de forma quando se liga a uma pequena molécula específica e, ao fazê-lo, liga ou desliga a produção de proteínas. Aqui, o riboswitch é ajustado para responder a íons fluoreto comuns, como os do sal fluoreto de sódio. Quando o fluoreto atravessa a membrana e entra na bolha, o riboswitch ativa o programa codificado no DNA e ordena a produção de uma enzima específica.
Reescrevendo a Membrana de Dentro
A enzima escolhida é a fosfolipase D, uma proteína que corta e edita moléculas lipídicas. Nessas células artificiais, a membrana inicial é composta majoritariamente por um lipídio neutro chamado fosfatidilcolina. A fosfolipase D recém-sintetizada atua apenas na metade interna da membrana, convertendo alguns desses lipídios neutros em lipídios carregados negativamente chamados fosfatidato. Como resultado, a membrana torna-se assimétrica: o lado interno fica mais negativamente carregado que o externo. Usando sondas fluorescentes que se ligam ao fosfatidato, a equipe acompanhou essa mudança ao longo do tempo. Eles mostraram que, ao ajustar a quantidade de DNA e de fluoreto, podiam controlar a velocidade e a intensidade com que a membrana interna era remodelada, com mudanças significativas surgindo em cerca de uma hora.
Mantendo o Desequilíbrio no Lugar
Em membranas macias e fluidas, as moléculas lipídicas lentamente derivam de um lado para o outro, o que apagaria o desequilíbrio criado cuidadosamente. Para contrariar isso, os pesquisadores adicionaram colesterol, um componente endurecedor também abundante nas membranas humanas. Com colesterol presente, os lipídios negativos recém-formados permaneceram majoritariamente no lado interno por pelo menos 90 minutos, enquanto muito menos deles vazou para o lado externo. Ao comparar bolhas com e sem colesterol e estimar quantos lipídios modificados apareceram em cada face, demonstraram que o colesterol retarda o flip‑flop dessas moléculas e ajuda a preservar uma assimetria de longa duração — uma característica importante das membranas celulares reais.
Ancoragem de Proteínas e Abertura de Portas
Depois de conseguir reescrever a membrana interna, os autores usaram essa nova química para controlar o que acontece na fronteira da célula artificial. Em um conjunto de experimentos, empregaram uma variante da atividade da mesma enzima para anexar alças “clicáveis” aos lipídios da folha interna, e então ancoraram uma proteína fluorescente a essas alças. Apenas quando o fluoreto foi adicionado as proteínas se reuniram ao longo da membrana, demonstrando recrutamento de proteínas dependente do estímulo. Em outro teste-chave, introduziram uma proteína de porta natural chamada MscL na membrana. Esse canal tende a abrir quando sente lipídios negativos e tensão. À medida que a fosfolipase D acumulou lipídios negativos do lado interno após a adição de fluoreto, os poros MscL abriram e permitiram que pequenas moléculas corantes entrassem nas bolhas, tornando-as visivelmente brilhantes — evidência clara de que a remodelação da membrana pode alternar uma proteína de membrana de um estado inativo para um estado ativo.
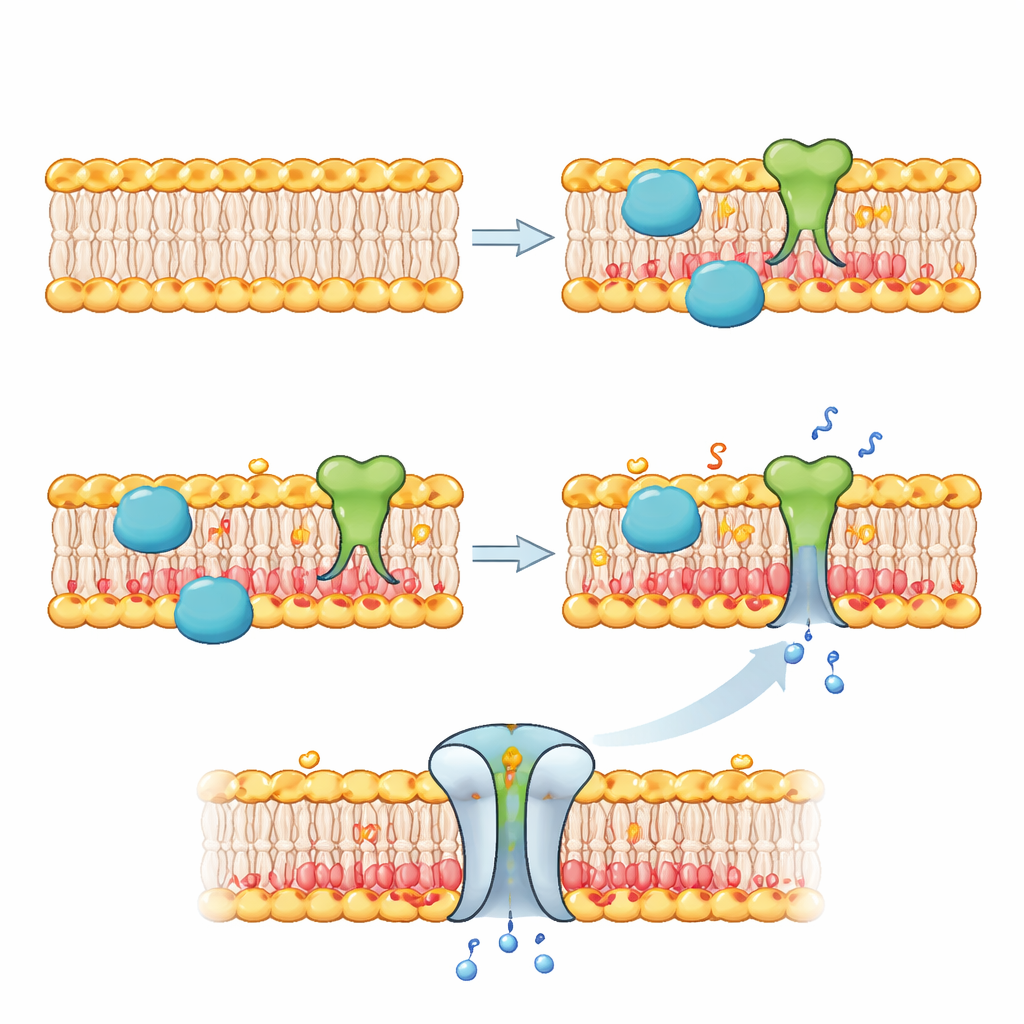
De Peles Programáveis a Células Sintéticas Inteligentes
Para um público não especialista, a mensagem principal é que os pesquisadores conectaram um sensor químico, um interruptor genético e uma enzima editora de membrana dentro de minúsculas bolhas gordurosas. Um sinal externo simples — um pouco de fluoreto — faz com que a célula artificial modifique o padrão de cargas da sua membrana por dentro, o que por sua vez controla quais proteínas se anexam à superfície e se portas incorporadas abrem ou fecham. Essa abordagem transforma bolhas passivas em objetos responsivos e ajustáveis que se parecem mais com células vivas. No futuro, esquemas semelhantes poderiam permitir que células artificiais detectassem sinais de tumores, remodelassem suas membranas e desencadeassem cascatas de reações ou liberação de fármacos, oferecendo uma nova via poderosa para dispositivos microscópicos programáveis e sensíveis ao ambiente.
Citação: Kamiya, K., Lee, S. & Baba, K. Riboswitch-controlled lipid conversion enables functional membrane asymmetry in artificial cells. Commun Biol 9, 580 (2026). https://doi.org/10.1038/s42003-026-09890-7
Palavras-chave: células artificiais, riboswitch, membranas lipídicas, assimetria de membrana, biologia sintética