Clear Sky Science · de
Riboswitch-gesteuerte Lipidumwandlung ermöglicht funktionelle Membranasymmetrie in künstlichen Zellen
Warum der Bau künstlicher Zellen wichtig ist
Jede lebende Zelle baut ihre äußere Hülle – die Membran – ständig um, um ihre Umgebung wahrzunehmen, Signale zu senden und zu überleben. Die meisten im Labor hergestellten künstlichen Zellen besitzen jedoch starre, unveränderte Membranen, was ihre Lebensechtheit einschränkt. Diese Arbeit beschreibt eine Methode, künstlichen Zellen eine Art „programmierbare Haut“ zu geben, die ihre Zusammensetzung als Reaktion auf ein einfaches chemisches Signal verändern kann. Diese Fähigkeit könnte es eines Tages winzigen synthetischen Zellen ermöglichen, Krankheiten zu erkennen, Medikamente gezielt freizusetzen oder Forschern zu helfen, echte Zellen von außen nach innen zu untersuchen.
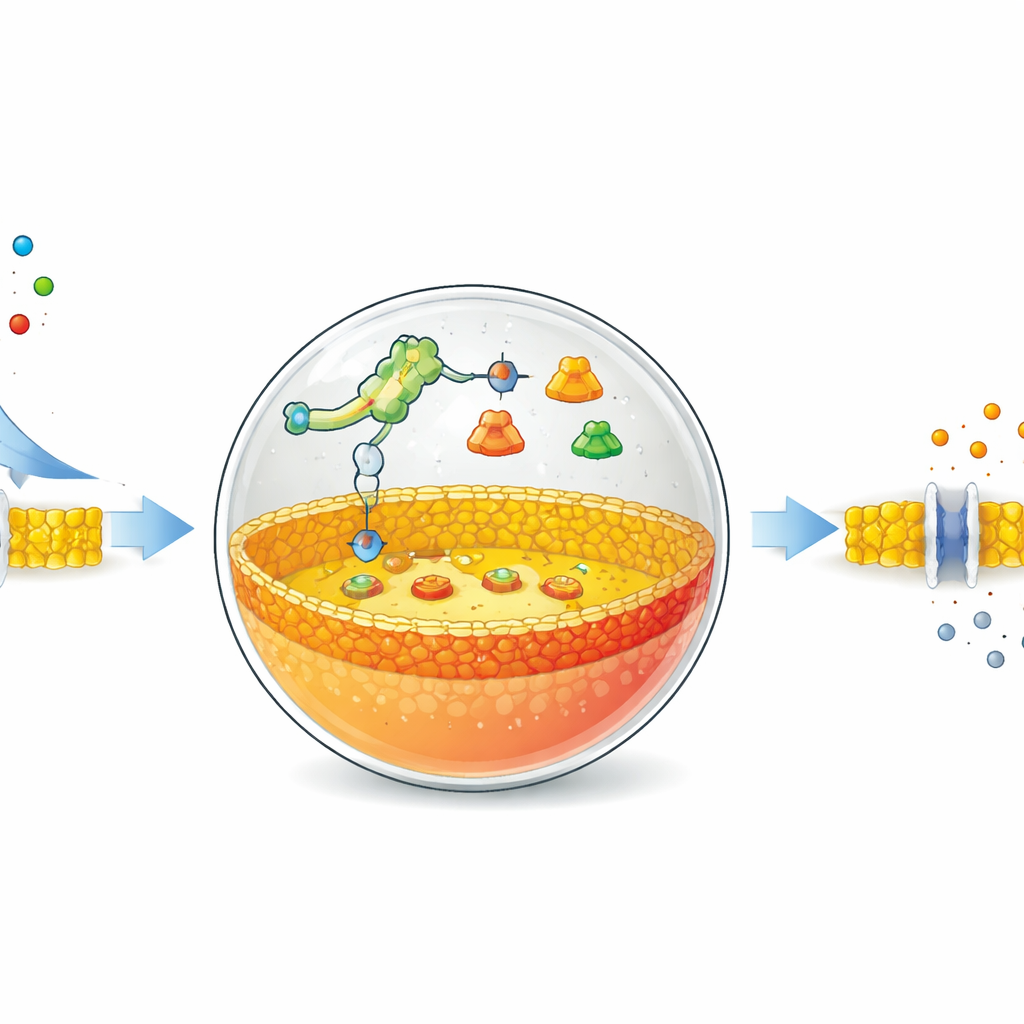
Ein Schalter, der auf ein einfaches Salz hört
Die Autoren beginnen mit hohlen Bläschen aus Fettmolekülen, ähnlich denen, die natürliche Zellmembranen bilden. In diese Bläschen bringen sie ein reduziertes Protein‑Herstellungssystem und spezielle DNA‑Anweisungen ein. Zentral für ihr Design ist ein Riboswitch – ein RNA‑Abschnitt, der seine Form ändert, wenn er ein bestimmtes kleines Molekül bindet, und dadurch die Proteinproduktion an- oder ausschaltet. Hier ist der Riboswitch so abgestimmt, dass er auf gewöhnliche Fluoridionen reagiert, wie sie etwa aus Natriumfluorid stammen. Wenn Fluorid durch die Membran in das Bläschen gelangt, aktiviert der Riboswitch das DNA‑Programm und veranlasst die Produktion eines spezifischen Enzyms.
Die Membran von innen umschreiben
Als Enzym wählten sie Phospholipase D, ein Protein, das Fettmoleküle zuschneidet und bearbeitet. In diesen künstlichen Zellen besteht die Ausgangsmembran größtenteils aus einem neutralen Fettstoff, dem Phosphatidylcholin. Neu gebildete Phospholipase D wirkt nur an der inneren Halbseite der Membran und wandelt einen Teil dieser neutralen Fette in negativ geladene Lipide namens Phosphatidsäure um. Infolgedessen wird die Membran asymmetrisch: die Innenseite ist negativer geladen als die Außenseite. Mit fluoreszenten Sonden, die an Phosphatidsäure binden, verfolgte das Team diese Veränderung über die Zeit. Sie zeigten, dass sie durch Anpassung der DNA‑Menge und des Fluorids steuern konnten, wie schnell und wie stark die innere Membran umgebaut wurde, wobei deutliche Veränderungen innerhalb von etwa einer Stunde sichtbar wurden.
Das Ungleichgewicht in Position halten
In weichen, flüssigen Membranen wandern Fettmoleküle langsam von einer Seite zur anderen, was das sorgfältig erzeugte Ungleichgewicht auslöschen würde. Um dem entgegenzuwirken, fügten die Forscher Cholesterin hinzu, eine verfestigende Komponente, die auch in menschlichen Zellmembranen reichlich vorkommt. In Gegenwart von Cholesterin blieben die neu gebildeten negativen Lipide für mindestens 90 Minuten überwiegend auf der Innenseite, während deutlich weniger von ihnen nach außen übergingen. Durch den Vergleich von Bläschen mit und ohne Cholesterin und die Abschätzung, wie viele modifizierte Lipide auf jeder Seite erschienen, zeigten sie, dass Cholesterin das Flip‑Flop dieser Moleküle verlangsamt und hilft, langlebige Asymmetrie zu erhalten – ein wichtiges Merkmal echter Zellmembranen.
Andockende Proteine und sich öffnende Tore
Sobald sie die innere Membran umschreiben konnten, nutzten die Autoren diese neue Chemie, um zu steuern, was an der Grenze der künstlichen Zelle geschieht. In einem Satz von Experimenten verwendeten sie eine Variantenaktivität desselben Enzyms, um „klickbare“ Griffe an Innenblattlipide anzubringen und daran ein fluoreszierendes Protein zu verankern. Nur wenn Fluorid zugegeben wurde, sammelten sich die Proteine entlang der Membran, was eine stimulusabhängige Proteinrekrutierung demonstrierte. In einem weiteren wichtigen Test setzten sie ein natürliches Torprotein namens MscL in die Membran ein. Dieser Kanal neigt dazu, sich zu öffnen, wenn er negative Lipide und Spannung spürt. Als die Phospholipase D nach Zugabe von Fluorid negative Lipide an der Innenseite aufbaute, öffneten sich MscL‑Poren und erlaubten kleinen Farbstoffmolekülen, in die Bläschen zu strömen, die dadurch sichtbar aufleuchteten – ein eindeutiger Beleg dafür, dass Membranumbau ein Membranprotein von einem inaktiven in einen aktiven Zustand versetzen kann.
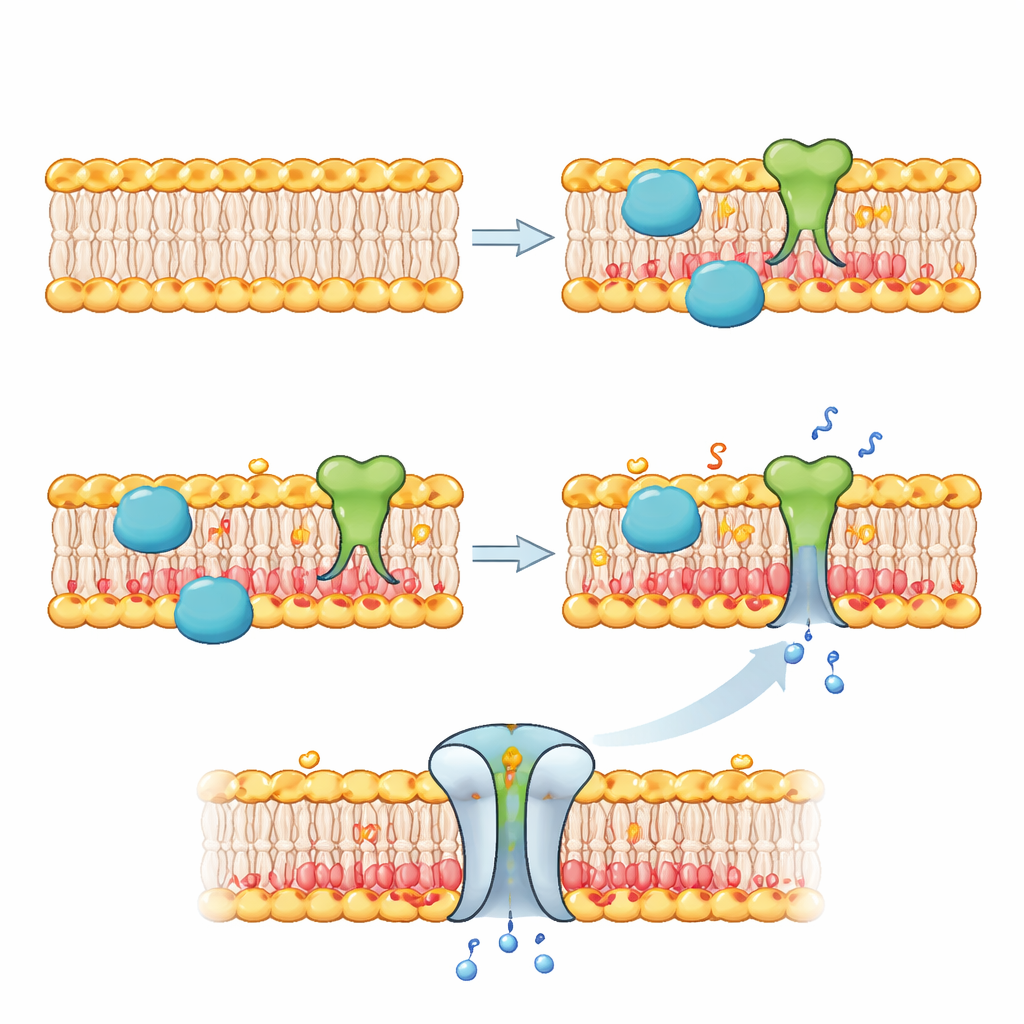
Von programmierbaren Häuten zu intelligenten synthetischen Zellen
Für Nicht‑Spezialisten lautet die Kernbotschaft, dass die Forscher einen chemischen Sensor, einen genetischen Schalter und ein membran‑editierendes Enzym in winzigen Fettbläschen miteinander verknüpft haben. Ein einfaches äußeres Signal – etwas Fluorid – veranlasst die künstliche Zelle, das Ladungsmuster ihrer Membran von innen zu ändern, was wiederum steuert, welche Proteine an der Oberfläche haften und ob integrierte Tore sich öffnen oder schließen. Dieser Ansatz verwandelt ansonsten passive Bläschen in reaktionsfähige, einstellbare Objekte, die lebenden Zellen ähnlicher sind. Blickt man voraus, könnten ähnliche Konzepte künstlichen Zellen erlauben, Signale von Tumoren zu erkennen, ihre Membranen umzubauen und Reaktionskaskaden oder Medikamentenfreisetzung auszulösen – eine potente neue Route zu umweltbewussten, programmierbaren mikroskopischen Geräten.
Zitation: Kamiya, K., Lee, S. & Baba, K. Riboswitch-controlled lipid conversion enables functional membrane asymmetry in artificial cells. Commun Biol 9, 580 (2026). https://doi.org/10.1038/s42003-026-09890-7
Schlüsselwörter: künstliche Zellen, Riboswitch, Lipidmembranen, Membranasymmetrie, synthetische Biologie