Clear Sky Science · ru
Контроль превращения липидов с помощью рибосвитча обеспечивает функциональную асимметрию мембраны в искусственных клетках
Зачем важно создавать «фальшивые» клетки
Каждая живая клетка постоянно перестраивает свою внешнюю оболочку — мембрану — чтобы ощущать окружение, передавать сигналы и поддерживать жизнедеятельность. Тем не менее большинство искусственных клеток, собранных в лаборатории, имеют застывшие, неизменные мембраны, что ограничивает их сходство с живыми системами. В этой работе описан способ наделить искусственные клетки некой «программируемой кожей», способной менять свой состав в ответ на простой химический сигнал. Такая способность в будущем может позволить крошечным синтетическим клеткам обнаруживать болезни, выбрасывать лекарства по требованию или помогать учёным исследовать работу настоящих клеток изнутри наружу.
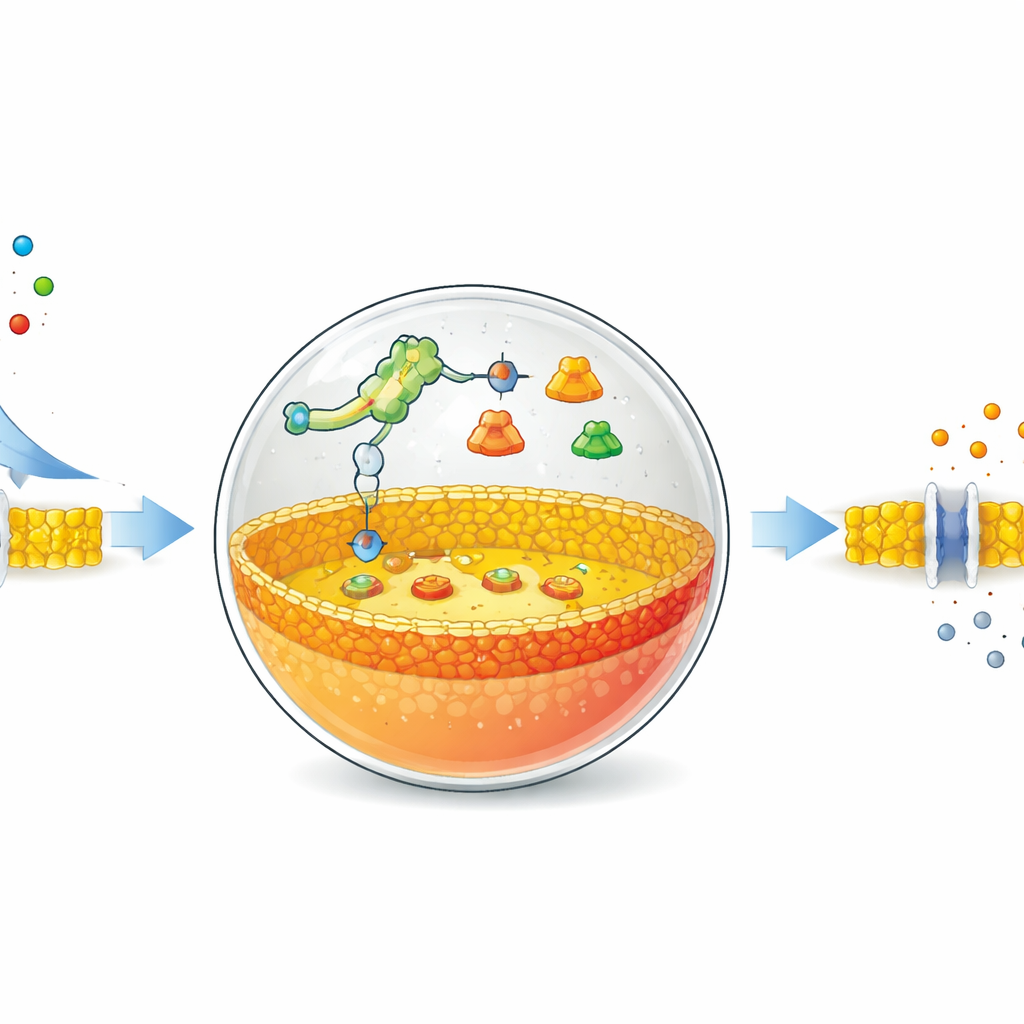
Переключатель, который реагирует на простую соль
Авторы начинают с полых пузырьков из жировых молекул, похожих на те, что формируют натуральные клеточные мембраны. Внутри этих пузырьков они помещают упрощённую систему синтеза белка и специальные ДНК‑инструкции. В центре конструкции находится рибосвитч — сегмент РНК, который меняет форму при связывании с определённой малой молекулой и тем самым включает или выключает синтез белка. В этой системе рибосвитч настроен реагировать на обычные ионы фторида, например из фторида натрия. Когда фторид проникает через мембрану внутрь пузырька, рибосвитч активирует программу на ДНК и запускает производство определённого фермента.
Переписывание мембраны изнутри
Выбранный фермент — фосфолипаза D, белок, расщепляющий и изменяющий молекулы жиров. В этих искусственных клетках исходная мембрана в основном состоит из нейтрального липида фосфатидилхолина. Новоиспечённая фосфолипаза D действует только на внутренний слой мембраны, превращая часть этих нейтральных липидов в отрицательно заряженные молекулы — фосфатидную кислоту. В результате мембрана становится асимметричной: внутренняя сторона приобретает более отрицательный заряд, чем внешняя. С помощью флуоресцентных зондов, связывающихся с фосфатидной кислотой, команда отслеживала это изменение во времени. Они показали, что, регулируя количество ДНК и фторида, можно контролировать скорость и степень перестройки внутренней мембраны, при этом заметные изменения появлялись примерно в течение часа.
Сохранение неравновесия
В мягких, текучих мембранах молекулы липидов медленно перетекают с одной стороны на другую, что со временем стирало бы созданное неравенство. Чтобы противостоять этому, исследователи добавили холестерин — уплотняющий компонент, также изобильный в мембранах человеческих клеток. При наличии холестерина вновь образованные отрицательные липиды оставались в основном на внутренней стороне по крайней мере в течение 90 минут, тогда как их утечка на внешнюю сторону была значительно меньше. Сопоставляя пузырьки с холестерином и без и оценивая, сколько модифицированных липидов появилось по обе стороны, они показали, что холестерин замедляет «флип‑флоп» этих молекул и помогает сохранять долгоживущую асимметрию — важную черту реальных клеточных мембран.
Пристыковка белков и открытие ворот
Добившись возможности переписывать внутреннюю мембрану, авторы использовали эту химию, чтобы управлять событиями на границе искусственной клетки. В одном наборе экспериментов они применили вариант активности того же фермента, чтобы присоединить «кликабельные» ручки к липидам внутреннего листа, а затем закрепили на этих ручках флуоресцентный белок. Белки собирались вдоль мембраны только после добавления фторида, демонстрируя зависимую от стимула рекрутировку белков. В другом важном тесте они включили в мембрану природный поровый белок MscL. Этот канал склонен открываться при возникновении отрицательных липидов и натяжении. По мере того как фосфолипаза D накапливала отрицательные липиды на внутренней стороне после добавления фторида, поры MscL открывались и позволяли маленьким красителям проникать в пузырьки, делая их яркими — наглядное свидетельство того, что перестройка мембраны может переключать мембранный белок из неактивного состояния в активное.
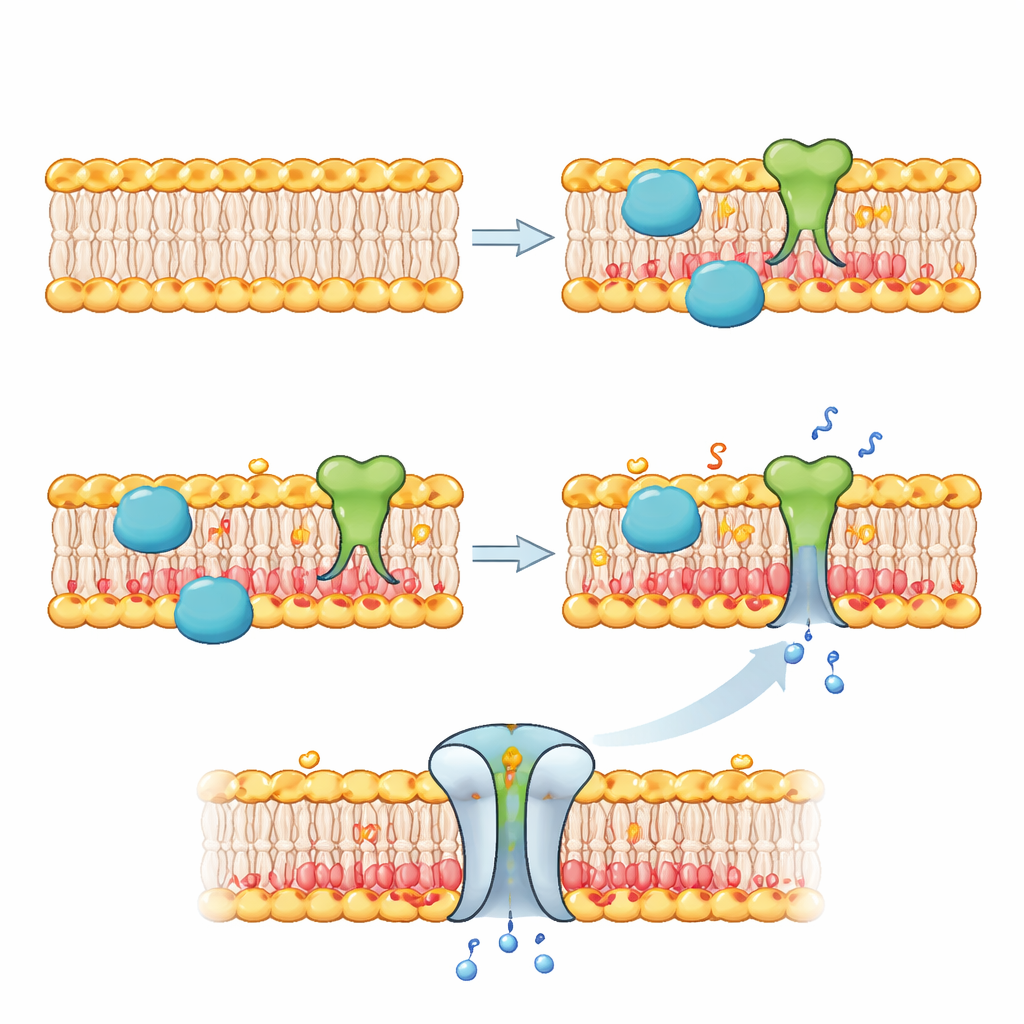
От программируемой «кожи» к умным синтетическим клеткам
Для неспециалиста ключевая идея такова: исследователи связали вместе химический сенсор, генетический переключатель и фермент, редактирующий мембрану, внутри крошечных жировых пузырьков. Простой внешний сигнал — немного фторида — заставляет искусственную клетку изменить распределение зарядов своей мембраны изнутри, что в свою очередь управляет тем, какие белки прикрепляются к поверхности и открываются ли встроенные ворота. Такой подход превращает в противном случае пассивные пузырьки в отзывчивые, настраиваемые объекты, которые ближе к живым клеткам. В перспективе подобные схемы могли бы позволить искусственным клеткам обнаруживать сигналы от опухолей, перестраивать свои мембраны и запускать каскады реакций или высвобождение лекарств, открывая мощный новый путь к экологически чувствительным программируемым микроскопическим устройствам.
Цитирование: Kamiya, K., Lee, S. & Baba, K. Riboswitch-controlled lipid conversion enables functional membrane asymmetry in artificial cells. Commun Biol 9, 580 (2026). https://doi.org/10.1038/s42003-026-09890-7
Ключевые слова: искусственные клетки, рибосвитч, липидные мембраны, асимметрия мембраны, синтетическая биология