Clear Sky Science · nl
Riboswitch-gestuurde lipidenconversie maakt functionele membraanasymmetrie mogelijk in kunstmatige cellen
Waarom het bouwen van nep‑cellen ertoe doet
Elke levende cel herstructureert voortdurend haar buitenste huid — het membraan — om haar omgeving waar te nemen, signalen uit te zenden en in leven te blijven. De meeste in het laboratorium gemaakte kunstmatige cellen hebben echter stijve, onveranderlijke membranen, wat hun levensachtigheid beperkt. Dit artikel beschrijft een manier om kunstmatige cellen een soort “programmeersbare huid” te geven die van samenstelling kan veranderen als reactie op een eenvoudige chemische prikkel. Die mogelijkheid zou het ooit kleinste synthetische cellen kunnen laten ziekte signaleren, medicijnen op verzoek vrijgeven of onderzoekers van buiten naar binnen laten onderzoeken hoe echte cellen werken.
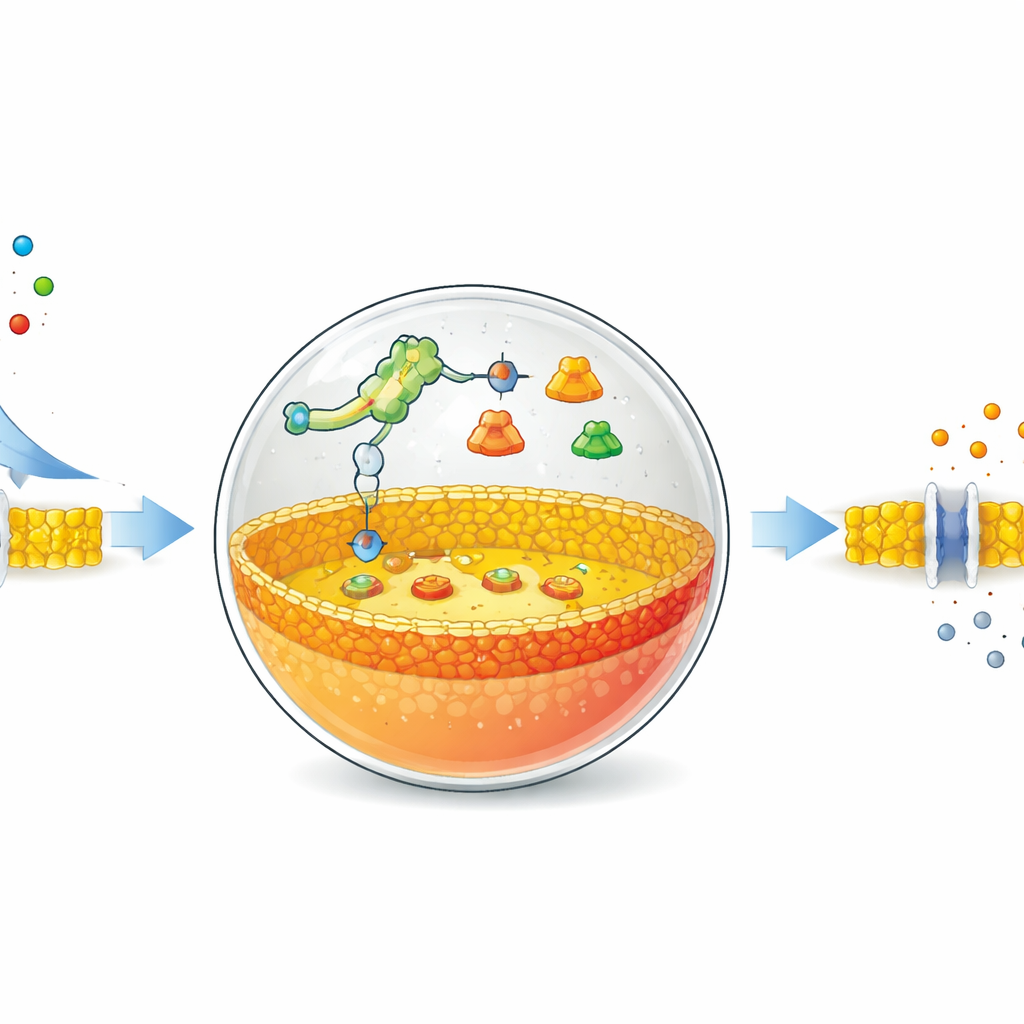
Een schakelaar die naar een eenvoudige zoutoplossing luistert
De auteurs beginnen met holle belletjes gemaakt van vetmoleculen, vergelijkbaar met die welke natuurlijke celmembranen vormen. In die belletjes plaatsen ze een uitgekleed eiwit‑productiesysteem en speciale DNA‑instructies. Centraal in hun ontwerp staat een riboswitch — een RNA‑segment dat van vorm verandert wanneer het aan een bepaald klein molecuul bindt en zo eiwitproductie aan of uit zet. Hier is de riboswitch afgestemd op gewone fluoride‑ionen, zoals uit natriumfluoride. Wanneer fluoride door het membraan in het belletje glipt, activeert de riboswitch het DNA‑programma en wordt de productie van een specifiek enzym op gang gebracht.
Het membraan van binnenuit herschrijven
Het gekozen enzym is fosfolipase D, een eiwit dat vetmoleculen knipt en aanpast. In deze kunstmatige cellen bestaat het beginnende membraan grotendeels uit een neutraal vet genaamd fosfatidylcholine. Nieuw geproduceerde fosfolipase D werkt alleen op de binnenste helft van het membraan en zet een deel van deze neutrale vetten om in negatief geladen lipiden die fosfatidezuur heten. Daardoor wordt het membraan asymmetrisch: de binnenzijde is negatiever geladen dan de buitenzijde. Met fluorescerende sondes die aan fosfatidezuur kleven, volgde het team deze verandering in de tijd. Ze lieten zien dat ze door de hoeveelheid DNA en fluoride aan te passen konden sturen hoe snel en hoe sterk het binnenmembraan werd omgebouwd, met duidelijke veranderingen binnen ongeveer een uur.
De onbalans in stand houden
In zachte, vloeibare membranen driften vetmoleculen langzaam van de ene kant naar de andere, wat de zorgvuldig gecreëerde onbalans zou wissen. Om dit tegen te gaan voegden de onderzoekers cholesterol toe, een verstevigende component die ook overvloedig in menselijke celmembranen aanwezig is. Met cholesterol bleef het nieuw gevormde negatieve lipide voor minstens 90 minuten grotendeels aan de binnenzijde, terwijl veel minder ervan naar de buitenzijde lekte. Door belletjes met en zonder cholesterol te vergelijken en te schatten hoeveel gemodificeerde lipiden aan elke kant verschenen, toonden ze aan dat cholesterol het flip‑flopgedrag van deze moleculen vertraagt en helpt langdurige asymmetrie te behouden — een belangrijk kenmerk van echte celmembranen.
Proteïnen vastzetten en poorten openen
Toen ze eenmaal het binnenmembraan konden herschrijven, gebruikten de auteurs deze nieuwe chemie om te sturen wat er aan de grens van de kunstmatige cel gebeurt. In één reeks experimenten gebruikten ze een variërende activiteit van hetzelfde enzym om “klikbare” handgrepen aan binnenbladlipiden vast te maken en verankerden vervolgens een fluorescent eiwit aan die handgrepen. Alleen wanneer fluoride werd toegevoegd, verzamelden de eiwitten zich langs het membraan, wat stimulus‑afhankelijke eiwitrekrutering aantoont. In een andere cruciale test voegden ze een natuurlijk poorteiwit genaamd MscL toe aan het membraan. Dit kanaal neigt te openen wanneer het negatieve lipiden en spanning waarneemt. Naarmate fosfolipase D na toevoeging van fluoride negatieve lipiden op de binnenzijde opbouwde, openden MscL‑poriën en lieten kleine kleurstofmoleculen in de belletjes stromen, waardoor ze zichtbaar oplichtten — duidelijk bewijs dat membraanherstructurering een membraaneiwit van een inactieve naar een actieve staat kan schakelen.
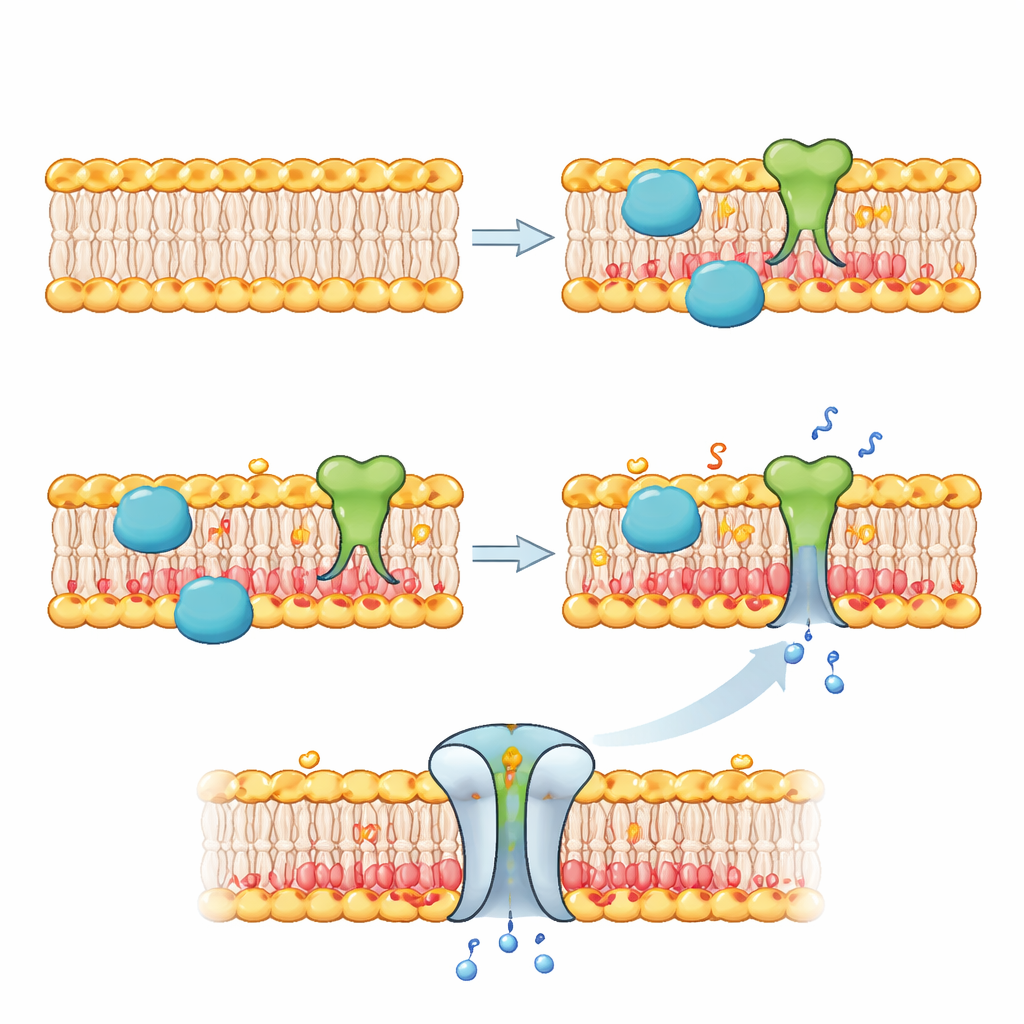
Van programmeerbare huiden naar slimme synthetische cellen
Voor een niet‑specialist is de kernboodschap dat de onderzoekers een chemische sensor, een genetische schakelaar en een membraan‑bewerkend enzym binnen kleine vetbelletjes aan elkaar hebben gekoppeld. Een simpele externe prikkel — een beetje fluoride — laat de kunstmatige cel het ladingpatroon van haar membraan van binnenuit veranderen, wat op zijn beurt bepaalt welke eiwitten aan het oppervlak blijven kleven en of ingebouwde poorten openen of sluiten. Deze aanpak verandert anders passieve belletjes in responsieve, regelbare objecten die meer op levende cellen lijken. Vooruitkijkend zouden soortgelijke schema’s kunstmatige cellen in staat kunnen stellen signalen van tumoren waar te nemen, hun membranen te herstructureren en cascade‑reacties of medicijnafgifte te activeren, wat een krachtige nieuwe route biedt naar milieubewuste, programmeerbare microscopische apparaten.
Bronvermelding: Kamiya, K., Lee, S. & Baba, K. Riboswitch-controlled lipid conversion enables functional membrane asymmetry in artificial cells. Commun Biol 9, 580 (2026). https://doi.org/10.1038/s42003-026-09890-7
Trefwoorden: kunstmatige cellen, riboswitch, lipidenmembranen, membraanasymmetrie, synthetische biologie