Clear Sky Science · pl
Kontrolowana przez ryboswitch konwersja lipidów umożliwia funkcjonalną asymetrię membran w sztucznych komórkach
Dlaczego warto budować sztuczne komórki
Każda żywa komórka nieustannie przebudowuje swoją zewnętrzną powłokę — błonę — aby wyczuwać otoczenie, wysyłać sygnały i przetrwać. Większość sztucznych komórek tworzonych w laboratorium ma jednak zamrożone, niezmienne błony, co ogranicza ich podobieństwo do komórek żywych. W artykule opisano sposób nadania sztucznym komórkom rodzaju „programowalnej skóry”, która może zmieniać swoje składniki w odpowiedzi na prosty chemiczny sygnał. Ta zdolność mogłaby w przyszłości pozwolić mikroskopijnym komórkom syntetycznym wykrywać choroby, uwalniać leki na żądanie lub pomóc naukowcom badać działanie prawdziwych komórek od zewnątrz do wnętrza.
Przełącznik, który reaguje na prostą sól
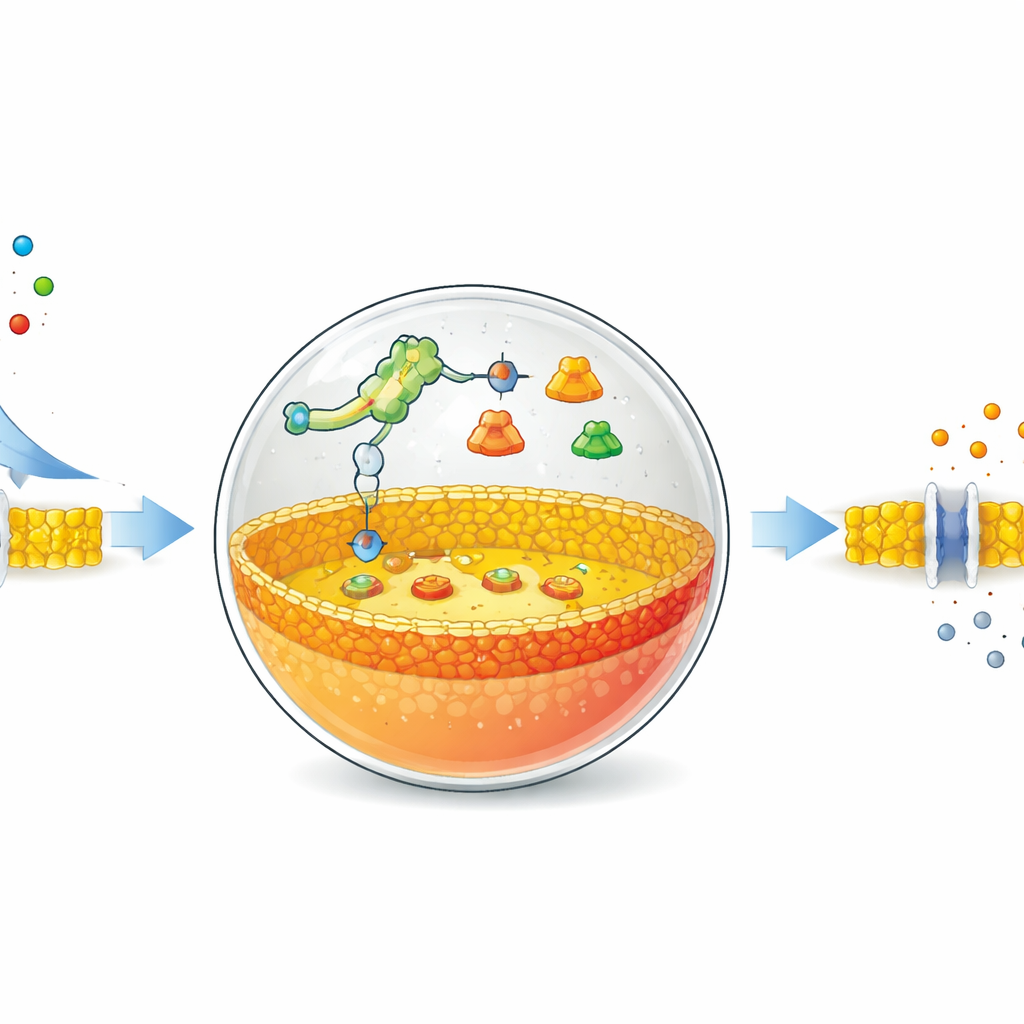
Autorzy zaczynają od pustych pęcherzyków zbudowanych z cząsteczek tłuszczu, podobnych do tych tworzących naturalne błony komórkowe. Wewnątrz tych pęcherzyków umieszczają uproszczony system syntezy białek i specjalne instrukcje DNA. Kluczowym elementem projektu jest ryboswitch — fragment RNA, który zmienia kształt po związaniu konkretnej małej cząsteczki i w ten sposób włącza lub wyłącza produkcję białek. W tym przypadku ryboswitch został dostrojony do reagowania na zwykłe jony fluorkowe, na przykład pochodzące z chlorku sodu fluorowego. Gdy fluorek przedostaje się przez błonę do wnętrza pęcherzyka, ryboswitch aktywuje program DNA i nakazuje syntezę określonego enzymu.
Pisanie błony od środka
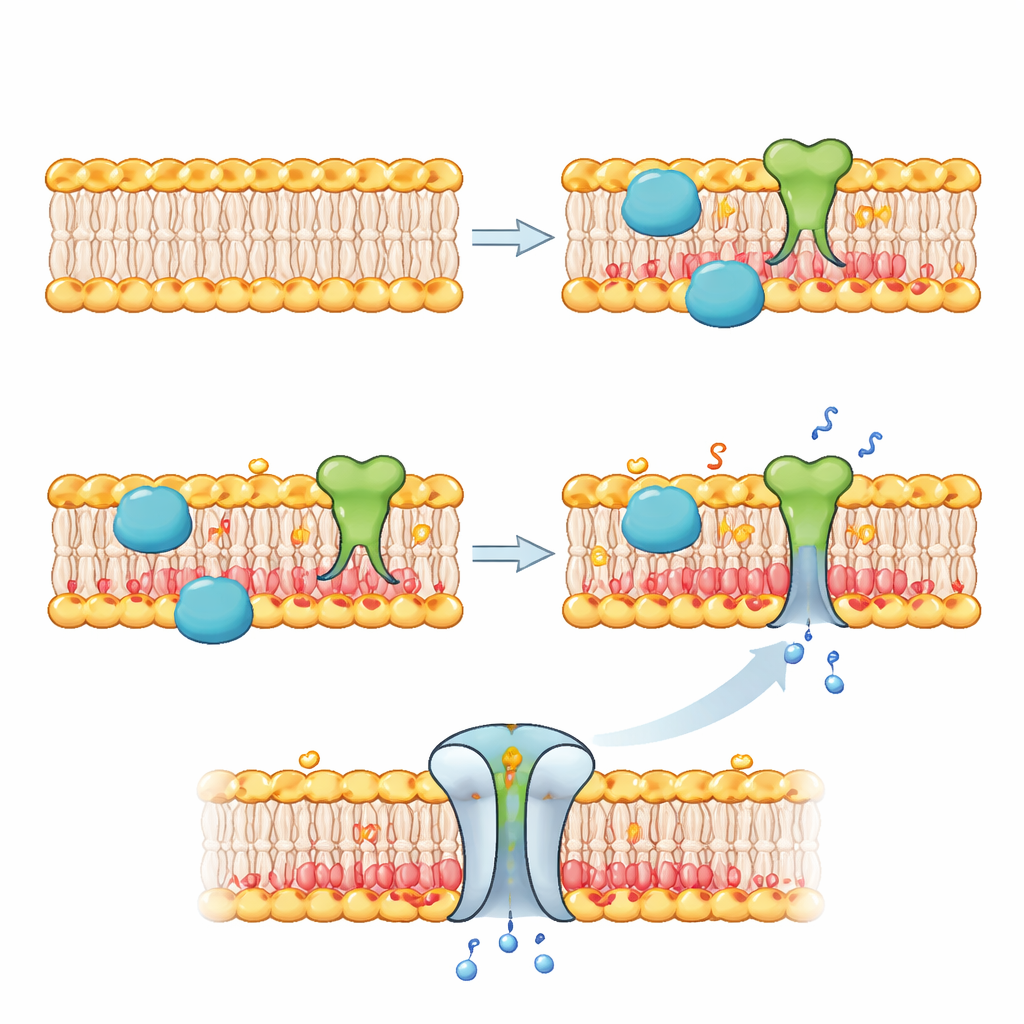
Wybranym enzymem jest fosfolipaza D, białko, które przecina i modyfikuje cząsteczki tłuszczu. W tych sztucznych komórkach początkowa błona składa się głównie z neutralnego lipidu zwanego fosfatydylocholiną. Nowo wytworzona fosfolipaza D działa tylko na wewnętrzną warstwę błony, przekształcając część tych neutralnych lipidów w naładowane ujemnie cząsteczki zwane kwasem fosfatydowym. W efekcie błona staje się asymetryczna: wewnętrzna strona jest bardziej ujemna niż zewnętrzna. Za pomocą fluorescencyjnych sond wiążących się z kwasem fosfatydowym zespół śledził tę zmianę w czasie. Pokazali, że regulując ilość DNA i fluorku można kontrolować, jak szybko i jak silnie przebudowywana jest wewnętrzna warstwa błony, przy czym istotne zmiany pojawiały się w ciągu około godziny.
Utrzymanie nierównowagi
W miękkich, płynnych błonach cząsteczki lipidów powoli przemieszczają się z jednej warstwy na drugą, co zatarłoby starannie stworzoną nierównowagę. Aby temu przeciwdziałać, badacze dodali cholesterol — składnik usztywniający, również obficie występujący w błonach ludzkich komórek. Przy obecności cholesterolu nowo powstałe ujemne lipidy pozostawały głównie po wewnętrznej stronie przez co najmniej 90 minut, podczas gdy znacznie mniej z nich migrowało na zewnętrzną stronę. Porównując pęcherzyki z cholesterolem i bez niego oraz szacując liczbę zmodyfikowanych lipidów po każdej stronie, wykazali, że cholesterol spowalnia „flip‑flop” tych cząsteczek i pomaga zachować długotrwałą asymetrię — ważną cechę prawdziwych błon komórkowych.
Zakotwiczanie białek i otwieranie bram
Kiedy już potrafili przepisać wewnętrzną warstwę błony, autorzy wykorzystali tę chemię do kontrolowania zdarzeń na granicy sztucznej komórki. W jednym zestawie eksperymentów użyli wariantu aktywności tego samego enzymu, aby przyłączyć do lipidów wewnętrznej warstwy „klikalne” uchwyty, a następnie zakotwiczyli do tych uchwytów białko fluorescencyjne. Dopiero po dodaniu fluorku białka gromadziły się wzdłuż błony, demonstrując rekrutację białek zależną od bodźca. W innym kluczowym teście dodali do błony naturalne białko kanałowe zwane MscL. Ten kanał ma tendencję do otwierania się, gdy wyczuje ujemne lipidy i napięcie. W miarę jak fosfolipaza D gromadziła ujemne lipidy po wewnętrznej stronie po dodaniu fluorku, pory MscL otwierały się i umożliwiały przepływ małych cząsteczek barwnika do pęcherzyków, widocznie je rozświetlając — przekonujący dowód, że przebudowa błony może przełączyć białko błonowe ze stanu nieaktywnego do aktywnego.
Od programowalnych skór do inteligentnych komórek syntetycznych
Dla osoby niebędącej specjalistą główny przekaz jest taki, że badacze połączyli czujnik chemiczny, genetyczny przełącznik i enzym modyfikujący błonę wewnątrz maleńkich pęcherzyków tłuszczu. Prosty zewnętrzny sygnał — trochę fluorku — powoduje, że sztuczna komórka zmienia wzór ładunków swojej błony od wewnątrz, co z kolei kontroluje, jakie białka przylegają do powierzchni i czy wbudowane bramy się otwierają lub zamykają. To podejście zamienia bierne pęcherzyki w reagujące, regulowalne obiekty, które bardziej przypominają komórki żywe. W przyszłości podobne rozwiązania mogłyby pozwolić sztucznym komórkom wykrywać sygnały z guzów, przebudowywać swoje błony i uruchamiać kaskady reakcji lub uwalnianie leków, oferując potężną nową drogę do środowiskowo świadomych, programowalnych mikroskopijnych urządzeń.
Cytowanie: Kamiya, K., Lee, S. & Baba, K. Riboswitch-controlled lipid conversion enables functional membrane asymmetry in artificial cells. Commun Biol 9, 580 (2026). https://doi.org/10.1038/s42003-026-09890-7
Słowa kluczowe: sztuczne komórki, ryboswitch, membrany lipidowe, asymetria membran, biologia syntetyczna