Clear Sky Science · it
La conversione lipidica controllata da un riboswitch abilita l’asimmetria funzionale della membrana in cellule artificiali
Perché costruire cellule finte è importante
Ogni cellula vivente rimodella costantemente la sua pelle esterna—la membrana—per percepire l’ambiente, inviare segnali e restare in vita. Tuttavia la maggior parte delle cellule artificiali prodotte in laboratorio ha membrane statiche e immutabili, cosa che limita quanto possano assomigliare a sistemi viventi. Questo lavoro descrive un modo per dotare le cellule artificiali di una sorta di “pelle programmabile” che può cambiare la propria composizione in risposta a un semplice segnale chimico. Questa capacità potrebbe un giorno permettere a minuscole cellule sintetiche di rilevare malattie, rilasciare farmaci su richiesta o aiutare gli scienziati a indagare come funzionano le cellule vere dall’esterno verso l’interno.
Un interruttore che risponde a un sale semplice
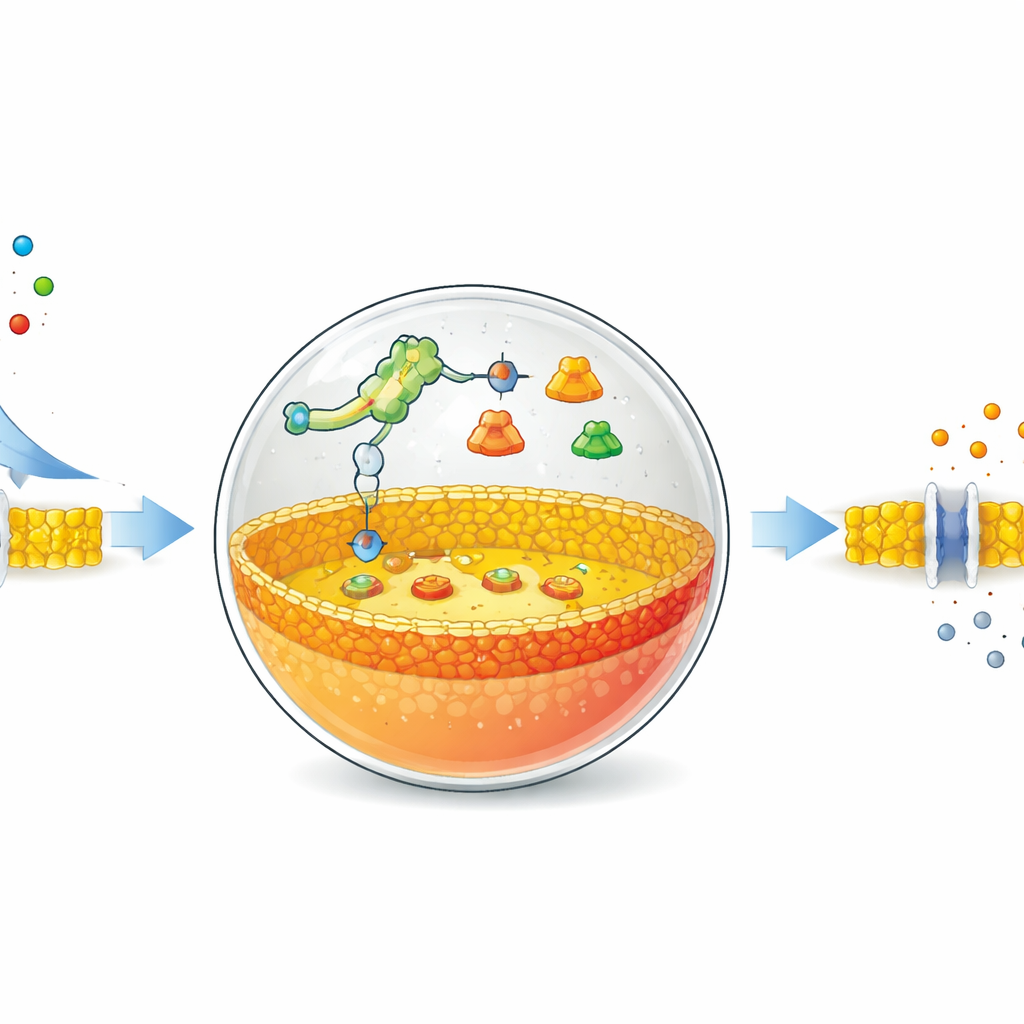
Gli autori partono da bolle cave fatte di molecole lipidiche, simili a quelle che formano le membrane cellulari naturali. All’interno di queste bolle inseriscono un sistema minimalista per la sintesi proteica e istruzioni di DNA speciali. Al centro del progetto c’è un riboswitch—un segmento di RNA che cambia forma quando si lega a una piccola molecola e così accende o spegne la produzione proteica. Qui il riboswitch è tarato per rispondere agli ioni fluoruro ordinari, come quelli del fluoruro di sodio. Quando il fluoruro attraversa la membrana e entra nella bolla, il riboswitch attiva il programma genetico e avvia la produzione di un enzima specifico.
Riscrivere la membrana dall’interno
L’enzima scelto è la fosfolipasi D, una proteina che taglia e modifica i lipidi. In queste cellule artificiali la membrana iniziale è costituita principalmente da un lipide neutro chiamato fosfatidilcolina. La fosfolipasi D neoformata agisce solo sulla metà interna della membrana, convertendo alcuni di questi lipidi neutri in lipidi carichi negativamente chiamati acidi fosfatidici. Di conseguenza la membrana diventa asimmetrica: il lato interno risulta più carico negativamente rispetto al lato esterno. Utilizzando sonde fluorescenti che si legano all’acido fosfatidico, il gruppo ha seguito questo cambiamento nel tempo. Hanno dimostrato che modulando la quantità di DNA e di fluoruro era possibile controllare la velocità e l’intensità della ristrutturazione della membrana interna, con variazioni significative che comparivano entro circa un’ora.
Mantenere lo squilibrio
In membrane morbide e fluide, le molecole lipidiche tendono a spostarsi lentamente da un lato all’altro, il che cancellerebbe l’asimmetria creata con cura. Per contrastare questo effetto i ricercatori hanno aggiunto colesterolo, un componente rigidizzante presente anche nelle membrane delle cellule umane. Con il colesterolo presente, i lipidi negativi neoformati rimanevano per lo più sul lato interno per almeno 90 minuti, mentre molto meno di essi trapelava sul lato esterno. Confrontando bolle con e senza colesterolo e stimando quante molecole lipidiche modificate apparivano su ciascun lato, hanno mostrato che il colesterolo rallenta il flip‑flop di questi lipidi e aiuta a preservare un’asimmetria di lunga durata—una caratteristica importante delle membrane cellulari reali.
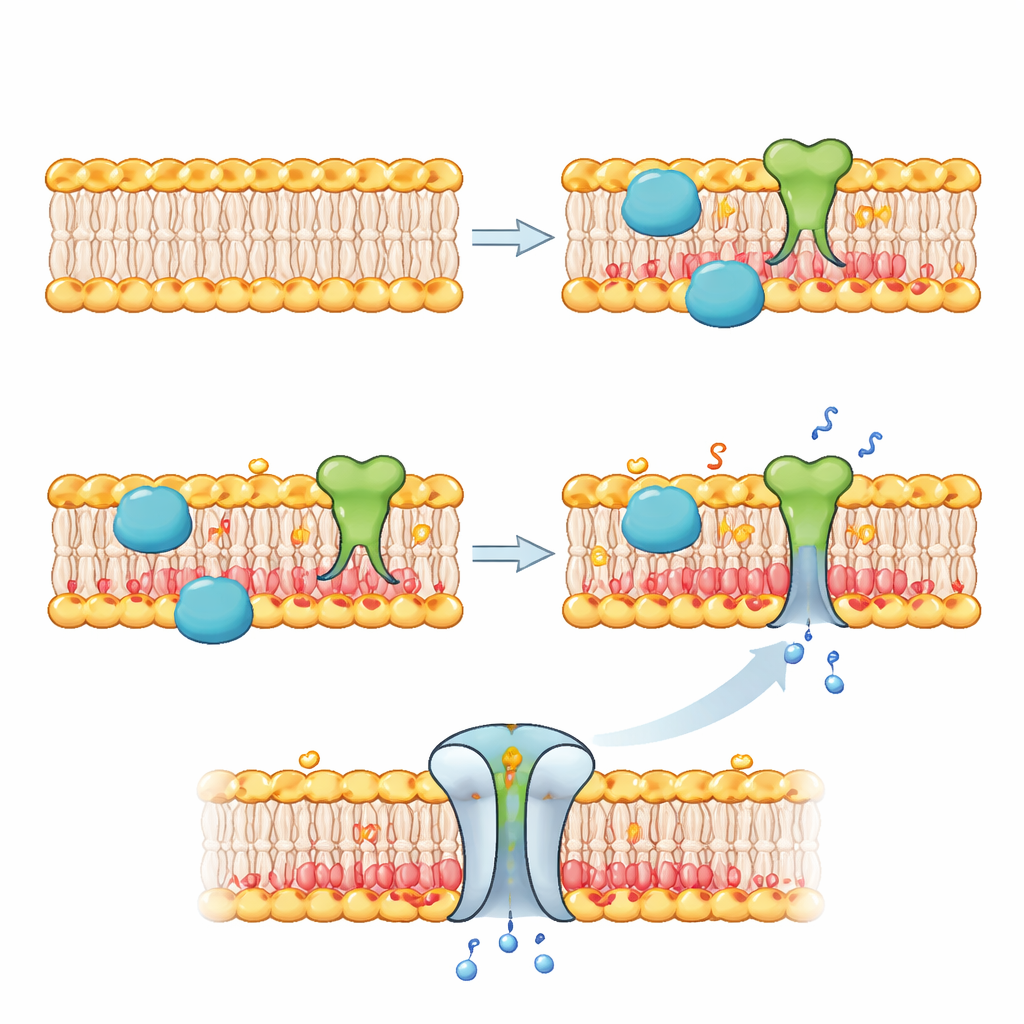
Ancoraggio di proteine e apertura di porte
Una volta in grado di riscrivere la membrana interna, gli autori hanno sfruttato questa nuova chimica per controllare ciò che accade al confine della cellula artificiale. In una serie di esperimenti hanno usato una variante dell’attività enzimatica per aggiungere maniglie “clickabili” ai lipidi della foglia interna, quindi hanno ancorato a queste maniglie una proteina fluorescente. Solo dopo l’aggiunta di fluoruro le proteine si sono raccolte lungo la membrana, dimostrando il reclutamento proteico dipendente dallo stimolo. In un altro test chiave hanno inserito nella membrana una proteina canale naturale chiamata MscL. Questo canale tende ad aprirsi quando rileva lipidi negativi e tensione. Quando la fosfolipasi D ha accumulato lipidi negativi sul lato interno dopo l’aggiunta di fluoruro, i pori MscL si sono aperti permettendo a piccole molecole coloranti di fluire nelle bolle, rendendole visibilmente luminose—una prova chiara che la ristrutturazione della membrana può attivare una proteina di membrana da uno stato inattivo a uno attivo.
Dalle pelli programmabili a cellule sintetiche intelligenti
Per un non specialista il messaggio fondamentale è che i ricercatori hanno collegato tra loro un sensore chimico, un interruttore genetico e un enzima che modifica la membrana all’interno di piccole bolle lipidiche. Un segnale esterno semplice—un po’ di fluoruro—fa sì che la cellula artificiale cambi il profilo di carica della sua membrana dall’interno, controllando così quali proteine si attaccano alla superficie e se i canali integrati si aprono o si chiudono. Questo approccio trasforma bolle altrimenti passive in oggetti reattivi e regolabili che somigliano di più alle cellule viventi. Guardando al futuro, schemi simili potrebbero permettere a cellule artificiali di rilevare segnali da tumori, rimodellare le loro membrane e scatenare catene di reazioni o il rilascio di farmaci, offrendo una nuova via potente per dispositivi microscopici programmabili e sensibili all’ambiente.
Citazione: Kamiya, K., Lee, S. & Baba, K. Riboswitch-controlled lipid conversion enables functional membrane asymmetry in artificial cells. Commun Biol 9, 580 (2026). https://doi.org/10.1038/s42003-026-09890-7
Parole chiave: cellule artificiali, riboswitch, membrane lipidiche, asimmetria di membrana, biologia sintetica