Clear Sky Science · es
La conversión lipídica controlada por un riboswitch permite asimetría funcional de la membrana en células artificiales
Por qué importa construir células falsas
Toda célula viva remodela constantemente su piel exterior—la membrana—para detectar el entorno, enviar señales y mantenerse con vida. Sin embargo, la mayoría de las células artificiales fabricadas en el laboratorio tienen membranas estáticas e inmutables, lo que limita cuán parecidas a las reales pueden ser. Este artículo describe una forma de dotar a las células artificiales de una especie de “piel programable” capaz de cambiar su composición en respuesta a una señal química simple. Esa capacidad podría, en el futuro, permitir que células sintéticas diminutas detecten enfermedades, liberen fármacos bajo demanda o ayuden a los científicos a investigar cómo funcionan las células reales desde el exterior hacia el interior.
Un interruptor que escucha una sal simple
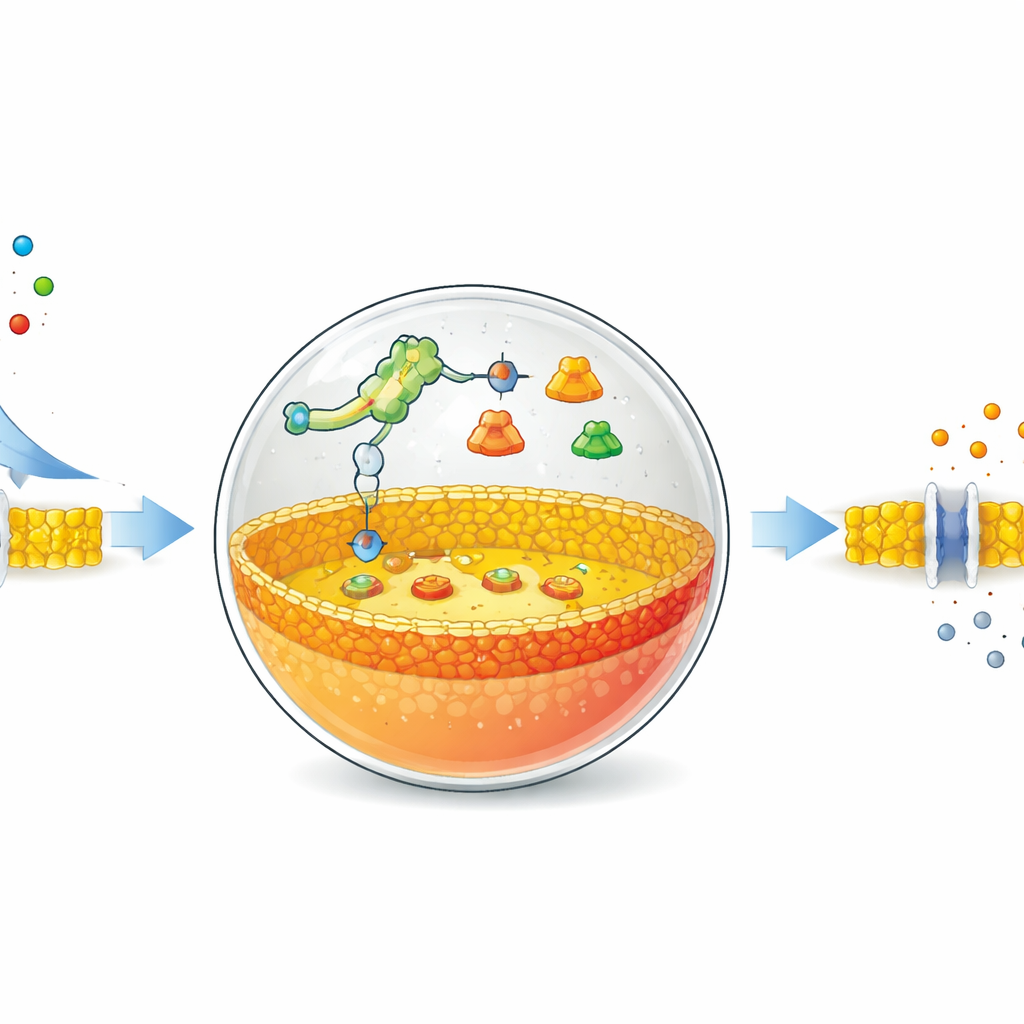
Los autores parten de burbujas huecas hechas de moléculas grasas, similares a las que forman las membranas celulares naturales. En el interior de estas burbujas colocan un sistema reducido de síntesis proteica y unas instrucciones de ADN especiales. El elemento central de su diseño es un riboswitch—un segmento de ARN que cambia de forma cuando se une a una molécula pequeña concreta y que, al hacerlo, activa o desactiva la producción de proteínas. Aquí, el riboswitch está ajustado para responder a iones de fluoruro ordinarios, como los procedentes del fluoruro sódico. Cuando el fluoruro atraviesa la membrana y entra en la burbuja, el riboswitch activa el programa del ADN y ordena la producción de una enzima específica.
Reescribiendo la membrana desde el interior
La enzima elegida es la fosfolipasa D, una proteína que corta y modifica moléculas grasas. En estas células artificiales, la membrana inicial está formada mayoritariamente por una grasa neutra llamada fosfatidilcolina. La fosfolipasa D recién sintetizada actúa únicamente sobre la mitad interna de la membrana, convirtiendo algunas de estas grasas neutras en otras cargadas negativamente llamadas ácido fosfatídico. Como resultado, la membrana se vuelve asimétrica: el lado interno queda más cargado negativamente que el externo. Usando sondas fluorescentes que se unen al ácido fosfatídico, el equipo siguió este cambio a lo largo del tiempo. Mostraron que, al ajustar la cantidad de ADN y de fluoruro, podían controlar la velocidad y la intensidad con que se remodelaba la membrana interna, con cambios significativos que aparecían en aproximadamente una hora.
Conservando el desequilibrio
En membranas blandas y fluidas, las moléculas grasas derivan lentamente de un lado a otro, lo que borraría el desequilibrio cuidadosamente creado. Para contrarrestarlo, los investigadores añadieron colesterol, un componente que rigidiza y que también abunda en las membranas humanas. Con colesterol presente, los lípidos nuevos y negativos permanecieron mayormente en el lado interno durante al menos 90 minutos, mientras que mucho menos de ellos se filtró al lado externo. Comparando burbujas con y sin colesterol y estimando cuántos lípidos modificados aparecían en cada cara, demostraron que el colesterol ralentiza el flip‑flop de estas moléculas y ayuda a preservar una asimetría duradera—una característica importante de las membranas celulares reales.
Anclar proteínas y abrir compuertas
Una vez que pudieron reescribir la membrana interna, los autores emplearon esta nueva química para controlar lo que sucede en el límite de la célula artificial. En un conjunto de experimentos usaron una actividad variante de la misma enzima para añadir asas «clicables» sobre los lípidos de la monocapa interna y, a continuación, anclaron una proteína fluorescente a esas asas. Solo cuando se añadió fluoruro las proteínas se acumularon a lo largo de la membrana, demostrando reclutamiento proteico dependiente del estímulo. En otra prueba clave, incorporaron a la membrana una proteína de puerta natural llamada MscL. Este canal tiende a abrirse cuando detecta lípidos negativos y tensión. A medida que la fosfolipasa D acumulaba lípidos negativos en la cara interna tras la adición de fluoruro, los poros de MscL se abrieron y permitieron que pequeñas moléculas de tinte entraran en las burbujas, haciéndolas visiblemente brillantes—evidencia clara de que la remodelación de la membrana puede cambiar una proteína de membrana de un estado inactivo a uno activo.
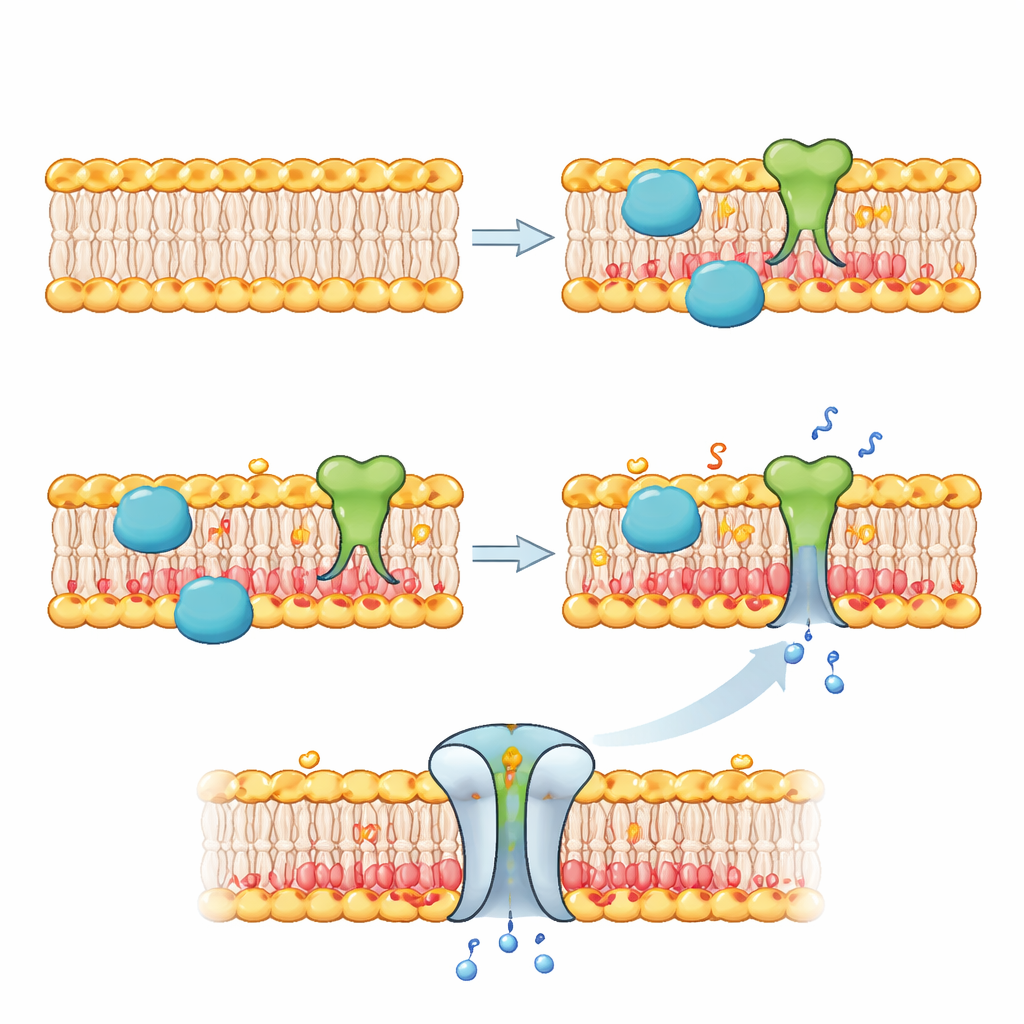
De pieles programables a células sintéticas inteligentes
Para un público no especialista, el mensaje principal es que los investigadores han conectado un sensor químico, un interruptor genético y una enzima editora de membranas dentro de diminutas burbujas grasas. Una señal externa sencilla—un poco de fluoruro—hace que la célula artificial cambie el patrón de carga de su membrana desde el interior, lo que a su vez controla qué proteínas se adhieren a la superficie y si las puertas incorporadas se abren o cierran. Este enfoque convierte burbujas pasivas en objetos sensibles y ajustables que se parecen más a las células vivas. Mirando hacia el futuro, esquemas similares podrían permitir que las células artificiales detecten señales de tumores, remodelen sus membranas y desencadenen cascadas de reacciones o la liberación de fármacos, ofreciendo una nueva vía potente para dispositivos microscópicos programables y conscientes del entorno.
Cita: Kamiya, K., Lee, S. & Baba, K. Riboswitch-controlled lipid conversion enables functional membrane asymmetry in artificial cells. Commun Biol 9, 580 (2026). https://doi.org/10.1038/s42003-026-09890-7
Palabras clave: células artificiales, riboswitch, membranas lipídicas, asimetría de membrana, biología sintética