Clear Sky Science · fr
Une conversion lipidique contrôlée par un riboswitch permet une asymétrie membranaire fonctionnelle dans des cellules artificielles
Pourquoi il est important de fabriquer de fausses cellules
Chaque cellule vivante remodèle en permanence sa peau externe — la membrane — pour détecter son environnement, transmettre des signaux et rester en vie. Pourtant, la plupart des cellules artificielles fabriquées en laboratoire ont des membranes figées et inertes, ce qui limite leur réalisme. Cet article décrit une méthode pour doter les cellules artificielles d’une sorte de « peau programmable » capable de modifier sa composition en réponse à un simple signal chimique. Cette capacité pourrait un jour permettre à de minuscules cellules synthétiques de détecter des maladies, libérer des médicaments à la demande ou aider les scientifiques à explorer le fonctionnement des cellules réelles de l’extérieur vers l’intérieur.
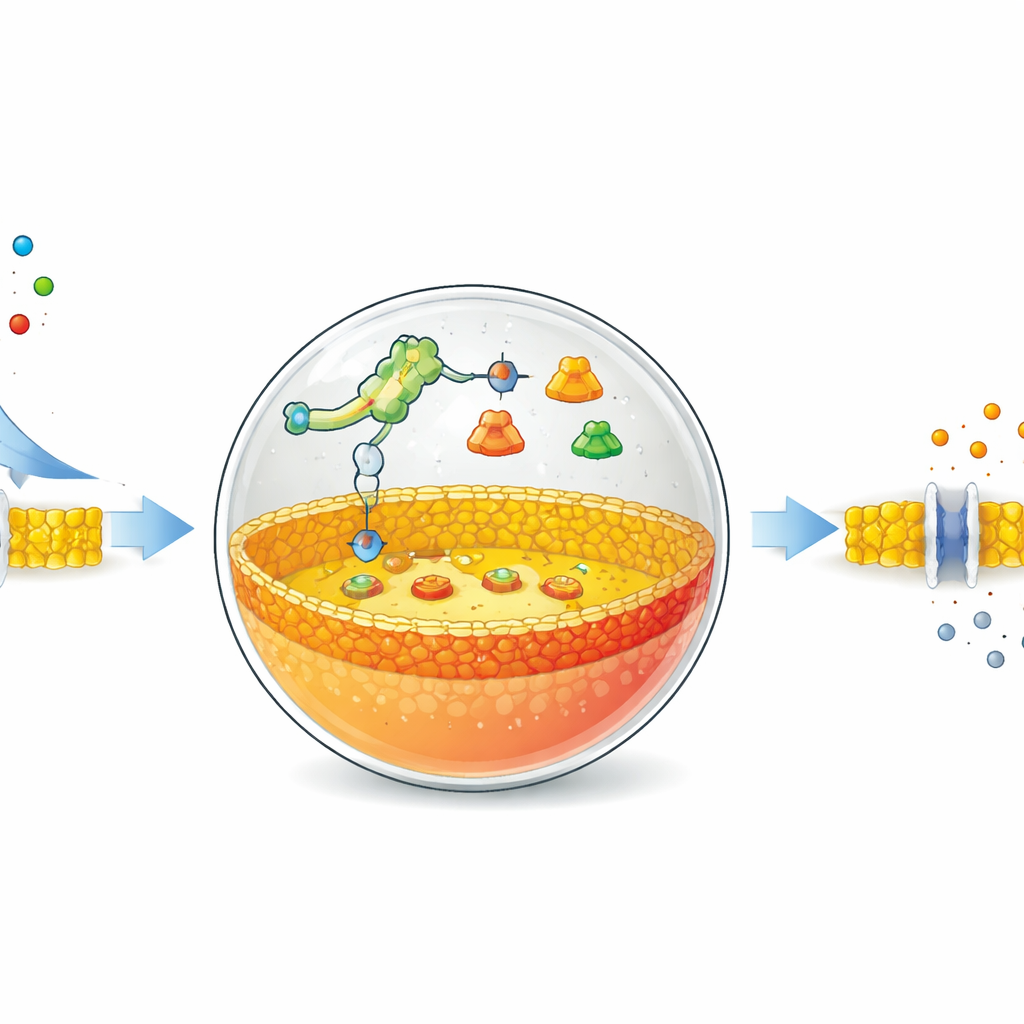
Un interrupteur qui écoute un sel simple
Les auteurs partent de bulles creuses constituées de molécules grasses, similaires à celles qui forment les membranes cellulaires naturelles. À l’intérieur de ces bulles, ils placent un système de production protéique réduit et des instructions génétiques spéciales. L’élément central de leur conception est un riboswitch — un segment d’ARN qui change de conformation lorsqu’il se lie à une petite molécule particulière et, ce faisant, active ou désactive la production protéique. Ici, le riboswitch est réglé pour répondre aux ions fluorure ordinaires, comme ceux du fluorure de sodium. Quand le fluorure traverse la membrane et pénètre dans la bulle, le riboswitch active le programme génétique et commande la production d’une enzyme spécifique.
Réécrire la membrane de l’intérieur
L’enzyme choisie est la phospholipase D, une protéine qui coupe et modifie les molécules grasses. Dans ces cellules artificielles, la membrane initiale est composée principalement d’un lipide neutre appelé phosphatidylcholine. La phospholipase D nouvellement synthétisée agit uniquement sur la moitié interne de la membrane, convertissant une partie de ces lipides neutres en lipides chargés négativement appelés acide phosphatidique. En conséquence, la membrane devient asymétrique : la face interne est plus chargée négativement que la face externe. À l’aide de sondes fluorescentes qui se lient à l’acide phosphatidique, l’équipe a suivi cette modification au fil du temps. Ils ont montré qu’en modulant la quantité d’ADN et de fluorure, ils pouvaient contrôler la vitesse et l’intensité du remodelage de la face interne de la membrane, avec des changements significatifs apparaissant en environ une heure.
Maintenir le déséquilibre en place
Dans des membranes souples et fluides, les lipides dérivent lentement d’un feuillet à l’autre, ce qui effacerait le déséquilibre soigneusement créé. Pour contrer cela, les chercheurs ont ajouté du cholestérol, un composant rigidifiant également abondant dans les membranes cellulaires humaines. En présence de cholestérol, les lipides négatifs nouvellement formés sont restés majoritairement du côté interne pendant au moins 90 minutes, tandis qu’une bien moindre proportion migrait vers la face externe. En comparant des bulles avec et sans cholestérol et en estimant combien de lipides modifiés apparaissaient de chaque côté, ils ont montré que le cholestérol ralentit le basculement (flip‑flop) de ces molécules et aide à préserver une asymétrie durable — une caractéristique importante des membranes réelles.
Ancrer des protéines et ouvrir des portes
Une fois capables de réécrire la face interne de la membrane, les auteurs ont utilisé cette nouvelle chimie pour contrôler ce qui se passe à la frontière de la cellule artificielle. Dans une série d’expériences, ils ont employé une activité variante de la même enzyme pour attacher des poignées « cliquables » sur les lipides du feuillet interne, puis ancrer une protéine fluorescente à ces poignées. Ce n’est que lorsque le fluorure a été ajouté que les protéines se sont rassemblées le long de la membrane, démontrant un recrutement protéique dépendant du stimulus. Dans un autre test clé, ils ont inséré une protéine canal naturelle appelée MscL dans la membrane. Ce canal a tendance à s’ouvrir lorsqu’il détecte des lipides négatifs et de la tension. À mesure que la phospholipase D accumulait des lipides négatifs sur la face interne après l’ajout de fluorure, les pores MscL se sont ouverts et ont permis à de petits colorants de pénétrer dans les bulles, les rendant visiblement brillantes — une preuve claire que le remodelage membranaire pouvait basculer une protéine membranaire d’un état inactif à un état actif.
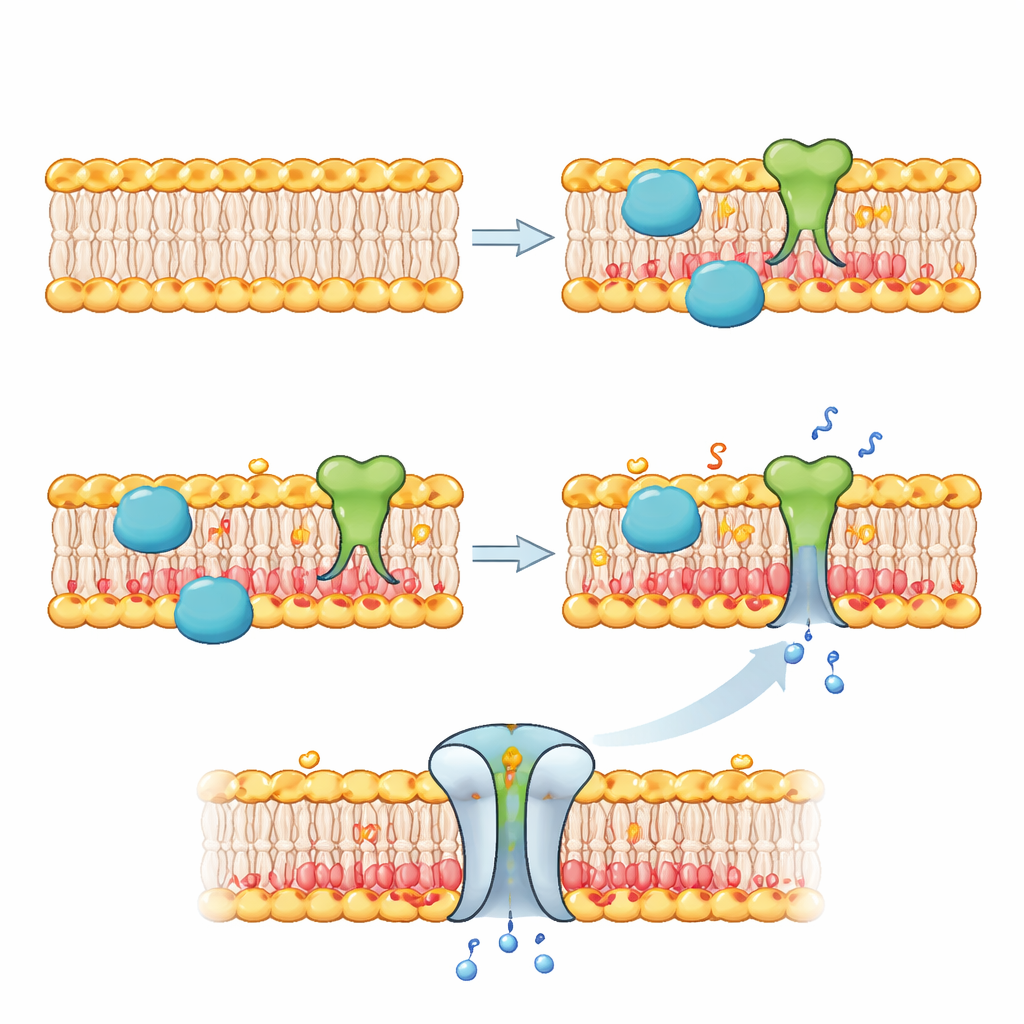
De peaux programmables à des cellules synthétiques intelligentes
Pour un non‑spécialiste, l’idée principale est que les chercheurs ont connecté un capteur chimique, un interrupteur génétique et une enzyme éditrice de membrane à l’intérieur de petites bulles lipidiques. Un simple signal externe — une petite quantité de fluorure — provoque un changement de la répartition des charges de la membrane depuis l’intérieur, ce qui contrôle à son tour quelles protéines adhèrent à la surface et si des portes intégrées s’ouvrent ou se ferment. Cette approche transforme des bulles par ailleurs passives en objets réactifs et ajustables qui ressemblent davantage à des cellules vivantes. À l’avenir, des dispositifs similaires pourraient permettre à des cellules artificielles de détecter des signaux provenant de tumeurs, de remodeler leurs membranes et de déclencher des cascades de réactions ou la libération de médicaments, offrant une nouvelle voie puissante vers des dispositifs microscopiques programmables et sensibles à leur environnement.
Citation: Kamiya, K., Lee, S. & Baba, K. Riboswitch-controlled lipid conversion enables functional membrane asymmetry in artificial cells. Commun Biol 9, 580 (2026). https://doi.org/10.1038/s42003-026-09890-7
Mots-clés: cellules artificielles, riboswitch, membranes lipidiques, asymétrie membranaire, biologie synthétique