Clear Sky Science · sv
MOF-medierad H4K16ac är avgörande för blastocystbildning hos får genom att forma promotorers tillgänglighet och transkription
Varför små fårembryon betyder något för oss
Innan en graviditet kan sitta säkert måste ett befruktat ägg omvandlas till en liten ihålig cellkula kallad blastocyst. Detta korta fönster, bara dagar efter befruktningen, är när de första cellöden bestäms och när många graviditeter tyst avbryts. I människor och produktionsdjur är förmågan att odla friska blastocyster i laboratoriet central för in vitro-fertilisering och djuravel. Denna studie granskar fårembryon för att förstå hur en specifik kemisk markör på DNA-paketerande proteiner hjälper embryon att framgångsrikt nå blastocyststadiet.
En närmare titt på livets första dagar
Hos däggdjur sker resan från befruktat ägg till blastocyst på under en vecka. Under denna period måste embryot först aktivera sitt eget genom och sedan sortera sina celler till en inre klump som blir fostret och ett yttre skal som blir moderkakan. Dessa omfattande förändringar styrs inte bara av gener utan också av epigenetiska markörer — små kemiska flaggor på DNA och dess associerade proteiner som talar om för gener när de ska slås på eller av. Författarna fokuserade på en sådan markör, kallad H4K16-acetylering, som skrivs av ett enzym känt som MOF. Tidigare arbete i möss, flugor och humana celler hade antytt att denna markör är kopplad till aktiva gener och tidig utveckling, men dess roll i produktionsdjursembryon var till stor del outforskad.
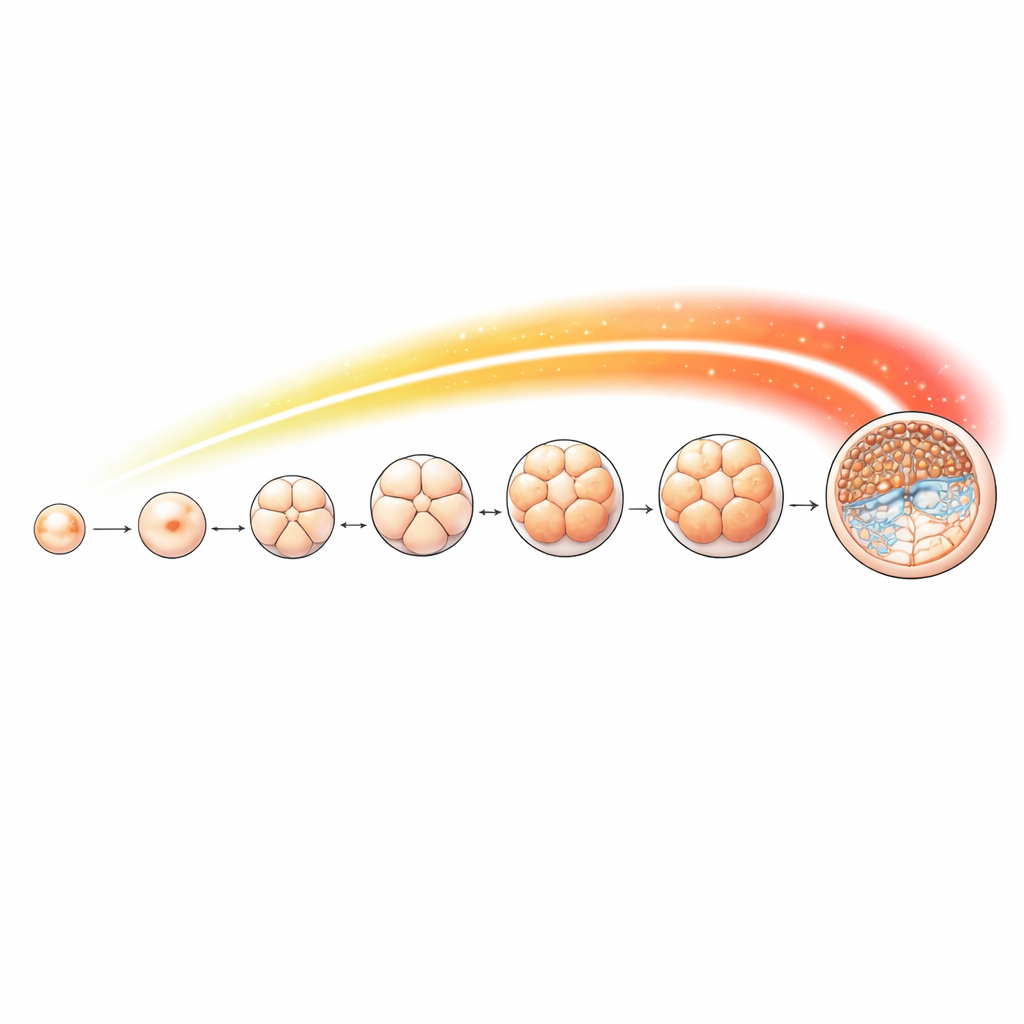
Kartläggning av en kemisk signal under tidig utveckling
För att följa denna markör i detalj samlade teamet fårägg och embryon vid viktiga stadier, från obefruktade oocyter genom 2-, 4-, 8- och 16-cellstadier, morula och slutligen blastocyst. De använde en känslig metod för att kartlägga var H4K16-acetylering sitter längs genomet vid varje steg. Markören var närvarande under hela utvecklingen men förändrades på ett stadiumspecifikt sätt. En särskilt tydlig ökning skedde från 8-cellstadiet och framåt, i samklang med den tid då embryots egna gener tar över kontrollen. Många av de platser där markören ansamlades låg nära genstarters regioner som styr viktiga cellulära processer såsom RNA-bearbetning, kromosomsegregering och DNA-replikation — uppgifter som är särskilt krävande när cellerna snabbt delar sig och blir specialiserade.
Vad händer när skrivarenzymet blockeras
För att testa om denna markör verkligen är nödvändig använde forskarna små molekyler för att hämma MOF:s aktivitet i tidiga embryon odlade i kultur. Blockering av MOF minskade drastiskt andelen embryon som nådde blastocyststadiet och orsakade att många stannade upp kring 8- till 16-cellstadiet. När teamet undersökte blastocyster som ändå bildades under MOF-hämning fann de omfattande störningar i genaktiviteten: tusentals gener var upp- eller nedreglerade jämfört med obehandlade kontroller. Gener som normalt bar stark H4K16-acetylering kring sina startreglage tenderade att tystna när den markören försvann. Många av dessa gener tillhör vägar som är avgörande för hantering av RNA, uppbyggnad av ribosomer och transport av molekyler in och ut ur kärnan — kärnuppgifter för ett växande embryo.
Att öppna genomet för transkription
Studien gick vidare genom att undersöka hur tillgängligt DNA var och var cellens huvudsakliga genläsarmaskin, RNA-polymeras II, befann sig. Regioner som var rika på H4K16-acetylering visade mer öppet kromatin — den lösare formen av DNA-paketering som tillåter molekylära maskiner att nå gener. Dessa samma regioner hyste också mer RNA-polymeras II. När MOF blockerades blev platser som förlorade markören mindre tillgängliga och visade minskad bindning av RNA-polymeras II, och närliggande gener uttrycktes på lägre nivåer. Med andra ord verkar H4K16-acetylering fungera som en dörrklinka som håller genreglagen fysiskt öppna så att transkriptionsmaskineriet kan binda och arbeta effektivt.
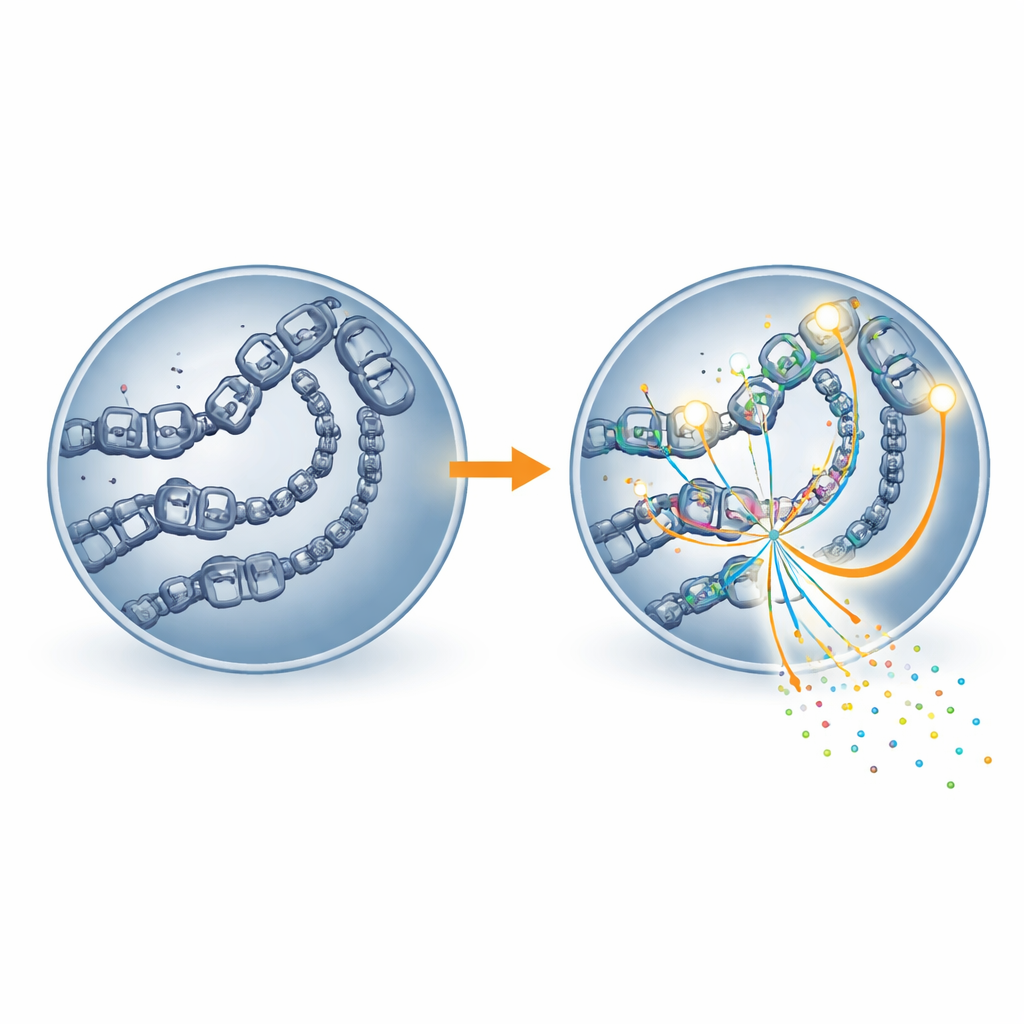
Konsekvenser för fertilitet och assisterad reproduktion
Genom att kombinera genomomfattande kartor, mätningar av genaktivitet och funktionella tester drar författarna slutsatsen att MOF-beroende H4K16-acetylering är en kritisk epigenetisk kontrollpunkt i fårembryon. När detta system fungerar korrekt hjälper det till att forma öppna, tillgängliga regioner vid viktiga genpromotorer, rekryterar RNA-polymeras II och stödjer de ordnade genprogram som behövs för att bygga en frisk blastocyst. När systemet störs går utvecklingen snett. Eftersom fårembryon delar många egenskaper med mänskliga embryon och ofta används som modeller, tyder fynden på att denna särskilda epigenetiska markör — och MOF-enzymet som skriver den — skulle kunna bli en användbar indikator på embryokvalitet och ett potentiellt mål för att förbättra framgången hos assisterade reproduktionstekniker.
Citering: Wang, L., Chen, B., Chen, X. et al. MOF-mediated H4K16ac is critical for blastocyst formation in sheep by shaping promoter accessibility and transcription. Commun Biol 9, 609 (2026). https://doi.org/10.1038/s42003-026-09868-5
Nyckelord: blastocystutveckling, epigenetisk reglering, histonacetylering, RNA-polymeras II, assisterad reproduktion