Clear Sky Science · it
H4K16ac mediata da MOF è critica per la formazione del blastocisto nelle pecore modellando l’accessibilità dei promotori e la trascrizione
Perché ci interessano gli embrioni di pecora
Prima che una gravidanza possa instaurarsi in sicurezza, un uovo fecondato deve trasformarsi in una piccola sfera cava di cellule chiamata blastocisto. Questa finestra temporale, pochi giorni dopo la fecondazione, è quando si decidono i primi destini cellulari e quando molte gravidanze falliscono silenziosamente. Negli esseri umani e negli animali da allevamento, la capacità di coltivare blastocisti sani in laboratorio è fondamentale per la fecondazione in vitro e la selezione riproduttiva. Questo studio esamina gli embrioni di pecora per capire come un particolare segnale chimico sugli istoni aiuti gli embrioni a raggiungere con successo lo stadio di blastocisto.
Uno sguardo ravvicinato ai primi giorni di vita
Nei mammiferi, il percorso dall’uovo fecondato al blastocisto avviene in meno di una settimana. Durante questo periodo, l’embrione deve prima attivare il proprio genoma e poi dividere le cellule in un ammasso interno che formerà il feto e in uno strato esterno che diventerà la placenta. Questi ampi cambiamenti sono guidati non solo dai geni, ma anche da marchi epigenetici—picule bandierine chimiche sul DNA e sulle proteine associate che indicano quando i geni devono accendersi o spegnersi. Gli autori si sono concentrati su uno di questi marchi, chiamato acetilazione di H4K16, che viene applicato da un enzima noto come MOF. Lavori precedenti in topo, mosca e cellule umane avevano suggerito che questo marchio è legato ai geni attivi e allo sviluppo precoce, ma il suo ruolo negli embrioni del bestiame era rimasto in gran parte inesplorato.
Mappare un segnale chimico durante lo sviluppo precoce
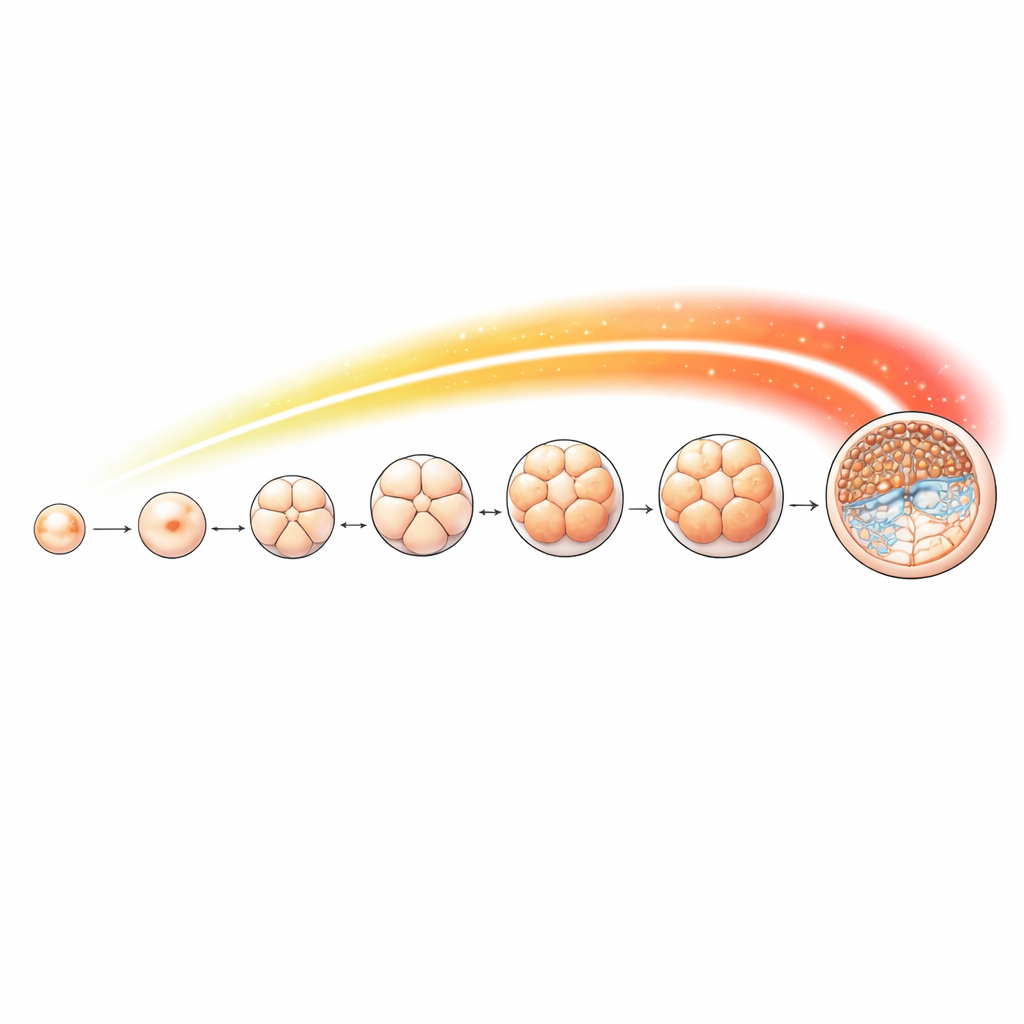
Per seguire questo marchio in dettaglio, il team ha raccolto ovociti ed embrioni di pecora in stadi chiave, dall’ovocita non fecondato fino agli stadi a 2, 4, 8 e 16 cellule, alla morula e infine al blastocisto. Hanno usato un metodo sensibile per mappare dove l’acetilazione di H4K16 è presente lungo il genoma a ciascuna tappa. Il marchio era presente durante tutto lo sviluppo ma variava in modo specifico per stadio. Un aumento particolarmente netto si è osservato a partire dallo stadio a 8 cellule, coincidente con il momento in cui i geni dell’embrione prendono il controllo. Molti dei siti dove il marchio si accumulava si trovavano vicino alle regioni d’inizio dei geni che controllano processi cellulari importanti come l’elaborazione dell’RNA, la segregazione dei cromosomi e la replicazione del DNA—compiti particolarmente impegnativi mentre le cellule si dividono rapidamente e si specializzano.
Cosa accade quando l’enzima scrittore viene bloccato
Per verificare se questo marchio sia davvero necessario, i ricercatori hanno usato piccole molecole per inibire l’attività di MOF in embrioni precoci coltivati in vitro. L’inibizione di MOF ha drasticamente ridotto la frazione di embrioni che raggiungevano lo stadio di blastocisto e ha fatto sì che molti rimanessero bloccati attorno alla fase da 8 a 16 cellule. Quando il team ha esaminato i blastocisti che si formavano nonostante l’inibizione di MOF, ha riscontrato una diffusa alterazione dell’attività genica: migliaia di geni risultavano up- o down-regolati rispetto ai controlli non trattati. I geni che normalmente presentano forte acetilazione di H4K16 attorno ai loro elementi di avvio tendevano a spegnersi quando quel marchio veniva perso. Molti di questi geni appartengono a vie cruciali per la gestione dell’RNA, per la costruzione dei ribosomi e per il trasporto di molecole dentro e fuori dal nucleo—compiti fondamentali per un embrione in crescita.
Aprire le porte del genoma alla trascrizione
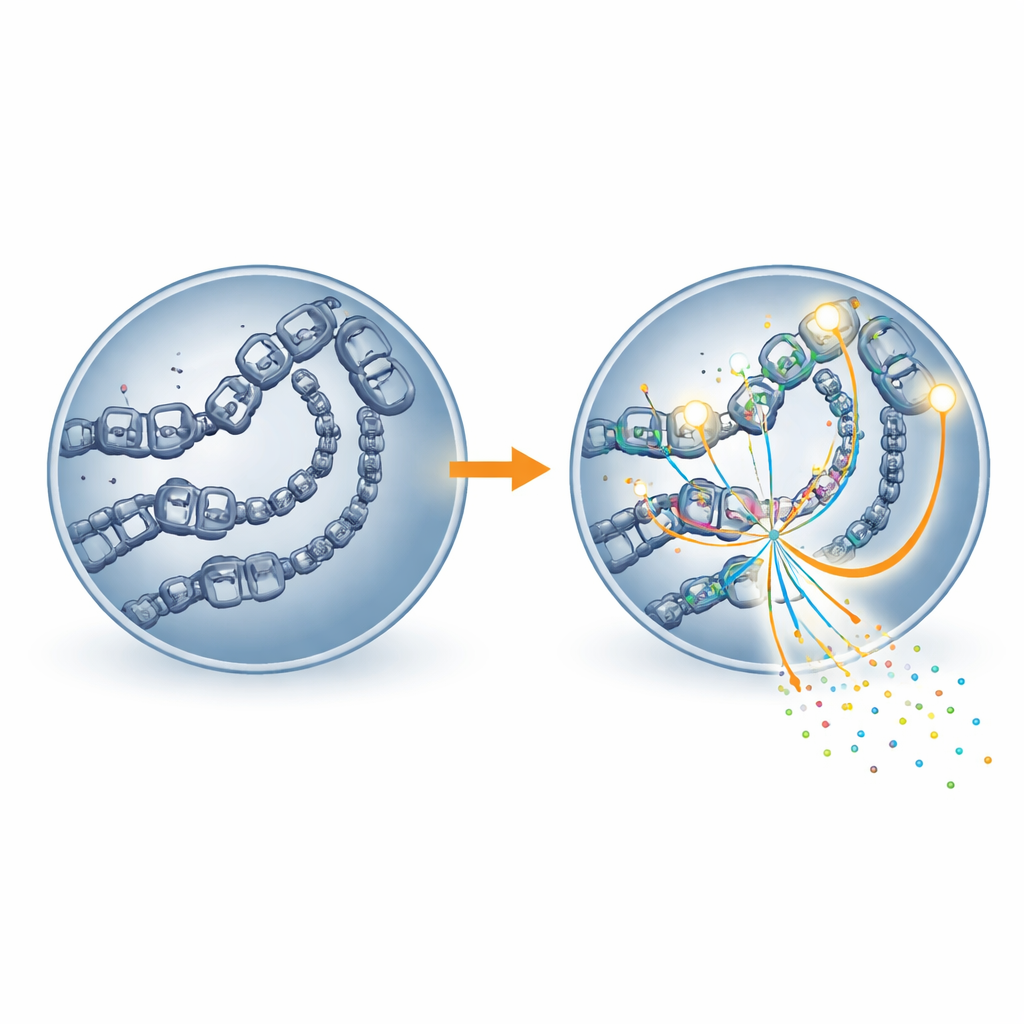
Lo studio è andato oltre esaminando quanto fosse accessibile il DNA e dove si trovasse la principale macchina di lettura genica della cellula, l’RNA polimerasi II. Le regioni arricchite di acetilazione di H4K16 mostravano una cromatina più aperta—la forma più lassa dell’impacchettamento del DNA che consente alle macchine molecolari di raggiungere i geni. Queste stesse regioni ospitavano anche più RNA polimerasi II. Quando MOF è stato bloccato, i siti che perdevano il marchio diventavano meno accessibili e mostravo una minore occupazione da parte dell’RNA polimerasi II, e i geni vicini venivano espressi a livelli inferiori. In altre parole, l’acetilazione di H4K16 sembra funzionare come un fermaporta che mantiene i regolatori genici fisicamente aperti così che la macchina di trascrizione possa legarsi e operare in modo efficiente.
Implicazioni per fertilità e riproduzione assistita
Combinando mappe genome-wide, misure dell’attività genica e test funzionali, gli autori concludono che l’acetilazione di H4K16 dipendente da MOF è un checkpoint epigenetico critico negli embrioni di pecora. Quando questo sistema funziona correttamente, contribuisce a plasmare regioni aperte e accessibili presso promotori genici chiave, richiama l’RNA polimerasi II e supporta i programmi genici ordinati necessari per costruire un blastocisto sano. Quando il sistema è compromesso, lo sviluppo vacilla. Poiché gli embrioni di pecora condividono molte caratteristiche con quelli umani e sono ampiamente usati come modelli, i risultati suggeriscono che questo particolare marchio epigenetico—e l’enzima MOF che lo applica—potrebbero diventare un indicatore utile della qualità embrionale e un potenziale bersaglio per migliorare il successo delle tecnologie di riproduzione assistita.
Citazione: Wang, L., Chen, B., Chen, X. et al. MOF-mediated H4K16ac is critical for blastocyst formation in sheep by shaping promoter accessibility and transcription. Commun Biol 9, 609 (2026). https://doi.org/10.1038/s42003-026-09868-5
Parole chiave: sviluppo del blastocisto, regolazione epigenetica, acetilazione degli istoni, RNA polimerasi II, riproduzione assistita