Clear Sky Science · pt
H4K16ac mediada por MOF é crítica para a formação do blastocisto em ovinos ao moldar a acessibilidade do promotor e a transcrição
Por que embriões minúsculos de ovelhas importam para nós
Antes que uma gravidez possa se estabelecer com segurança, um óvulo fecundado precisa se transformar em uma pequena esfera oca de células chamada blastocisto. Essa janela breve, poucos dias após a fertilização, é quando os primeiros destinos celulares são decididos e quando muitas gestações falham silenciosamente. Em humanos e em animais de produção, a capacidade de cultivar blastocistos saudáveis em laboratório é central para a fertilização in vitro e para o melhoramento animal. Este estudo examina embriões de ovelha para entender como uma marca química específica nas proteínas que empacotam o DNA ajuda os embriões a alcançar com sucesso o estágio de blastocisto.
Um olhar mais próximo aos primeiros dias de vida
Em mamíferos, a jornada do óvulo fecundado ao blastocisto ocorre em menos de uma semana. Durante esse período, o embrião primeiro precisa ativar seu próprio genoma e depois separar suas células em um aglomerado interno que formará o feto e uma camada externa que se tornará a placenta. Essas mudanças abrangentes são guiadas não apenas pelos genes, mas também por marcas epigenéticas — pequenas sinalizações químicas no DNA e nas proteínas associadas que indicam quando os genes devem ligar ou desligar. Os autores focaram em uma dessas marcas, chamada acetilação de H4K16, que é adicionada por uma enzima conhecida como MOF. Trabalhos anteriores em camundongos, moscas e células humanas sugeriam que essa marca está associada a genes ativos e ao desenvolvimento inicial, mas seu papel em embriões de animais de produção permanecia pouco explorado.
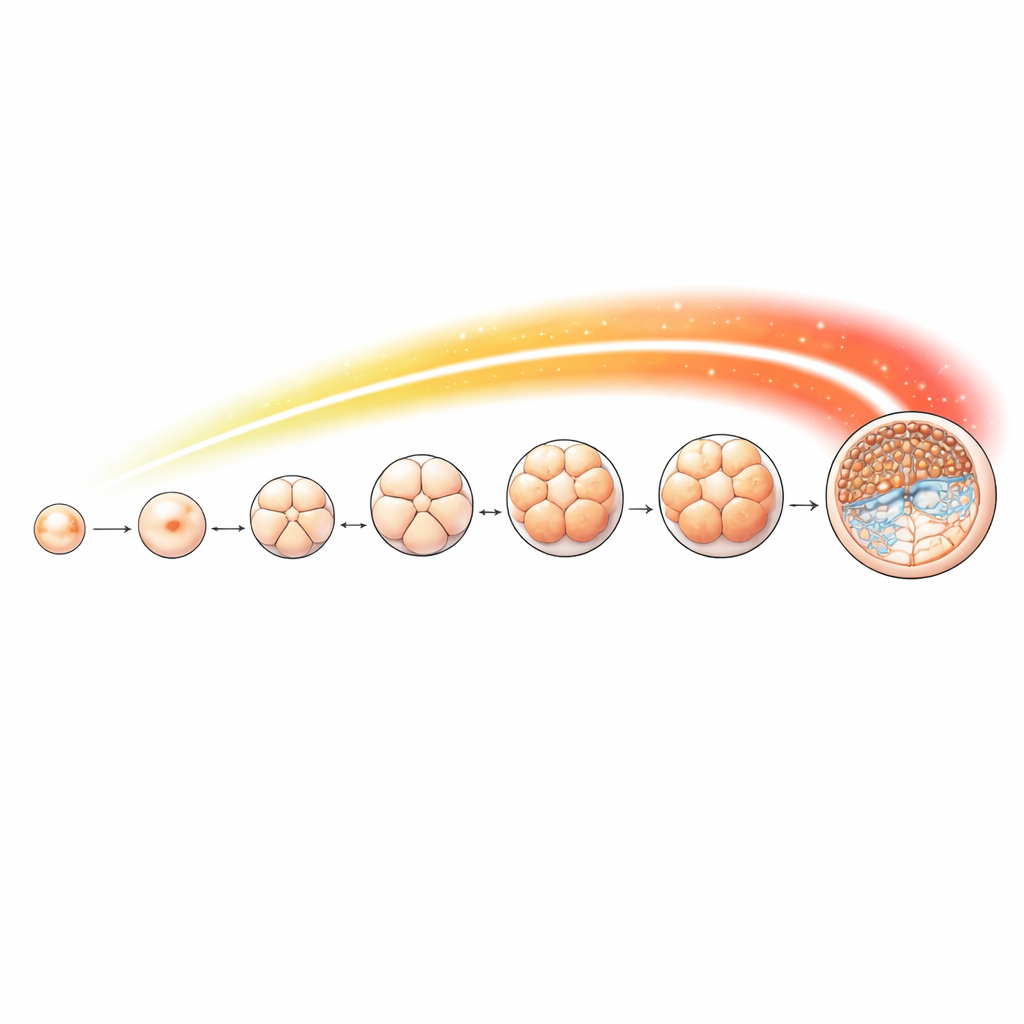
Mapeando um sinal químico ao longo do desenvolvimento inicial
Para rastrear essa marca em detalhe, a equipe coletou óvulos e embriões de ovelha em estágios-chave, desde oócitos não fertilizados até estágios de 2, 4, 8 e 16 células, mórula e, finalmente, blastocisto. Usaram um método sensível para mapear onde a acetilação de H4K16 se localiza ao longo do genoma em cada etapa. A marca estava presente durante todo o desenvolvimento, mas variou de forma específica por estágio. Um aumento particularmente acentuado ocorreu a partir do estágio de 8 células em diante, coincidindo com o momento em que os próprios genes do embrião assumem o controle. Muitos dos locais onde a marca se acumulou situavam-se próximos a regiões de início de genes que controlam processos celulares importantes, como processamento de RNA, segregação de cromossomos e replicação do DNA — tarefas especialmente exigentes quando as células se dividem rapidamente e se especializam.
O que acontece quando a enzima que escreve a marca é bloqueada
Para testar se essa marca é realmente necessária, os pesquisadores usaram pequenas moléculas para inibir a atividade da MOF em embriões iniciais cultivados em laboratório. Bloquear a MOF reduziu drasticamente a fração de embriões que atingiram o estágio de blastocisto e fez muitos estacionarem em torno das fases de 8 a 16 células. Quando a equipe examinou os blastocistos que se formaram sob inibição da MOF, encontrou uma ampla perturbação da atividade gênica: milhares de genes foram regulados para cima ou para baixo em comparação com controles não tratados. Genes que normalmente apresentam forte acetilação de H4K16 em suas regiões de início tendiam a se silenciar quando essa marca era perdida. Muitos desses genes pertencem a vias cruciais para o gerenciamento de RNA, construção de ribossomos e transporte de moléculas dentro e fora do núcleo — tarefas centrais para um embrião em crescimento.
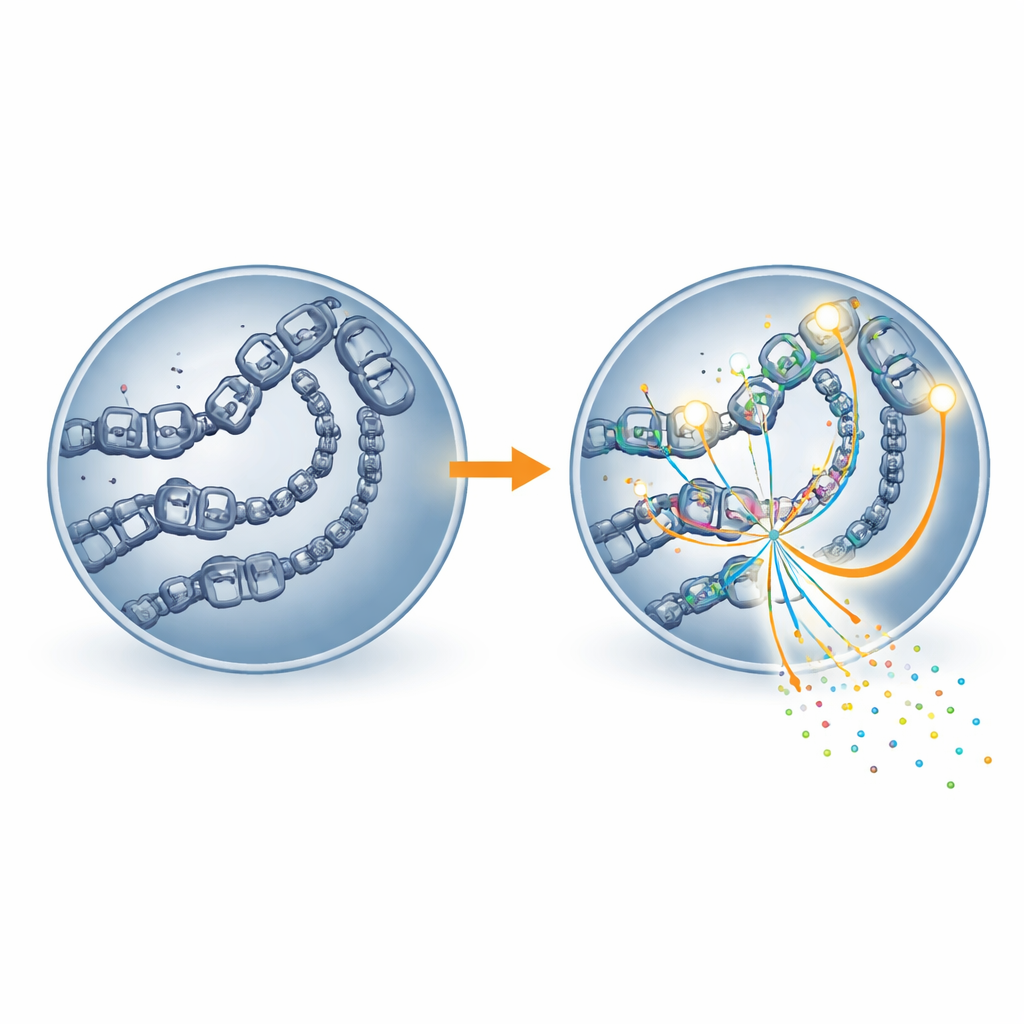
Abrindo as portas do genoma para a transcrição
O estudo avançou ainda mais ao analisar quão acessível estava o DNA e onde a principal maquinaria de leitura gênica da célula, a RNA polimerase II, se posicionava. Regiões enriquecidas em acetilação de H4K16 apresentaram cromatina mais aberta — a forma mais frouxa de empacotamento do DNA que permite que máquinas moleculares alcancem os genes. Essas mesmas regiões também hospedavam mais RNA polimerase II. Quando a MOF foi bloqueada, locais que perderam a marca tornaram-se menos acessíveis e mostraram redução da ocupação pela RNA polimerase II, e os genes próximos foram expressos em níveis mais baixos. Em outras palavras, a acetilação de H4K16 parece atuar como uma cunha que mantém os interruptores gênicos fisicamente abertos para que a maquinaria de transcrição possa se ligar e trabalhar com eficiência.
Implicações para fertilidade e reprodução assistida
Ao combinar mapas genômicos abrangentes, medições de atividade gênica e testes funcionais, os autores concluem que a acetilação de H4K16 dependente de MOF é um ponto de verificação epigenético crítico em embriões de ovelha. Quando esse sistema funciona corretamente, ele ajuda a moldar regiões abertas e acessíveis em promotores gênicos-chave, atrai a RNA polimerase II e sustenta os programas gênicos ordenados necessários para construir um blastocisto saudável. Quando o sistema é perturbado, o desenvolvimento falha. Como embriões de ovelha compartilham muitas características com embriões humanos e são amplamente usados como modelos, os resultados sugerem que essa marca epigenética — e a enzima MOF que a escreve — pode se tornar um indicador útil da qualidade embrionária e um alvo potencial para melhorar o sucesso das tecnologias de reprodução assistida.
Citação: Wang, L., Chen, B., Chen, X. et al. MOF-mediated H4K16ac is critical for blastocyst formation in sheep by shaping promoter accessibility and transcription. Commun Biol 9, 609 (2026). https://doi.org/10.1038/s42003-026-09868-5
Palavras-chave: desenvolvimento do blastocisto, regulação epigenética, acetilação de histonas, RNA polimerase II, reprodução assistida