Clear Sky Science · pl
Acetylacja H4K16 zależna od MOF jest kluczowa dla powstawania blastocysty u owiec poprzez kształtowanie dostępności promotorów i transkrypcji
Dlaczego małe zarodki owiec mają dla nas znaczenie
Zanim ciąża może bezpiecznie się zagnieździć, zapłodnione jajo musi przekształcić się w małą, pustą kulę komórek zwaną blastocystą. Ten krótki etap, zaledwie kilka dni po zapłodnieniu, to moment, w którym zapadają pierwsze decyzje o losie komórek i gdy wiele ciąż przerywa się w sposób niezauważony. Zarówno u ludzi, jak i u zwierząt gospodarskich zdolność do hodowli zdrowych blastocyst in vitro jest kluczowa dla procedur zapłodnienia pozaustrojowego i selekcji hodowlanej. W tej pracy przyglądamy się wnętrzu zarodków owczych, by zrozumieć, jak specyficzna chemiczna etykieta na białkach pakujących DNA pomaga zarodkom pomyślnie osiągnąć stadium blastocysty.
Bliższe spojrzenie na pierwsze dni życia
U ssaków droga od zapłodnionego jaja do blastocysty zajmuje mniej niż tydzień. W tym czasie zarodek musi najpierw uruchomić własne geny, a potem podzielić komórki na wewnętrzną grupeczkę, która stworzy płód, i zewnętrzną powłokę, która stanie się łożyskiem. Te rozległe przemiany są kierowane nie tylko przez sekwencje genów, lecz także przez znaki epigenetyczne — drobne chemiczne flagi na DNA i związanych z nim białkach, które informują, kiedy geny mają być włączane lub wyłączane. Autorzy skupili się na jednym z takich znaków, zwanym acetylacją H4K16, który jest zapisywany przez enzym znany jako MOF. Wcześniejsze badania na myszach, muszkach i komórkach ludzkich sugerowały związek tego znaku z aktywnymi genami i wczesnym rozwojem, ale jego rola w zarodkach zwierząt gospodarskich pozostawała w dużej mierze niepoznana.
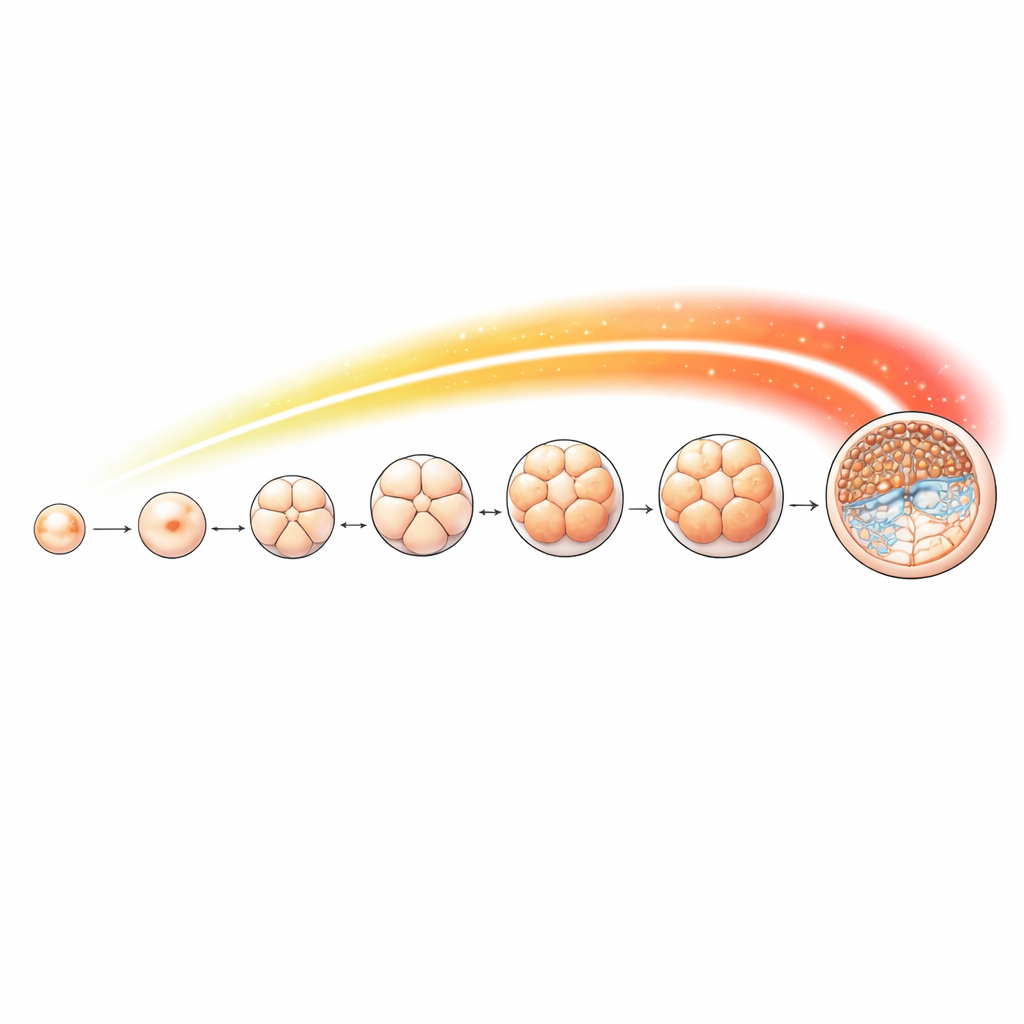
Mapowanie sygnału chemicznego w czasie wczesnego rozwoju
Aby szczegółowo śledzić ten znak, zespół zebrał jaja i zarodki owcze na kluczowych etapach, od niezapłodnionych oocytów przez stadia 2-, 4-, 8- i 16-komórkowe, morulę i wreszcie blastocystę. Użyli czułej metody do mapowania miejsc występowania acetylacji H4K16 wzdłuż genomu na każdym etapie. Znak był obecny przez cały rozwój, ale zmieniał się w sposób zależny od stadium. Szczególnie wyraźny wzrost obserwowano od stadium 8-komórkowego, pokrywający się z momentem, gdy kontrolę przejmują własne geny zarodka. Wiele miejsc, w których gromadził się znak, leżało w pobliżu regionów startowych genów kontrolujących istotne procesy komórkowe, takie jak przetwarzanie RNA, segregacja chromosomów i replikacja DNA — zadania szczególnie intensywne, gdy komórki szybko się dzielą i specjalizują.
Co się dzieje, gdy enzym "piszący" zostaje zablokowany
Aby sprawdzić, czy ten znak jest naprawdę niezbędny, badacze użyli małych cząsteczek hamujących aktywność MOF w wczesnych zarodkach hodowanych in vitro. Zablokowanie MOF drastycznie zmniejszyło odsetek zarodków osiągających stadium blastocysty i spowodowało, że wiele z nich zatrzymywało się w okolicach fazy 8–16 komórek. Gdy zespół przyjrzał się blastocystom, które utworzyły się mimo zahamowania MOF, stwierdził szeroko zakłóconą aktywność genów: tysiące genów były w porównaniu z kontrolami albo nadekspresjonowane, albo wyciszone. Geny, które normalnie nosiły silną acetylację H4K16 wokół swoich rozruszników, miały tendencję do wygaszania, gdy tego znaku zabrakło. Wiele z tych genów należy do szlaków kluczowych dla zarządzania RNA, budowy rybosomów i transportu cząsteczek do jądra i poza nie — podstawowych zadań dla rozwijającego się zarodka.
Otwarcie drzwi genomu dla transkrypcji
Badanie poszło dalej, analizując dostępność DNA i lokalizację głównej machiny czytającej geny, polimerazy RNA II. Regiony wzbogacone w acetylację H4K16 wykazywały bardziej otwartą chromatynę — luźniejszą formę pakowania DNA, która pozwala maszynom molekularnym dotrzeć do genów. Te same regiony gromadziły też więcej polimerazy RNA II. Gdy MOF był zahamowany, miejsca tracące znak stawały się mniej dostępne i wykazywały niższe obsadzenie przez polimerazę RNA II, a pobliskie geny miały zmniejszoną ekspresję. Innymi słowy, acetylacja H4K16 zdaje się działać jak klin, który utrzymuje przełączniki genów fizycznie otwarte, umożliwiając maszynie transkrypcyjnej przyłączenie się i sprawną pracę.
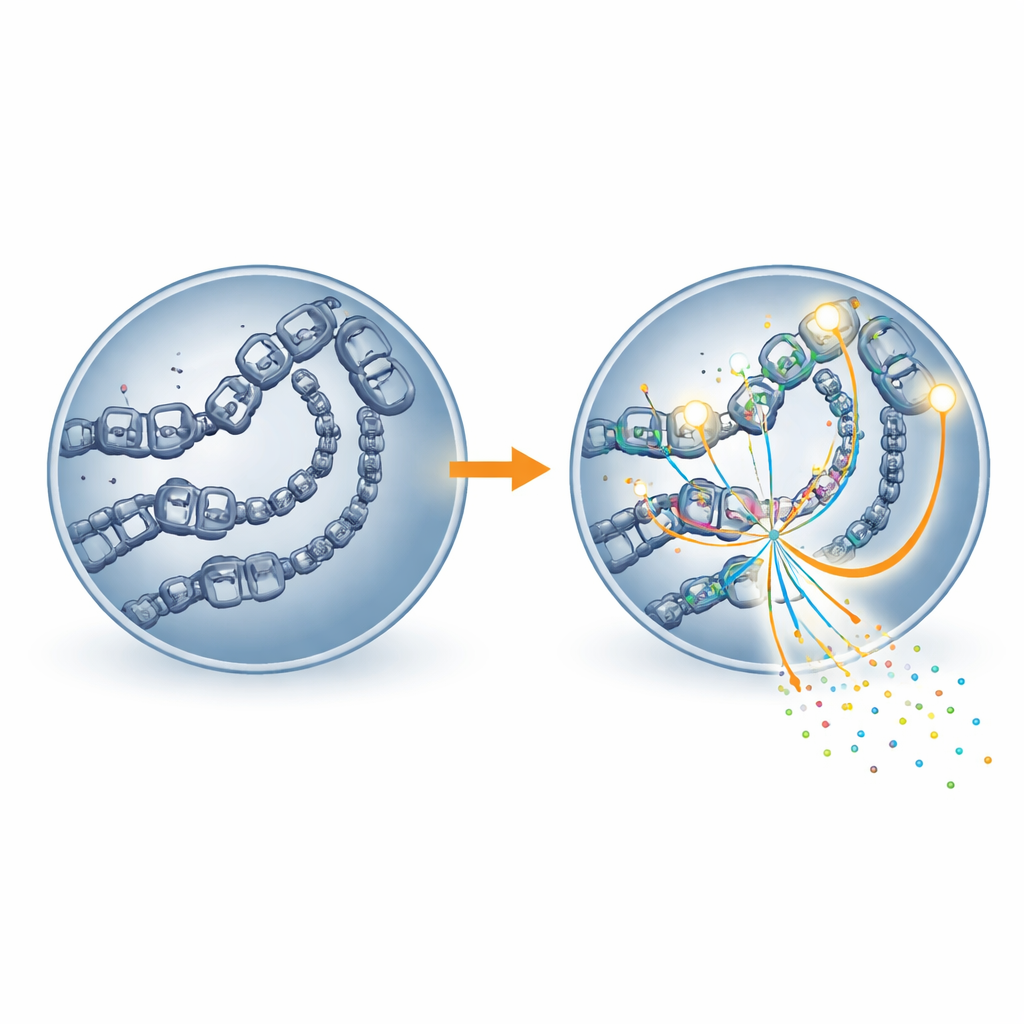
Implikacje dla płodności i technik wspomaganego rozrodu
Łącząc mapy obejmujące cały genom, pomiary aktywności genów i testy funkcjonalne, autorzy dochodzą do wniosku, że acetylacja H4K16 zależna od MOF jest krytycznym punktem kontrolnym epigenetyki w zarodkach owczych. Gdy ten system działa prawidłowo, pomaga kształtować otwarte, dostępne regiony przy kluczowych promotorach genów, przyciąga polimerazę RNA II i wspiera uporządkowane programy genowe niezbędne do zbudowania zdrowej blastocysty. Gdy system jest zaburzony, rozwój załamuje się. Ponieważ zarodki owcze dzielą wiele cech z zarodkami ludzkimi i są powszechnie stosowane jako modele, wyniki sugerują, że ten konkretny znak epigenetyczny — oraz enzym MOF, który go dodaje — mogą stać się użytecznym wskaźnikiem jakości zarodka i potencjalnym celem do poprawy skuteczności technik wspomaganego rozrodu.
Cytowanie: Wang, L., Chen, B., Chen, X. et al. MOF-mediated H4K16ac is critical for blastocyst formation in sheep by shaping promoter accessibility and transcription. Commun Biol 9, 609 (2026). https://doi.org/10.1038/s42003-026-09868-5
Słowa kluczowe: rozwój blastocysty, regulacja epigenetyczna, acetylacja histonów, polimeraza RNA II, techniki wspomaganego rozrodu