Clear Sky Science · ru
MOF-опосредованная H4K16ac критична для формирования бластоцисты у овец, формируя доступность промотеров и транскрипцию
Почему маленькие эмбрионы овец важны для нас
Прежде чем беременность сможет успешно закрепиться, оплодотворённая яйцеклетка должна превратиться в крошечный полый шар клеток, называемый бластоцистой. Этот короткий период, всего через несколько дней после оплодотворения, — момент, когда принимаются первые решения о судьбе клеток и когда многие беременности незаметно прерываются. Для человека и сельскохозяйственных животных умение вырастить здоровые бластоцисты в лаборатории является ключевым для экстракорпорального оплодотворения и разведения животных. В этом исследовании заглядывают внутрь эмбрионов овец, чтобы понять, как специфический химический маркер на белках, упаковывающих ДНК, помогает эмбрионам успешно достигать стадии бластоцисты.
Взгляд поближе на первые дни жизни
У млекопитающих путь от оплодотворённой яйцеклетки до бластоцисты занимает менее недели. В этот период эмбрион сначала должен включить собственный геном, а затем разделить клетки на внутреннюю группу, которая сформирует плод, и наружную оболочку, которая станет плацентой. Эти масштабные изменения направляются не только генами, но и эпигенетическими метками — небольшими химическими флагами на ДНК и её ассоциированных белках, которые подсказывают генам, когда быть включёнными или выключенными. Авторы сосредоточились на одной такой метке, называемой ацетилированием H4K16, которую «пишет» фермент MOF. Предыдущие работы на мышах, дрозофилах и человеческих клетках намекали, что эта метка связана с активными генами и ранним развитием, но её роль в эмбрионах сельскохозяйственных животных оставалась в основном неизученной.
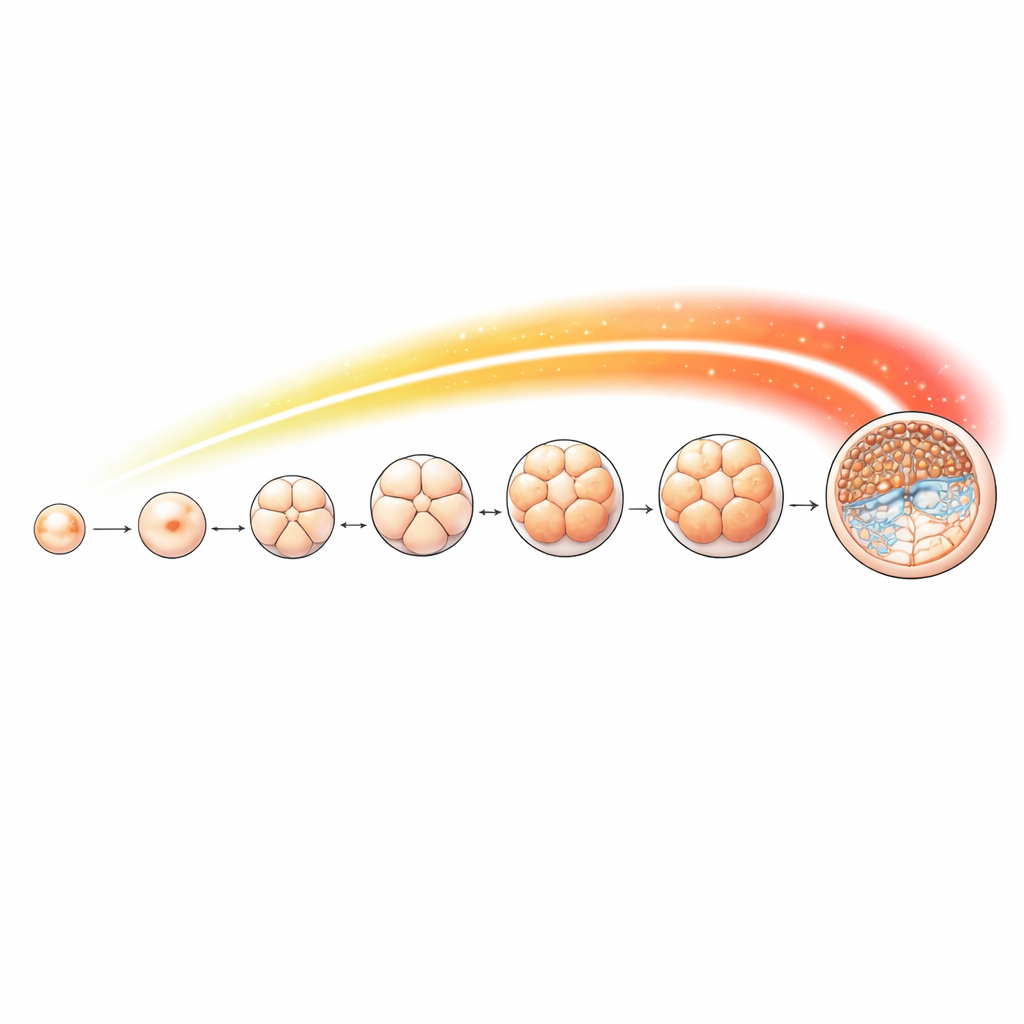
Картирование химического сигнала в ходе раннего развития
Чтобы подробно проследить за этой меткой, команда собрала яйцеклетки и эмбрионы овец на ключевых стадиях — от неоплодотворённых ооцитов до стадий 2, 4, 8 и 16 клеток, морулы и, наконец, бластоцисты. Они использовали чувствительный метод для картирования расположения ацетилирования H4K16 по всему геному на каждом этапе. Метка присутствовала на протяжении всего развития, но менялась в зависимости от стадии. Особенно резкий подъём наблюдался, начиная со стадии 8 клеток, совпадая со временем, когда контроль переходит к собственным генам эмбриона. Многие участки накопления метки находились рядом с областями старта генов, контролирующих важные клеточные процессы, такие как процессинг РНК, сегрегация хромосом и репликация ДНК — задачи, особенно востребованные при быстром делении и специализации клеток.
Что происходит, когда фермент-писатель блокируется
Чтобы проверить, действительно ли эта метка необходима, исследователи использовали малые молекулы для ингибирования активности MOF в ранних эмбрионах, выращиваемых в культуре. Блокировка MOF резко сократила долю эмбрионов, достигших стадии бластоцисты, и многие при этом останавливались на уровне 8–16 клеток. Когда команда проанализировала бластоцисты, сформировавшиеся при ингибировании MOF, они обнаружили повсеместные нарушения в активности генов: тысячи генов были как повышены, так и понижены по сравнению с необработанными контролями. Гены, которые обычно несут сильное ацетилирование H4K16 вокруг своих стартовых регуляторов, как правило, молчали при утрате этой метки. Многие из этих генов входят в пути, критичные для обработки РНК, сборки рибосом и транспорта молекул внутрь и наружу из ядра — базовые функции для растущего эмбриона.
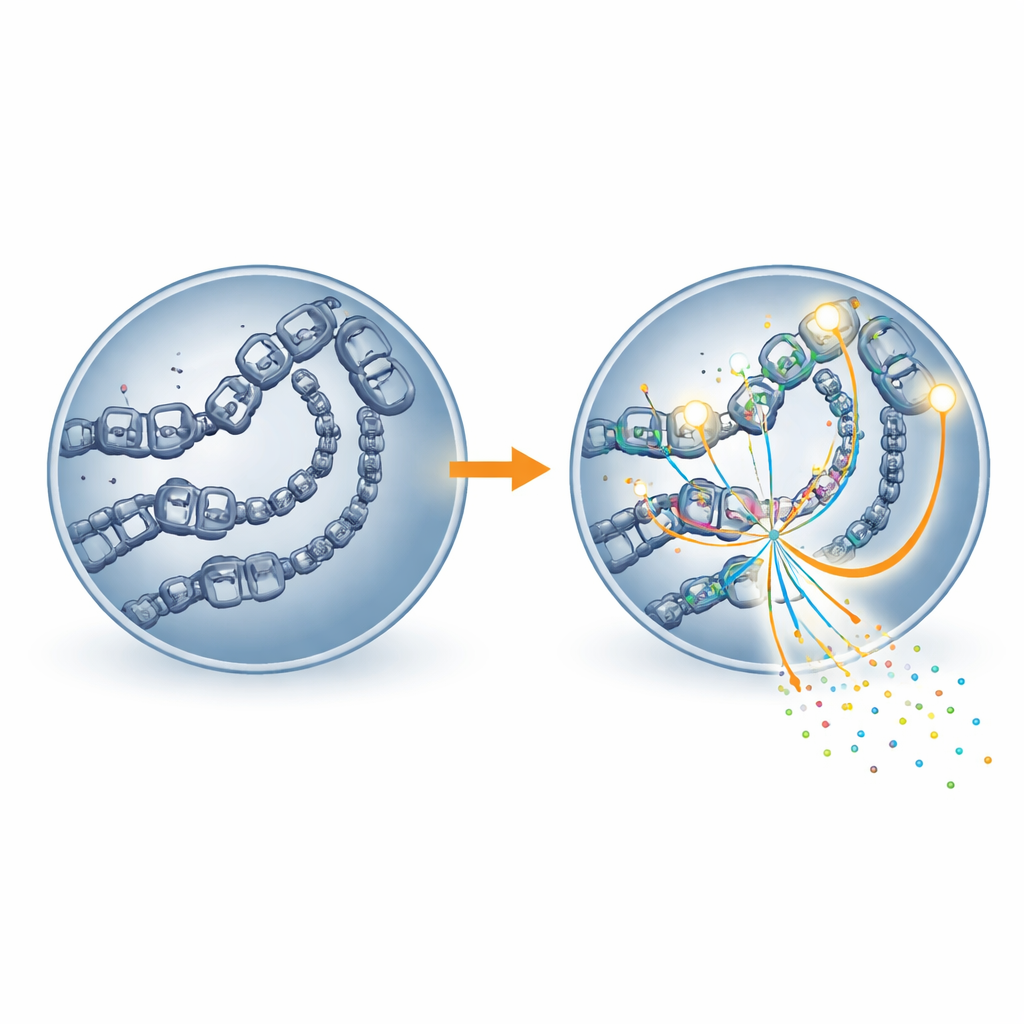
Открывая «двери» генома для транскрипции
Исследование пошло дальше, изучив доступность ДНК и расположение главного аппарата считывания генов клетки — РНК-полимеразы II. Регионы, обогащённые ацетилированием H4K16, демонстрировали более открытую хроматиновую структуру — более рыхлую форму упаковки ДНК, которая позволяет молекулярным машинам добираться до генов. В этих же регионах также наблюдалась повышенная локализация РНК-полимеразы II. При блокировке MOF участки, потерявшие метку, становились менее доступными и показывали уменьшенное присутствие РНК-полимеразы II, а соседние гены экспрессировались в меньшей степени. Иными словами, ацетилирование H4K16, по-видимому, действует как «подставка для двери», удерживая регуляторы генов физически открытыми, чтобы транскрипционный аппарат мог связываться и эффективно работать.
Последствия для фертильности и вспомогательных репродуктивных технологий
Комбинируя карты на уровне всего генома, измерения активности генов и функциональные тесты, авторы приходят к выводу, что MOF-зависимое ацетилирование H4K16 является критическим эпигенетическим контрольным пунктом в эмбрионах овец. Когда эта система работает правильно, она помогает формировать открытые, доступные участки в ключевых промоторах генов, привлекать РНК-полимеразу II и поддерживать упорядоченные генетические программы, необходимые для построения здоровой бластоцисты. При нарушении этой системы развитие даёт сбой. Поскольку эмбрионы овец разделяют многие особенности с человеческими эмбрионами и широко используются как модель, эти результаты указывают на то, что эта конкретная эпигенетическая метка — и фермент MOF, который её наносит — могут стать полезным показателем качества эмбриона и потенциальной мишенью для повышения эффективности вспомогательных репродуктивных технологий.
Цитирование: Wang, L., Chen, B., Chen, X. et al. MOF-mediated H4K16ac is critical for blastocyst formation in sheep by shaping promoter accessibility and transcription. Commun Biol 9, 609 (2026). https://doi.org/10.1038/s42003-026-09868-5
Ключевые слова: развитие бластоцисты, эпигенетическая регуляция, ацетилирование гистонов, РНК-полимераза II, вспомогательное воспроизведение