Clear Sky Science · nl
MOF-gemedieerde H4K16ac is cruciaal voor blastocystvorming bij schaap door promotertoegankelijkheid en transcriptie vorm te geven
Waarom kleine schaapsembrio’s van belang voor ons zijn
Voordat een zwangerschap zich veilig kan vestigen, moet een bevruchte eicel zich omvormen tot een kleine holle bol cellen die een blastocyst wordt genoemd. In dit korte venster, slechts enkele dagen na bevruchting, worden de eerste cellulaire lotsbestemmingen bepaald en stranden veel zwangerschappen stilletjes. Bij mensen en veeteelt is het vermogen om gezonde blastocysten in het laboratorium te laten groeien essentieel voor in-vitrofertilisatie en fokprogramma’s. Deze studie kijkt in schaapsembrio’s om te begrijpen hoe een specifieke chemische markering op DNA-verpakkende eiwitten embryo’s helpt succesvol het blastocyststadium te bereiken.
Een nadere blik op de eerste levensdagen
Bij zoogdieren verloopt de overgang van bevruchte eicel naar blastocyst in minder dan een week. Gedurende deze periode moet het embryo eerst zijn eigen genoom activeren en vervolgens zijn cellen verdelen in een binnenste groep die het embryo vormt en een buitenste laag die de placenta zal worden. Deze ingrijpende veranderingen worden niet alleen gestuurd door genen, maar ook door epigenetische merkers—kleine chemische vlaggetjes op DNA en de daarbij behorende eiwitten die aangeven wanneer genen aan of uit moeten staan. De auteurs richtten zich op één dergelijke merker, H4K16-acetylatie, die wordt aangebracht door een enzym genaamd MOF. Eerder werk in muizen, vliegen en humane cellen suggereerde dat deze merker samenhangt met actieve genen en vroege ontwikkeling, maar de rol ervan in embryo’s van landbouwdieren bleef grotendeels onontgonnen.
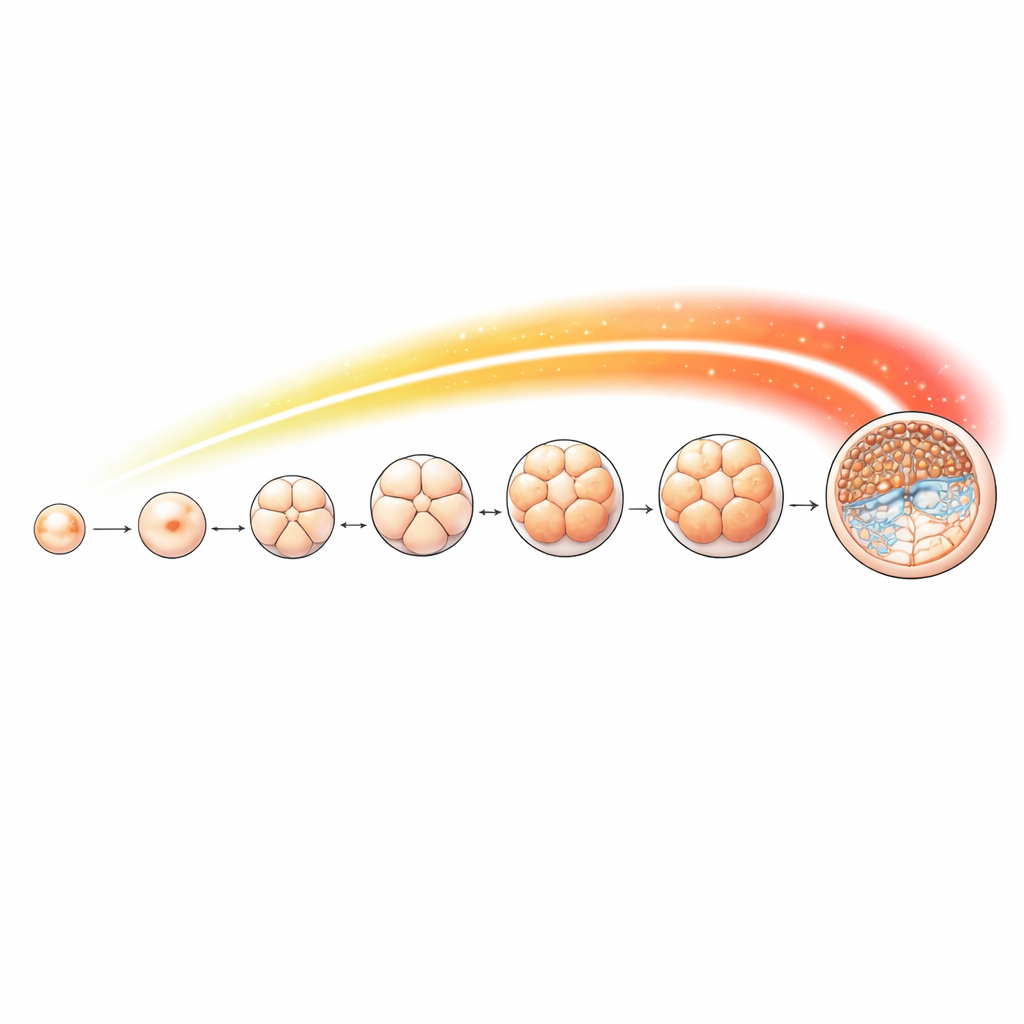
Een chemisch signaal in kaart brengen tijdens vroege ontwikkeling
Om deze merker in detail te volgen, verzamelde het team schaapseicellen en embryo’s in sleutelstadia, van bevruchtingsonafhankelijke oöcyten tot 2-, 4-, 8- en 16-cellige stadia, morula en uiteindelijk blastocyst. Ze gebruikten een gevoelige methode om te bepalen waar H4K16-acetylatie op elk moment langs het genoom aanwezig is. De merker kwam gedurende de ontwikkeling continu voor maar veranderde per stadium. Een opvallende stijging trad op vanaf het 8-cellige stadium, samenvallend met het moment waarop de eigen genen van het embryo de controle overnemen. Veel van de locaties waar de merker zich ophoopte lagen nabij de startregio’s van genen die belangrijke cellulaire processen regelen zoals RNA-verwerking, chromosoomsegregatie en DNA-replicatie—taken die extra zwaar wegen wanneer cellen snel delen en zich specialiseren.
Wat gebeurt er als het schrijvende enzym wordt geblokkeerd
Om te testen of deze merker werkelijk noodzakelijk is, gebruikten de onderzoekers kleine moleculen om de activiteit van MOF te remmen in vroeg ontwikkelende embryo’s in cultuur. Het blokkeren van MOF verminderde het aandeel embryo’s dat het blastocyststadium bereikte drastisch en zorgde ervoor dat veel embryo’s bleven steken rond het 8- tot 16-cellige stadium. Toen het team de blastocysten onderzocht die toch onder MOF-remming waren gevormd, vonden ze een wijdverspreide verstoring van genexpressie: duizenden genen waren hoger of lager geactiveerd vergeleken met onbehandelde controles. Genen die normaal sterke H4K16-acetylatie rond hun startschakelaars dragen, vielen vaak stil wanneer die merker verloren ging. Veel van deze genen behoren tot routes die cruciaal zijn voor het beheer van RNA, de bouw van ribosomen en het transport van moleculen in en uit de kern—kernfuncties voor een groeiend embryo.
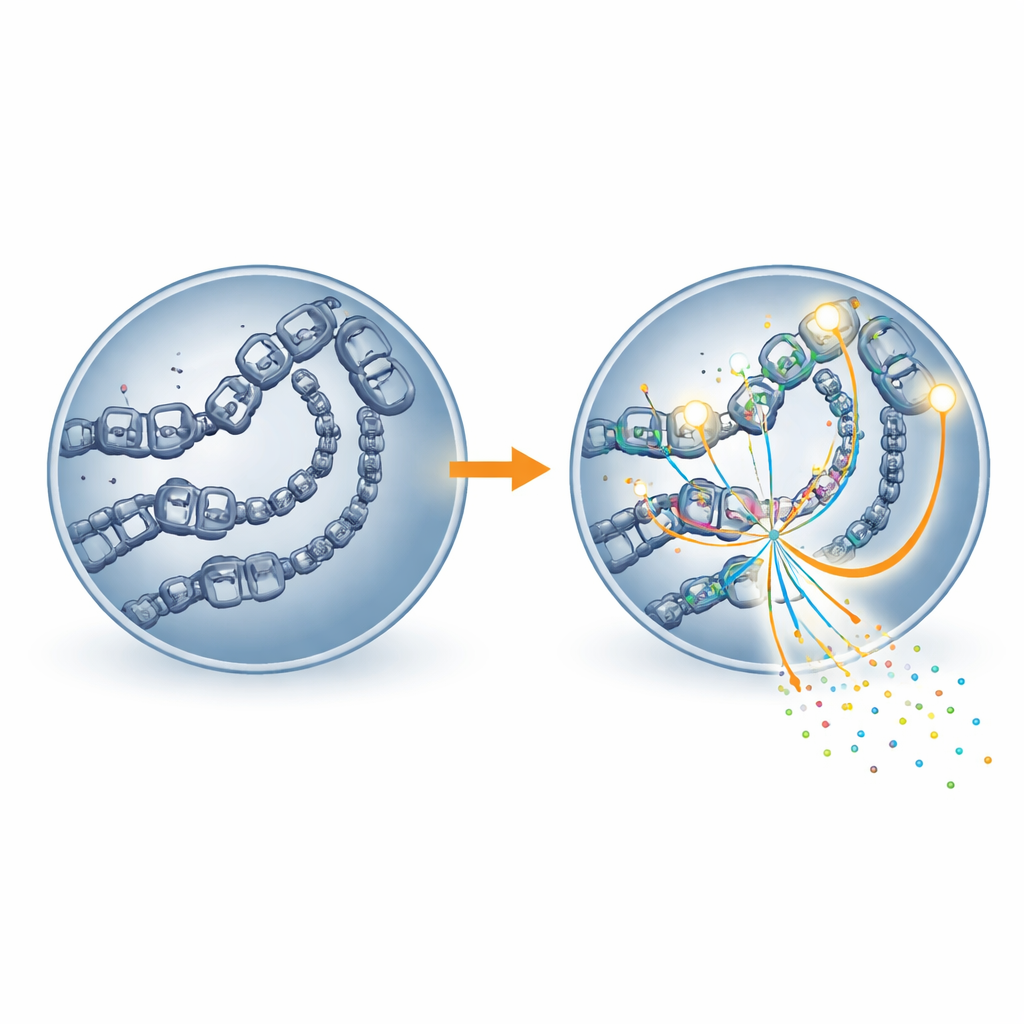
De deuren van het genoom openen voor transcriptie
De studie ging verder door te kijken naar hoe toegankelijk het DNA was en waar de belangrijkste genlezende machine van de cel, RNA-polymerase II, zich bevond. Regio’s die verrijkt waren in H4K16-acetylatie vertoonden meer open chromatine—de lossere vorm van DNA‑verpakking die moleculaire machines toegang tot genen geeft. Dezezelfde regio’s huisvestten ook meer RNA-polymerase II. Wanneer MOF werd geblokkeerd, werden locaties die de merker verloren minder toegankelijk en vertoonden ze verminderde bezetting door RNA‑polymerase II, en de nabije genen werden op lagere niveaus tot expressie gebracht. Met andere woorden lijkt H4K16-acetylatie te werken als een deurdop die genstartschakelaars fysiek openhoudt zodat de transcriptiemachines kunnen binden en efficiënt werken.
Gevolgen voor vruchtbaarheid en geassisteerde reproductie
Door genoomwijde kaarten, metingen van genactiviteit en functionele tests te combineren, concluderen de auteurs dat MOF‑afhankelijke H4K16-acetylatie een kritisch epigenetisch controlepunt is in schaapsembrio’s. Wanneer dit systeem goed functioneert, helpt het open, toegankelijke regio’s bij sleutelpromoters te vormen, trekt het RNA‑polymerase II aan en ondersteunt het de ordelijke genprogramma’s die nodig zijn om een gezonde blastocyst te bouwen. Wanneer het systeem verstoord is, stokt de ontwikkeling. Omdat schaapsembrio’s veel kenmerken delen met humane embryo’s en vaak als model worden gebruikt, suggereren de bevindingen dat deze specifieke epigenetische merker—en het MOF-enzym dat hem aanbrengt—een nuttige indicator van embryo‑kwaliteit kunnen worden en een potentieel doelwit voor het verbeteren van het succes van geassisteerde voortplantingstechnologieën.
Bronvermelding: Wang, L., Chen, B., Chen, X. et al. MOF-mediated H4K16ac is critical for blastocyst formation in sheep by shaping promoter accessibility and transcription. Commun Biol 9, 609 (2026). https://doi.org/10.1038/s42003-026-09868-5
Trefwoorden: blastocystontwikkeling, epigenetische regulatie, histonacetylatie, RNA-polymerase II, geassisteerde reproductie