Clear Sky Science · es
La acetilación H4K16 mediada por MOF es crítica para la formación del blastocisto en ovejas al configurar la accesibilidad del promotor y la transcripción
Por qué nos importan los diminutos embriones de oveja
Antes de que un embarazo pueda establecerse con seguridad, un óvulo fertilizado debe transformarse en una pequeña esfera hueca de células llamada blastocisto. Esta ventana breve, solo días después de la fertilización, es cuando se deciden los primeros destinos celulares y cuando muchos embarazos fallan silenciosamente. En humanos y animales de producción, poder desarrollar blastocistos sanos en el laboratorio es fundamental para la fertilización in vitro y la reproducción animal. Este estudio examina embriones de oveja para entender cómo una etiqueta química específica en las proteínas que empaquetan el ADN ayuda a que los embriones alcancen con éxito la etapa de blastocisto.
Una mirada más cercana a los primeros días de la vida
En los mamíferos, el trayecto desde el óvulo fertilizado hasta el blastocisto ocurre en menos de una semana. Durante este periodo, el embrión debe primero activar su propio genoma y luego clasificar sus células en un cúmulo interno que formará el feto y una capa externa que se convertirá en la placenta. Estos cambios de gran alcance están guiados no solo por los genes, sino también por marcas epigenéticas: pequeñas señales químicas en el ADN y sus proteínas asociadas que indican cuándo activar o silenciar genes. Los autores se centraron en una de estas marcas, llamada acetilación en H4K16, que es añadida por una enzima conocida como MOF. Trabajos previos en ratones, moscas y células humanas sugerían que esta marca se asocia con genes activos y con el desarrollo temprano, pero su papel en embriones de animales de producción seguía siendo en gran parte inexplorado.
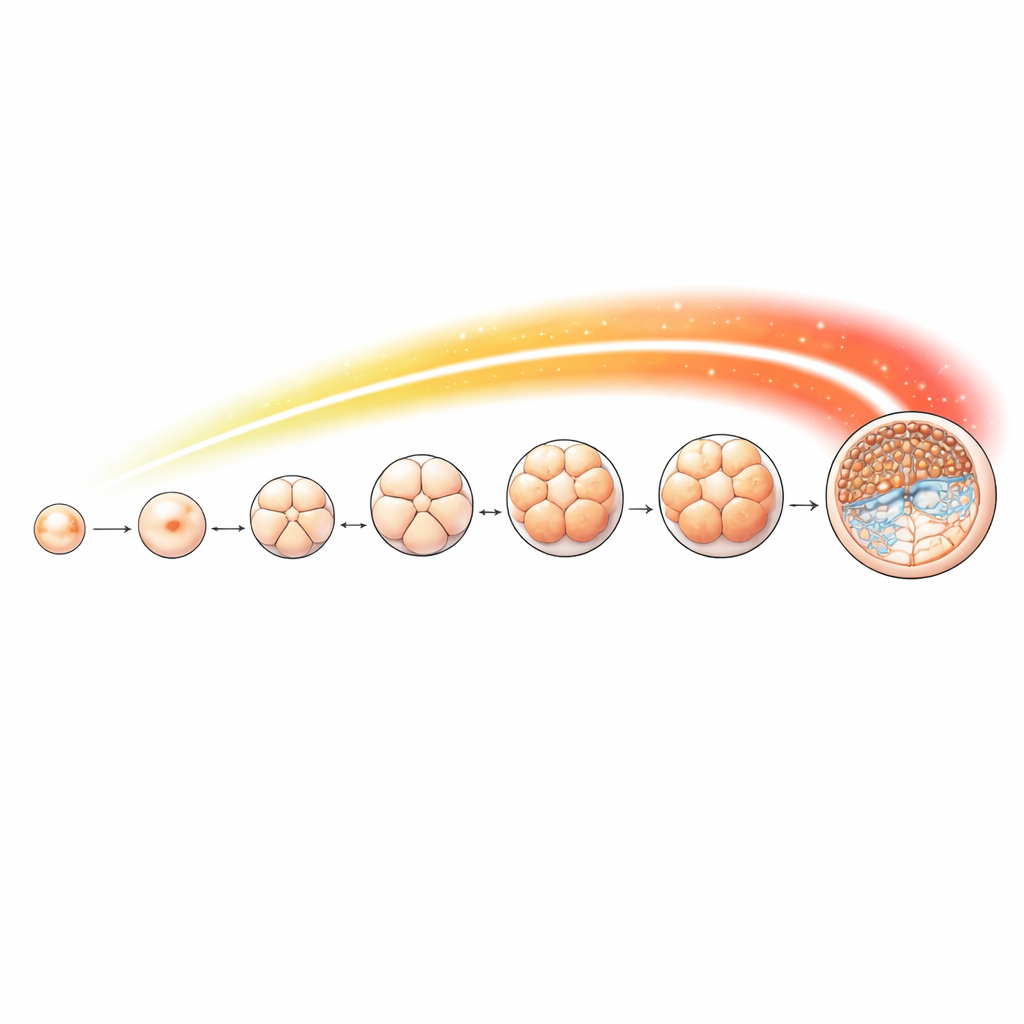
Cartografiar una señal química a lo largo del desarrollo temprano
Para rastrear esta marca en detalle, el equipo recolectó óvulos y embriones de oveja en etapas clave, desde ovocitos no fertilizados hasta fases de 2, 4, 8 y 16 células, mórula y finalmente blastocisto. Emplearon un método sensible para mapear dónde se localiza la acetilación H4K16 a lo largo del genoma en cada paso. La marca estuvo presente durante todo el desarrollo, pero varió según la etapa. Un aumento particularmente marcado ocurrió a partir de la etapa de 8 células, coincidiendo con el momento en que los genes del propio embrión toman el control. Muchos de los sitios donde la marca se acumuló se encontraban cerca de las regiones de inicio de genes que controlan procesos celulares importantes como el procesamiento del ARN, la segregación cromosómica y la replicación del ADN: tareas especialmente exigentes cuando las células se dividen rápidamente y se especializan.
Qué ocurre cuando se bloquea la enzima que escribe la marca
Para probar si esta marca es realmente necesaria, los investigadores usaron pequeñas moléculas para inhibir la actividad de MOF en embriones tempranos cultivados in vitro. Bloquear MOF redujo drásticamente la fracción de embriones que alcanzaron la etapa de blastocisto y provocó que muchos se estancaran alrededor de las fases de 8 a 16 células. Cuando el equipo examinó los blastocistos que se formaron bajo inhibición de MOF, halló una alteración generalizada de la actividad génica: miles de genes se expresaron a niveles más altos o más bajos en comparación con los controles no tratados. Los genes que normalmente presentan una fuerte acetilación H4K16 alrededor de sus regiones de inicio tendieron a silenciarse cuando se perdió esa marca. Muchos de estos genes pertenecen a vías cruciales para gestionar el ARN, ensamblar ribosomas y transportar moléculas dentro y fuera del núcleo: tareas centrales para un embrión en crecimiento.
Abrir las puertas del genoma a la transcripción
El estudio fue más allá al analizar cuán accesible estaba el ADN y dónde se situaba la principal máquina de lectura génica de la célula, la ARN polimerasa II. Las regiones enriquecidas en acetilación H4K16 mostraron una cromatina más abierta—la forma más laxa del empaquetamiento del ADN que permite a las máquinas moleculares alcanzar los genes. Estas mismas regiones también alojaban mayor cantidad de ARN polimerasa II. Cuando se bloqueó MOF, los sitios que perdieron la marca se volvieron menos accesibles y mostraron una ocupación reducida por ARN polimerasa II, y los genes cercanos se expresaron a niveles más bajos. En otras palabras, la acetilación H4K16 parece actuar como un tope que mantiene físicamente abiertas las palancas génicas para que la maquinaria de transcripción pueda unirse y funcionar con eficiencia.
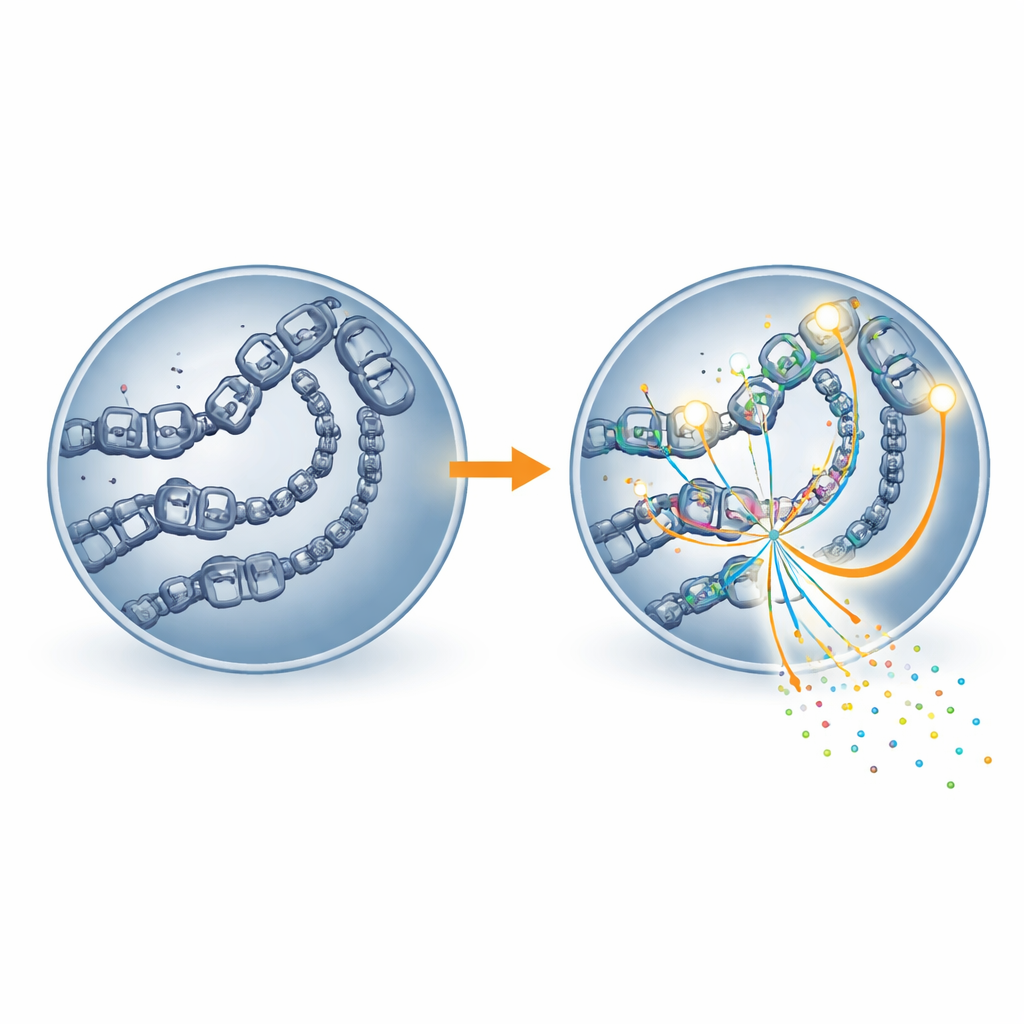
Implicaciones para la fertilidad y la reproducción asistida
Al combinar mapas genómicos, mediciones de actividad génica y pruebas funcionales, los autores concluyen que la acetilación H4K16 dependiente de MOF es un punto de control epigenético crítico en embriones de oveja. Cuando este sistema funciona correctamente, ayuda a configurar regiones abiertas y accesibles en promotores génicos clave, atrae a la ARN polimerasa II y sostiene los programas génicos ordenados necesarios para construir un blastocisto sano. Cuando el sistema se ve alterado, el desarrollo falla. Dado que los embriones de oveja comparten muchas características con los embriones humanos y se usan ampliamente como modelos, los hallazgos sugieren que esta marca epigenética concreta—y la enzima MOF que la escribe—podrían convertirse en un indicador útil de la calidad embrionaria y en un posible objetivo para mejorar el éxito de las tecnologías de reproducción asistida.
Cita: Wang, L., Chen, B., Chen, X. et al. MOF-mediated H4K16ac is critical for blastocyst formation in sheep by shaping promoter accessibility and transcription. Commun Biol 9, 609 (2026). https://doi.org/10.1038/s42003-026-09868-5
Palabras clave: desarrollo del blastocisto, regulación epigenética, acetilación de histonas, ARN polimerasa II, reproducción asistida