Clear Sky Science · de
MOF-vermittelte H4K16ac ist entscheidend für die Blastozystenbildung bei Schafen, indem sie Promoterzugänglichkeit und Transkription formt
Warum winzige Schaf-Embryonen für uns wichtig sind
Bevor eine Schwangerschaft sicher entstehen kann, muss sich eine befruchtete Eizelle in eine winzige, hohle Zellkugel verwandeln, die Blastozyste genannt wird. Dieses kurze Zeitfenster, nur wenige Tage nach der Befruchtung, ist die Phase, in der die ersten Zellschicksale festgelegt werden und in der viele Schwangerschaften still scheitern. Bei Menschen und Nutztieren ist die Fähigkeit, gesunde Blastozysten im Labor zu erzeugen, zentral für In-vitro-Fertilisation und Tierzucht. Diese Studie schaut in Schaf-Embryonen hinein, um zu verstehen, wie ein spezielles chemisches Markierungssignal auf DNA-verpackenden Proteinen den Embryonen hilft, erfolgreich das Blastozystenstadium zu erreichen.
Ein genauerer Blick auf die ersten Lebenstage
Bei Säugetieren vollzieht sich der Weg von der befruchteten Eizelle zur Blastozyste in weniger als einer Woche. In dieser Zeit muss der Embryo zunächst sein eigenes Genom anschalten und dann seine Zellen in eine innere Gruppe, die den Fötus bildet, und eine äußere Hülle, die zur Plazenta wird, aufteilen. Diese weitreichenden Veränderungen werden nicht nur von Genen gesteuert, sondern auch von epigenetischen Markern—kleinen chemischen Signalen auf der DNA und ihren assoziierten Proteinen, die Genen sagen, wann sie an- oder ausgeschaltet werden sollen. Die Autoren konzentrierten sich auf einen solchen Marker, die Acetylierung an H4K16, die von einem Enzym namens MOF angebracht wird. Frühere Arbeiten an Mäusen, Fliegen und menschlichen Zellen deuteten darauf hin, dass dieses Signal mit aktiven Genen und frühem Entwicklungsprozess verknüpft ist, doch seine Rolle in Embryonen von Nutztieren war bisher weitgehend ungeklärt.
Eine chemische Spur durch die frühe Entwicklung kartieren
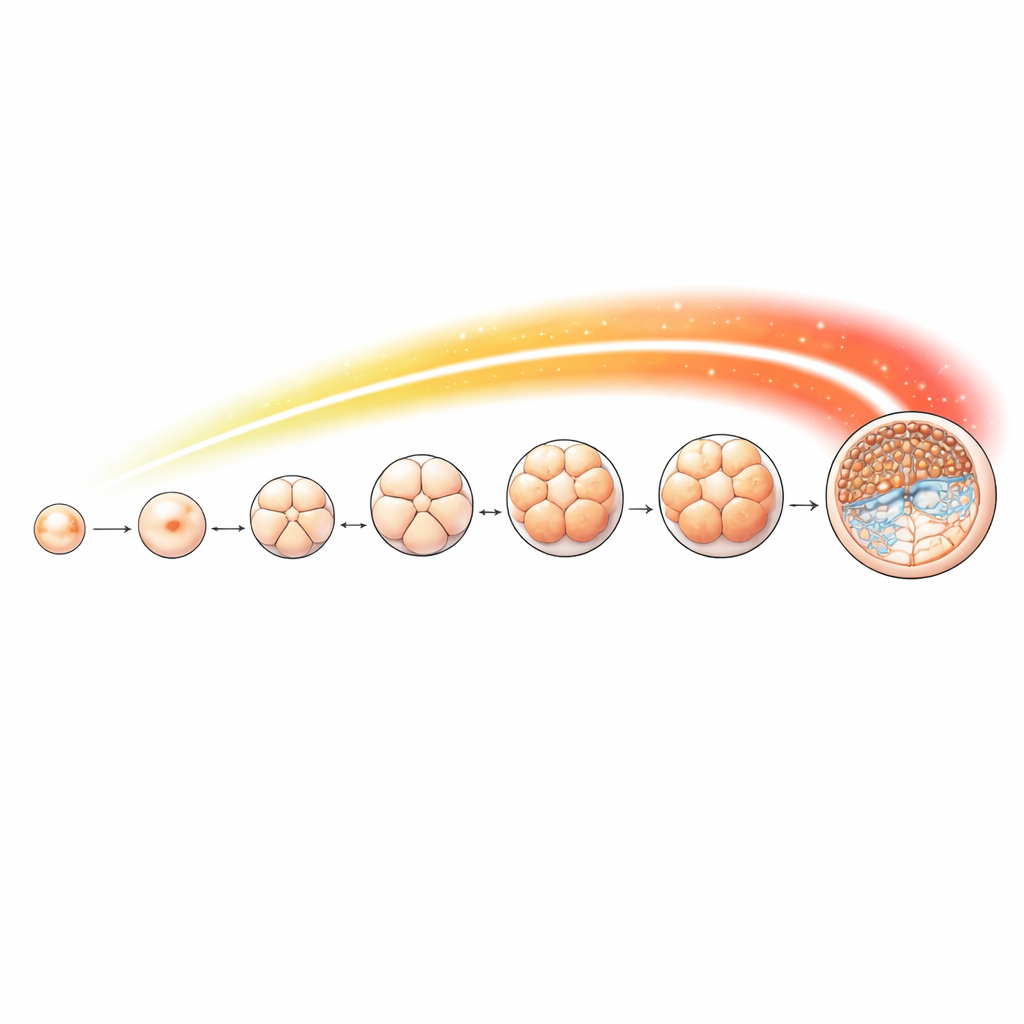
Um dieses Signal im Detail zu verfolgen, sammelte das Team Schaf-Eizellen und Embryonen zu Schlüsselschritten, von unbefruchteten Oozyten über 2-, 4-, 8- und 16-Zell-Stadien, Morula und schließlich Blastozyste. Sie nutzten eine empfindliche Methode, um an jedem Schritt nachzuvollziehen, wo H4K16-Acetylierung im Genom vorkommt. Der Marker war während der gesamten Entwicklung vorhanden, änderte sich jedoch stadienabhängig. Ein besonders starker Anstieg zeigte sich ab dem 8-Zell-Stadium, zugleich mit dem Zeitpunkt, an dem die Gene des Embryos selbst die Kontrolle übernehmen. Viele der Stellen, an denen sich das Signal anhäufte, lagen nahe den Genstartregionen, die wichtige zelluläre Prozesse wie RNA-Verarbeitung, Chromosomen-Separation und DNA-Replikation steuern—Aufgaben, die besonders anspruchsvoll sind, wenn Zellen sich schnell teilen und spezialisieren.
Was passiert, wenn das "Schreib"-Enzym blockiert wird
Um zu prüfen, ob dieser Marker wirklich notwendig ist, setzten die Forscher kleine Moleküle ein, um die Aktivität von MOF in frühen, im Kultur gezüchteten Embryonen zu hemmen. Die Blockade von MOF verringerte drastisch den Anteil der Embryonen, die das Blastozystenstadium erreichten, und viele blieben um das 8- bis 16-Zell-Stadium stehen. Als das Team die unter MOF-Hemmung entstandenen Blastozysten untersuchte, fanden sie weitreichende Störungen der Genaktivität: Tausende Gene waren im Vergleich zu unbehandelten Kontrollen hoch- oder herunterreguliert. Gene, die normalerweise starke H4K16-Acetylierung an ihren Startschaltern tragen, schalteten tendenziell ab, wenn dieses Mark verloren ging. Viele dieser Gene gehören zu Wegen, die für RNA-Management, Ribosomenaufbau und den Molekültransport in und aus dem Zellkern entscheidend sind—Kernaufgaben für einen wachsenden Embryo.
Die Türen des Genoms für die Transkription öffnen
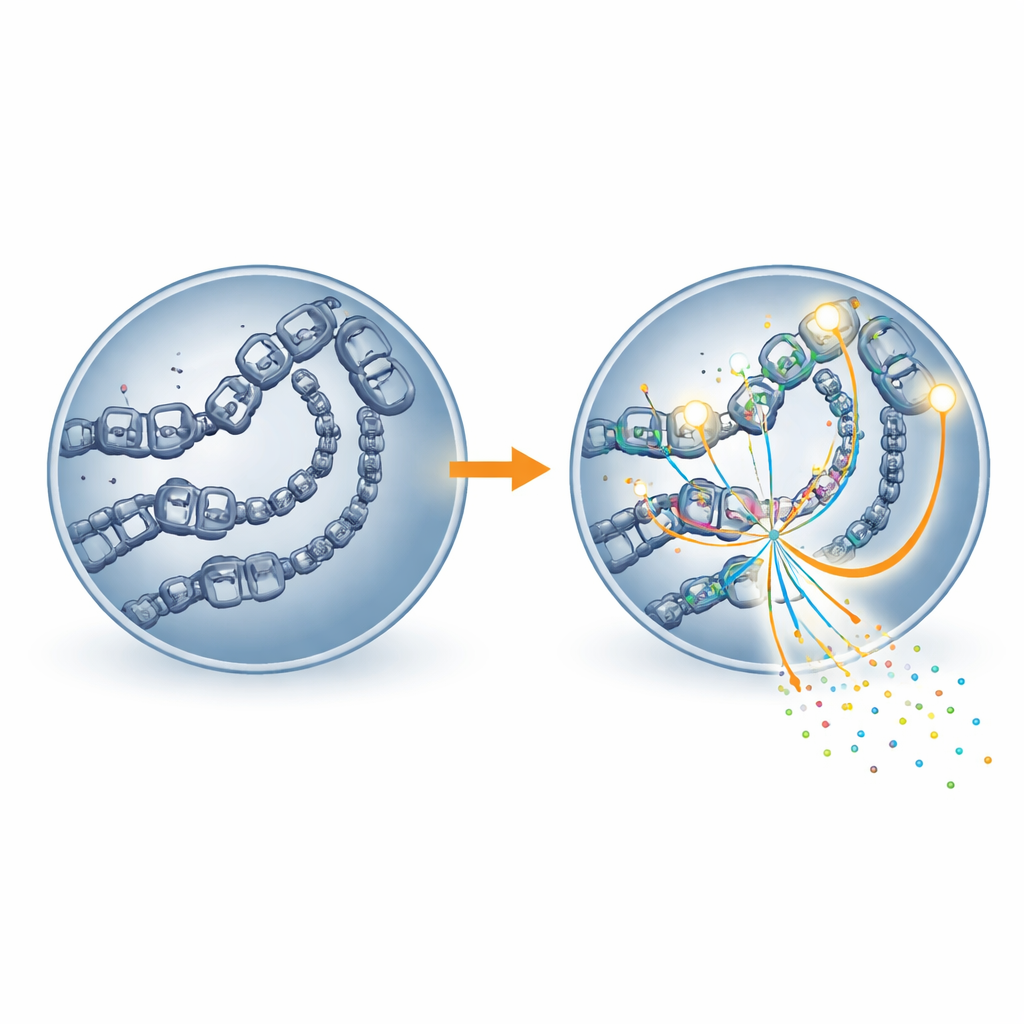
Die Studie ging weiter, indem sie untersuchte, wie zugänglich die DNA war und wo die Haupt-Genablesemaschine der Zelle, die RNA-Polymerase II, lokalisiert war. Regionen, die reich an H4K16-Acetylierung waren, zeigten offeneres Chromatin—die lockerere Form der DNA-Verpackung, die es molekularen Maschinen erlaubt, Gene zu erreichen. Dieselben Regionen beherbergten außerdem mehr RNA-Polymerase II. Wenn MOF blockiert wurde, wurden Stellen, die das Mark verloren, weniger zugänglich und zeigten eine verringerte Besetzung durch RNA-Polymerase II; die benachbarten Gene wurden schwächer exprimiert. Mit anderen Worten: H4K16-Acetylierung scheint wie ein Türkeil zu wirken, der Gen-Schalter physisch offenhält, damit die Transkriptionsmaschinerie binden und effizient arbeiten kann.
Folgen für Fruchtbarkeit und assistierte Reproduktion
Durch die Kombination von genomweiten Karten, Messungen der Genaktivität und funktionellen Tests kommen die Autoren zu dem Schluss, dass MOF-abhängige H4K16-Acetylierung ein kritischer epigenetischer Kontrollpunkt in Schaf-Embryonen ist. Wenn dieses System richtig funktioniert, trägt es dazu bei, offene, zugängliche Regionen an wichtigen Genpromotoren zu formen, RNA-Polymerase II anzuziehen und die geordneten Genprogramme zu unterstützen, die notwendig sind, um eine gesunde Blastozyste aufzubauen. Wird das System gestört, stockt die Entwicklung. Da Schaf-Embryonen viele Gemeinsamkeiten mit menschlichen Embryonen aufweisen und häufig als Modell verwendet werden, legen die Ergebnisse nahe, dass dieses spezifische epigenetische Zeichen—und das MOF-Enzym, das es setzt—zu einem nützlichen Indikator für Embryonenqualität und einem potenziellen Ziel zur Verbesserung des Erfolgs assistierter Reproduktionstechnologien werden könnten.
Zitation: Wang, L., Chen, B., Chen, X. et al. MOF-mediated H4K16ac is critical for blastocyst formation in sheep by shaping promoter accessibility and transcription. Commun Biol 9, 609 (2026). https://doi.org/10.1038/s42003-026-09868-5
Schlüsselwörter: Blastozystenentwicklung, epigenetische Regulation, Histonacetylierung, RNA-Polymerase II, assistierte Fortpflanzung