Clear Sky Science · fr
L’acétylation H4K16 médiée par MOF est essentielle à la formation du blastocyste chez le mouton en modelant l’accessibilité des promoteurs et la transcription
Pourquoi de tout petits embryons de mouton nous intéressent
Avant qu’une grossesse puisse s’installer en toute sécurité, un ovule fécondé doit se transformer en une petite sphère creuse de cellules appelée blastocyste. Cette brève fenêtre, quelques jours seulement après la fécondation, est le moment où se décident les premiers destins cellulaires et où de nombreuses grossesses échouent silencieusement. Chez l’humain comme chez les animaux d’élevage, pouvoir cultiver des blastocystes sains en laboratoire est au cœur de la fécondation in vitro et du croisement assisté. Cette étude examine des embryons de mouton pour comprendre comment un marquage chimique spécifique des protéines qui emballent l’ADN aide les embryons à atteindre avec succès le stade de blastocyste.
Un regard rapproché sur les premiers jours de la vie
Chez les mammifères, le trajet de l’ovule fécondé au blastocyste se déroule en moins d’une semaine. Pendant cette période, l’embryon doit d’abord activer son propre génome puis répartir ses cellules en une masse interne qui formera le fœtus et en une enveloppe externe qui deviendra le placenta. Ces changements majeurs sont guidés non seulement par les gènes, mais aussi par des marques épigénétiques — de petits drapeaux chimiques sur l’ADN et ses protéines associées qui indiquent quand les gènes doivent s’allumer ou s’éteindre. Les auteurs se sont concentrés sur l’une de ces marques, l’acétylation de H4K16, déposée par une enzyme appelée MOF. Des travaux antérieurs chez la souris, la mouche et des cellules humaines suggéraient que cette marque est liée aux gènes actifs et au développement précoce, mais son rôle dans les embryons d’animaux d’élevage restait largement inexploré.
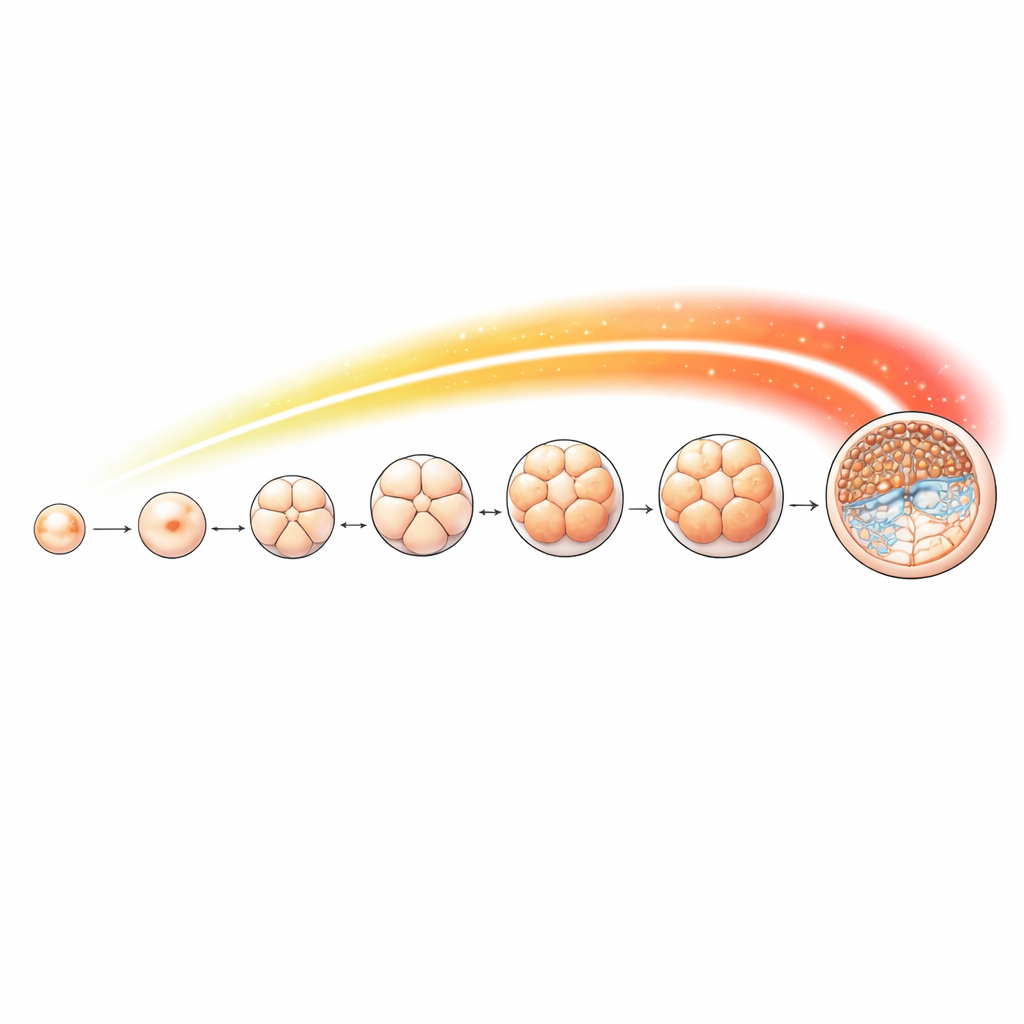
Cartographier un signal chimique pendant le développement précoce
Pour suivre cette marque en détail, l’équipe a prélevé des ovocytes et des embryons de mouton à des stades clés, depuis des ovocytes non fécondés jusqu’aux stades 2, 4, 8 et 16 cellules, la morula, puis le blastocyste. Ils ont utilisé une méthode sensible pour localiser l’acétylation H4K16 le long du génome à chaque étape. La marque était présente tout au long du développement mais variait selon les stades. Une augmentation particulièrement nette est survenue à partir du stade 8 cellules, coïncidant avec le moment où les gènes de l’embryon prennent le contrôle. De nombreux sites d’accumulation de la marque se situaient près des régions de démarrage des gènes qui régulent des processus cellulaires importants comme le traitement de l’ARN, la ségrégation des chromosomes et la réplication de l’ADN — des tâches particulièrement exigeantes quand les cellules se divisent rapidement et se spécialisent.
Que se passe-t-il lorsque l’enzyme rédactrice est bloquée
Pour tester si cette marque est réellement nécessaire, les chercheurs ont utilisé de petites molécules pour inhiber l’activité de MOF dans des embryons en culture. Le blocage de MOF a fortement diminué la fraction d’embryons parvenant au stade blastocyste et a provoqué l’arrêt de nombreux embryons autour des phases 8 à 16 cellules. Lorsqu’ils ont examiné les blastocystes qui se formaient malgré l’inhibition de MOF, ils ont observé une perturbation généralisée de l’activité génique : des milliers de gènes étaient surexprimés ou sous-exprimés par rapport aux témoins non traités. Les gènes qui présentent normalement une forte acétylation H4K16 autour de leurs régions de départ avaient tendance à s’éteindre quand cette marque disparaissait. Beaucoup de ces gènes appartiennent à des voies essentielles à la gestion de l’ARN, à la construction des ribosomes et au transport des molécules vers l’intérieur et l’extérieur du noyau — des fonctions centrales pour un embryon en croissance.
Ouvrir les portes du génome à la transcription
L’étude a poussé plus loin l’analyse en examinant l’accessibilité de l’ADN et la localisation de la principale machinerie de lecture des gènes, l’ARN polymérase II. Les régions enrichies en acétylation H4K16 présentaient une chromatine plus ouverte — une forme d’emballage de l’ADN plus lâche qui permet aux complexes moléculaires d’accéder aux gènes. Ces mêmes régions accueillaient également plus d’ARN polymérase II. Lorsque MOF était inhibé, les sites ayant perdu la marque devenaient moins accessibles et montraient une moindre occupation par l’ARN polymérase II, et les gènes voisins étaient exprimés à des niveaux plus faibles. En d’autres termes, l’acétylation H4K16 semble jouer le rôle d’une cale qui maintient physiquement ouverts les interrupteurs géniques pour que la machinerie de transcription puisse se fixer et fonctionner efficacement.
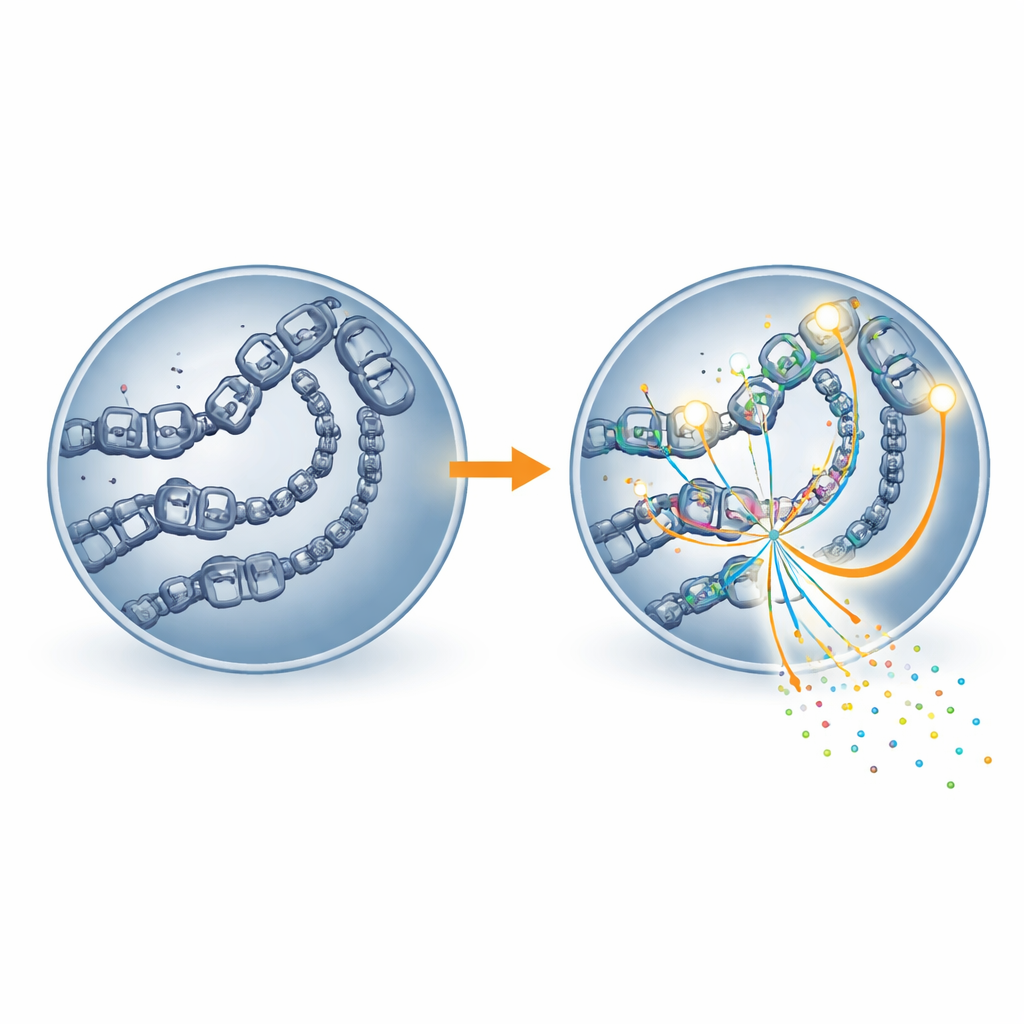
Conséquences pour la fertilité et la reproduction assistée
En combinant des cartes à l’échelle du génome, des mesures d’activité génique et des tests fonctionnels, les auteurs concluent que l’acétylation H4K16 dépendante de MOF constitue un point de contrôle épigénétique critique chez l’embryon de mouton. Lorsque ce système fonctionne correctement, il contribue à façonner des régions ouvertes et accessibles au niveau des promoteurs clés, attire l’ARN polymérase II et soutient les programmes géniques ordonnés nécessaires à la formation d’un blastocyste sain. Lorsque le système est perturbé, le développement se grippe. Étant donné que les embryons de mouton partagent de nombreuses caractéristiques avec les embryons humains et sont couramment utilisés comme modèles, ces résultats suggèrent que cette marque épigénétique — et l’enzyme MOF qui la dépose — pourrait devenir un indicateur utile de la qualité embryonnaire et une cible potentielle pour améliorer le succès des techniques de reproduction assistée.
Citation: Wang, L., Chen, B., Chen, X. et al. MOF-mediated H4K16ac is critical for blastocyst formation in sheep by shaping promoter accessibility and transcription. Commun Biol 9, 609 (2026). https://doi.org/10.1038/s42003-026-09868-5
Mots-clés: développement du blastocyste, régulation épigénétique, acétylation des histones, ARN polymérase II, reproduction assistée