Clear Sky Science · sv
METTL3-medierad åldrande hos fibroblastliknande synoviocyter främjar progress av artros i käkleden
Varför slitage i käkleden spelar roll
Klickande, smärta eller stelhet i käken kan vara mer än en irritation; för många är det tecken på artros i käkleden (temporomandibular joint), en smärtsam degenerativ sjukdom i käkleden. Denna studie gräver under ledens yta för att ställa en enkel men viktig fråga: varför börjar den stötdämpande brosken i käken brytas ner, och kan en avisst förlopp av en viss typ av cellåldrande skydda den? Forskarna avslöjar en molekylär kedja av händelser inne i ledens beklädnads‑celler som kan öppna dörren för mer riktade och mindre invasiva behandlingar än dagens läkemedel eller kirurgi.
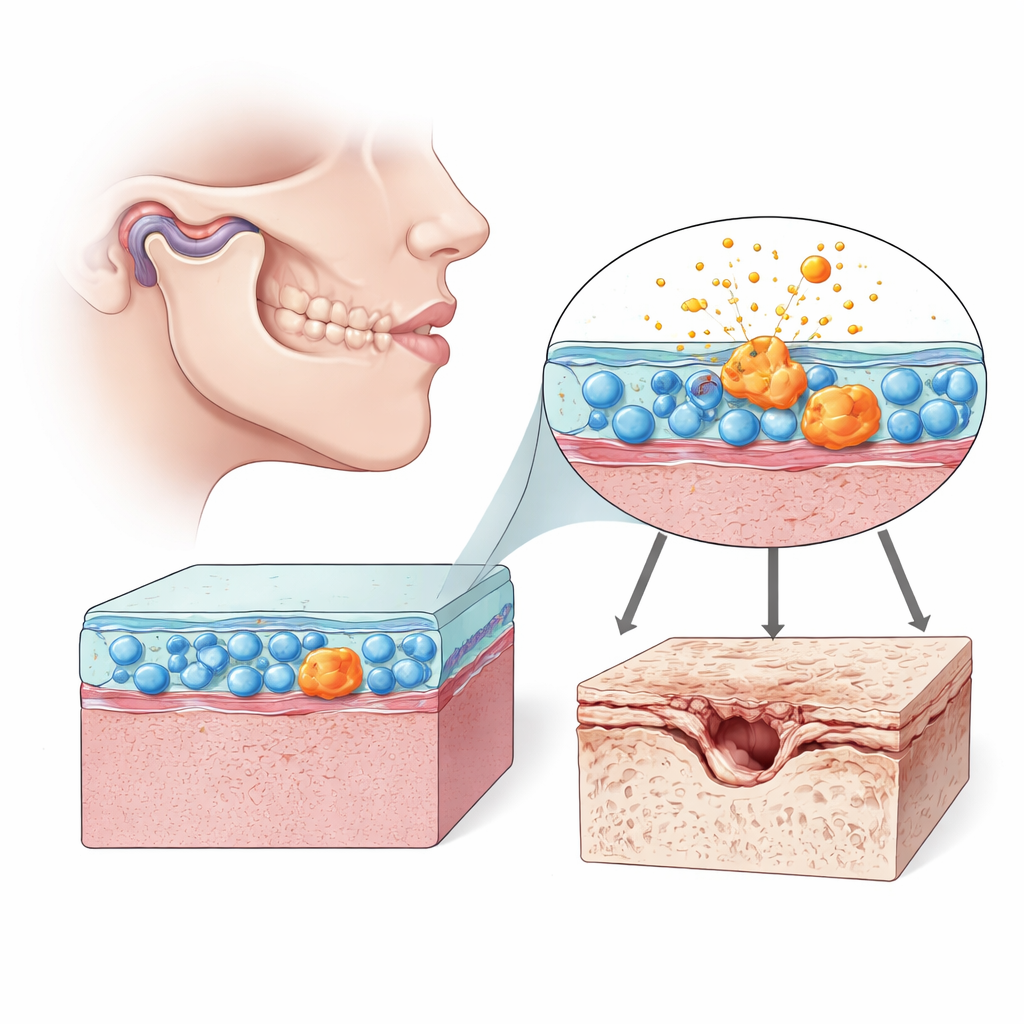
Celler som tyst formar ledhälsa
Inne i varje rörlig led finns en mjuk beklädnad kallad synovium, fylld med fibroblastliknande synoviocyter—celler som hjälper till att smörja och försörja leden. I käkleden (TMJ) hjälper dessa celler till att hålla den lilla disken och broskytenorna glidande när vi tuggar och pratar. Men när dessa synovialceller går fel kan de översvämma leden med inflammatoriska molekyler och enzymer som bryter ner brosk. Författarna fokuserade på hur dessa celler beter sig vid TMJ‑artros hos råttor och i humana cellkulturer, med särskild uppmärksamhet på tecken på cellulärt åldrande, eller senescens, och mitochondriernas hälsa.
När ledbeklädnadens celler åldras i förtid
Genom att använda en kemikalie för att framkalla TMJ‑artros hos råttor bekräftade gruppen klassiska drag av sjukdomen: ojämnhet i benet under brosket, uttunnat brosk, ökad smärtkänslighet och högre nivåer av inflammatoriska budbärare. I ledbeklädnaden visade många synoviocyter markörer för senescens—celler som slutat dela sig men förblir metaboliskt aktiva och starkt inflammatoriska. Dessa senescenta celler hade slöa interna städsystem och skadade mitokondrier. När forskarna isolerade dessa ledbeklädnadsceller och odlade dem tillsammans med humana broskceller började broskcellerna producera fler nedbrytningsenzym och mindre strukturellt kollagen, vilket visar att de åldrade synovialcellerna direkt kunde driva brosknedbrytning.
Brutet cellulärt städarbete och en viktig molekylbarometer
Friska celler återvinner ständigt utslitna mitokondrier genom en process kallad mitofagi, vilket förhindrar ansamling av defekta komponenter. I både rått‑ och humana synoviocyter som förts in i ett senescent tillstånd försvagades mitofagin: skadade mitokondrier staplades upp, mitokondriemembranpotentialen sjönk och proteiner kopplade till mitokondrieåtervinning minskade. Ett läkemedel som ökar mitofagi återställde delvis dessa åldersdrag, vilket tyder på att bristande mitokondriellt städarbete hjälper till att låsa cellerna i ett skadligt, senescent tillstånd. Teamet riktade sedan in sig på ett protein kallat METTL3, som lägger till en kemisk märkning (m6A) på RNA‑molekyler och kan förändra hur länge dessa budskap finns kvar i cellen. METTL3‑nivåerna var förhöjda i sjuka leder och i senescenta synoviocyter, tillsammans med ökade m6A‑markeringar överlag.
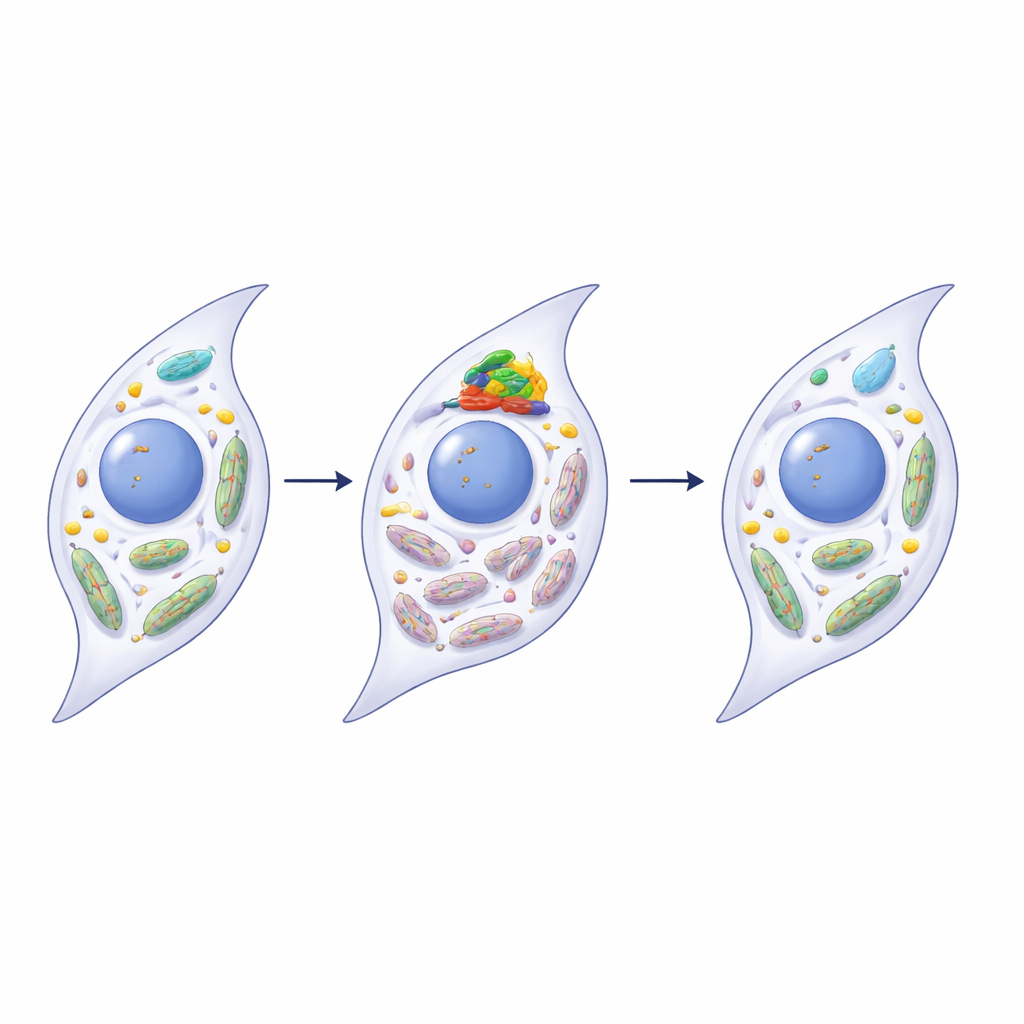
Återställning av mitokondriernas hälsa via PINK1
Forskarna upptäckte att METTL3 direkt påverkar ett mitokondriellt kvalitetskontrollprotein kallat PINK1, en central aktör i mitofagi. I sjuka leder och i åldrande synoviocyter bar PINK1‑RNA fler m6A‑markeringar och blev mindre stabilt, vilket minskade PINK1‑proteinmängderna. När METTL3 tystades i humana synoviocyter förlorade PINK1‑RNA en del av dessa markeringar, överlevde längre och producerade mer PINK1‑protein. Detta återställde i sin tur mitofagi, förbättrade mitokondriernas funktion och minskade flera kännetecken på senescens och inflammation. Att överuttrycka PINK1 ensamt hade liknande föryngrande effekter, medan blockering av PINK1 försvagade nyttan av METTL3‑tystning, vilket knöt ihop dessa steg i en enhetlig väg från RNA‑modifiering till mitokondrieupprättning.
Från cellåldrande till skada i käkleden
För att se om dessa åldrande synoviocyter kunde skada en led i ett levande djur injicerade teamet antingen normala eller senescenta synoviocyter i friska råttekäkleder. Leder som fick senescenta celler utvecklade snabbt drag av artros: försämrad benkvalitet under brosket, ojämna och uttunnade broskytytor, ökad smärtkänslighet, högre nivåer av inflammatoriska proteiner och tydliga reduktioner i markörer för mitofagi. Denna experimentella länkade molekylära förändringar inne i synovialcellerna till fullskalig leddegeneration och smärta.
Vad detta betyder för framtida vård av käkleden
Enkelt uttryckt tyder studien på att TMJ‑artros inte bara drivs av mekanisk belastning, utan av förtida åldrande i ledbeklädnadens celler vars trasiga mitokondriella städsystem håller dem fast i ett destruktivt läge. Ett molekylärt ”skrivande” protein, METTL3, påskyndar denna process genom att destabilisera RNA för PINK1, en nyckelvakt för mitokondriernas hälsa. Att dämpa METTL3 eller öka PINK1 återställde renare, effektivare mitokondrier, lugnade senescent beteende och skyddade brosk i experimentella modeller. Även om dessa fynd fortfarande måste bekräftas hos mänskliga patienter pekar de mot en ny slags terapi: istället för att bara dölja smärta eller ersätta skadad vävnad, skulle man kunna bromsa käkleddens artros genom att omprogrammera hur synovialceller åldras och underhåller sina inre kraftverk.
Citering: Tian, K., Du, Q., Guo, J. et al. METTL3-mediated fibroblast-like synoviocytes senescence promotes temporomandibular joint osteoarthritis progression. Commun Biol 9, 510 (2026). https://doi.org/10.1038/s42003-026-09773-x
Nyckelord: artros i käkleden, cellulärt åldrande, mitofagi, METTL3, PINK1