Clear Sky Science · de
METTL3-vermittelte Seneszenz fibroblastenähnlicher Synoviozyten fördert das Fortschreiten der Kiefergelenksarthrose
Warum Abnutzung des Kiefergelenks wichtig ist
Knacken, Schmerzen oder Steifheit im Kiefer sind mehr als nur lästig; für viele Menschen sind sie ein Hinweis auf Kiefergelenksarthrose (TMJ-OA), eine schmerzhafte Verschleißerkrankung des Kiefergelenks. Diese Studie blickt unter die Oberfläche des Gelenks und stellt eine einfache, aber wichtige Frage: Warum beginnt der dämpfende Knorpel im Kiefer zu zerfallen, und könnte das Verlangsamen einer bestimmten Form von Zellalterung ihn schützen? Die Forschenden legen eine molekulare Kette von Ereignissen in den gelenkauskleidenden Zellen frei, die den Weg zu gezielteren, weniger invasiven Behandlungen eröffnen könnte als aktuelle Medikamente oder Operationen.
Zellen, die still die Gelenkgesundheit formen
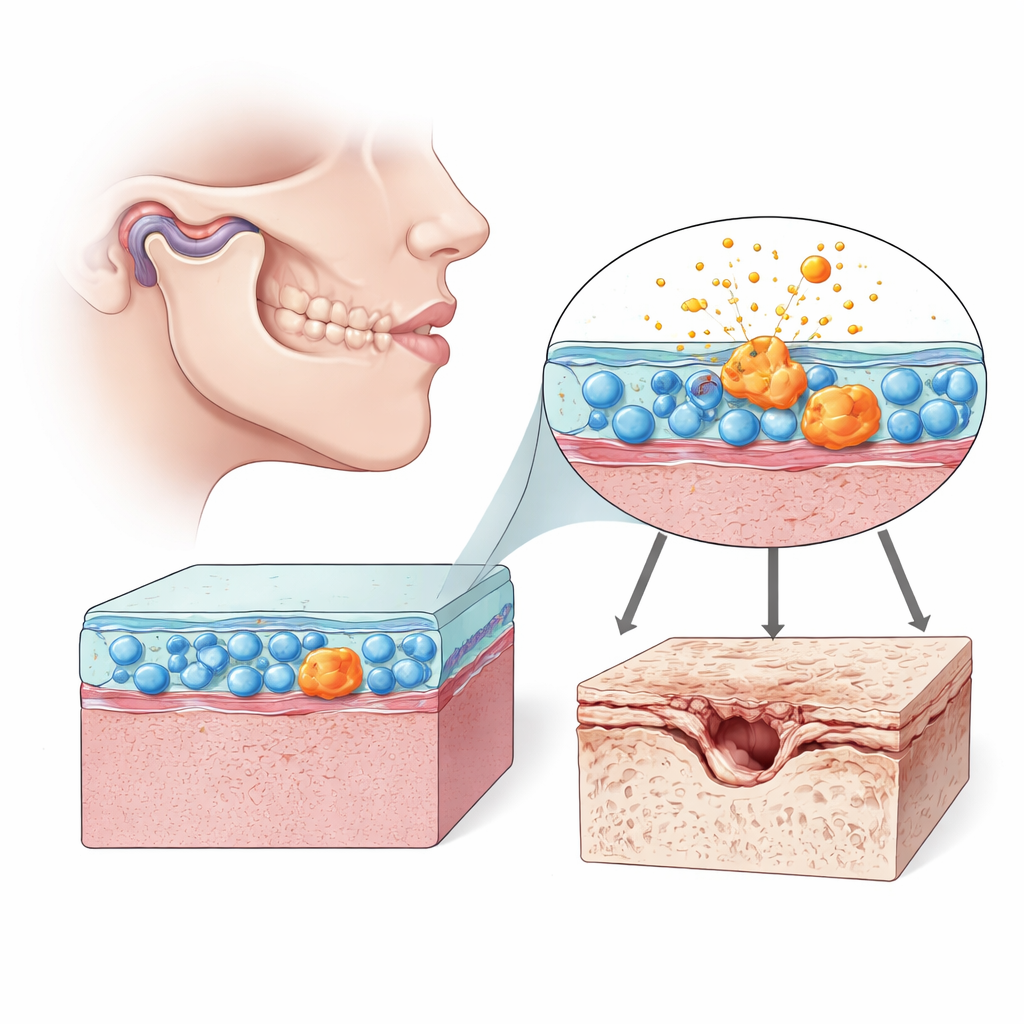
In jedem beweglichen Gelenk liegt eine weiche Auskleidung, die Synovialmembran, gefüllt mit fibroblastenähnlichen Synoviozyten — Zellen, die das Gelenk schmieren und ernähren. Im Kiefergelenk (TMJ) helfen diese Zellen, die kleine Scheibe und die Knorpeloberflächen beim Kauen und Sprechen glatt gleiten zu lassen. Wenn diese synovialen Zellen jedoch fehlreguliert sind, können sie das Gelenk mit entzündlichen Molekülen und enzymatischen Baubrechern überschwemmen, die den Knorpel angreifen. Die Autor*innen konzentrierten sich darauf, wie sich diese Zellen bei TMJ-Arthrose in Ratten und in menschlichen Zellkulturen verhalten, mit besonderem Augenmerk auf Anzeichen zellulärer Alterung (Seneszenz) und auf die Gesundheit ihrer Energieproduktionszentren, der Mitochondrien.
Wenn gelenkauskleidende Zellen vorzeitig altern
Mit einem chemischen Reiz, der TMJ-Arthrose bei Ratten auslöst, bestätigte das Team die klassischen Merkmale der Krankheit: aufgerauter Knochen unter dem Knorpel, verdünnter Knorpel, erhöhte Schmerzempfindlichkeit und höhere Spiegel entzündlicher Botenstoffe. In der Gelenkauskleidung zeigten viele Synoviozyten Seneszenzmarker — Zellen, die nicht mehr teilen, aber metabolisch aktiv und stark entzündungsfördernd sind. Diese seneszenten Zellen wiesen trägere interne Reinigungsmechanismen und beschädigte Mitochondrien auf. Als die Forschenden diese gelenkauskleidenden Zellen isolierten und mit menschlichen Knorpelzellen kultivierten, begannen die Knorpelzellen, mehr Abbauenzyme und weniger strukturelles Kollagen zu produzieren, was zeigt, dass gealterte synoviale Zellen direkt Knorpelschaden antreiben können.
Gestörte zelluläre Reinigung und ein wichtiger molekularer Schalter
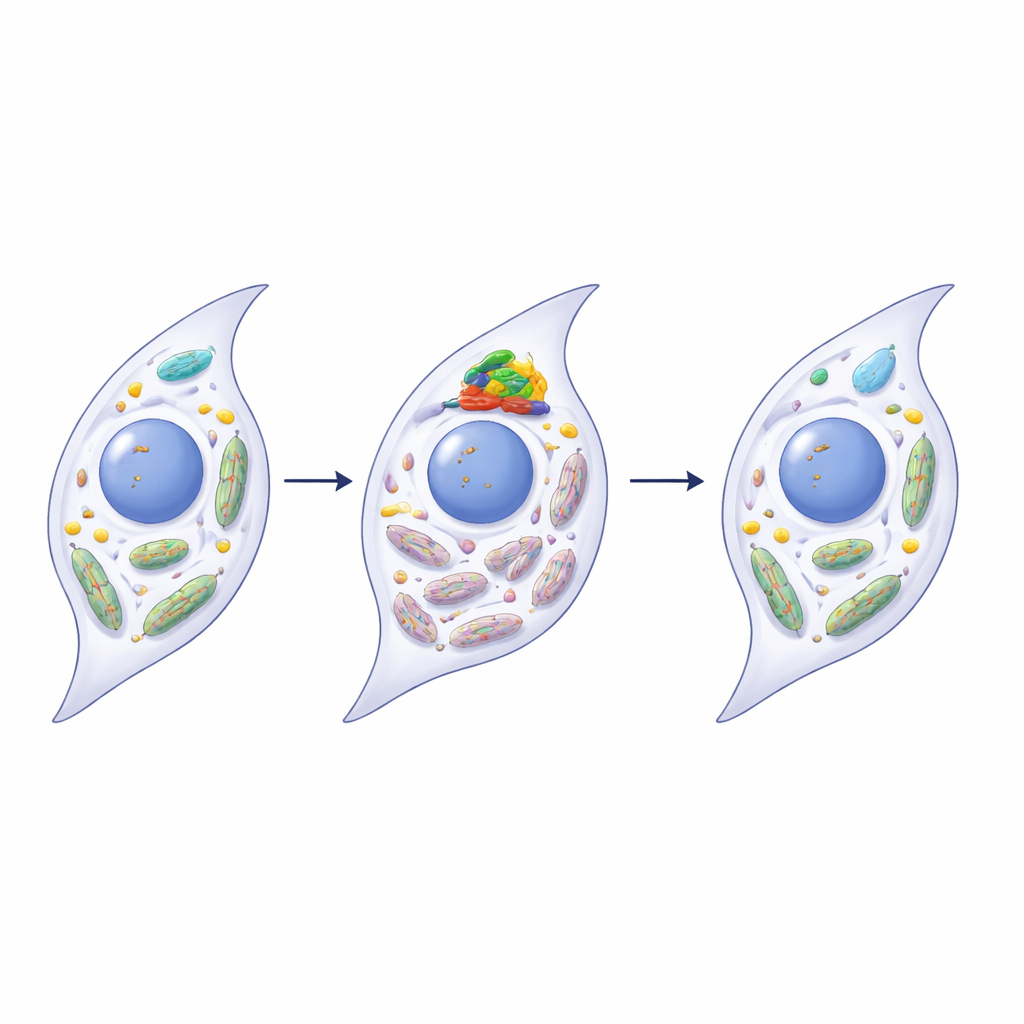
Gesunde Zellen recyceln ständig abgenutzte Mitochondrien durch einen Prozess namens Mitophagie, wodurch die Anhäufung defekter Komponenten vermieden wird. Sowohl in Ratten- als auch in menschlichen Synoviozyten, die in einen seneszenten Zustand gedrängt wurden, war die Mitophagie geschwächt: beschädigte Mitochondrien türmten sich auf, das mitochondriale Membranpotenzial fiel, und Proteine, die mit der mitochondrialen Rezyklierung zusammenhängen, gingen zurück. Ein Medikament, das die Mitophagie fördert, kehrte diese Alterungsmerkmale teilweise um, was darauf hindeutet, dass schlechte mitochondriale Reinigung diese Zellen in einem schädlichen, seneszenten Zustand festsetzt. Das Team richtete dann das Augenmerk auf ein Protein namens METTL3, das eine chemische Markierung (m6A) an RNA-Moleküle anbringt und so die Lebensdauer dieser Nachrichten in der Zelle verändern kann. METTL3-Spiegel waren in erkrankten Gelenken und in seneszenten Synoviozyten erhöht, zusammen mit einem Anstieg der Gesamt-m6A-Markierungen.
Wiederherstellung der mitochondrialen Gesundheit über PINK1
Die Forschenden fanden heraus, dass METTL3 direkt ein mitochondriales Qualitätskontrollprotein namens PINK1 beeinflusst, einen zentralen Akteur der Mitophagie. In erkrankten Gelenken und in alternden Synoviozyten trug die RNA für PINK1 mehr m6A-Markierungen und wurde instabiler, was die PINK1-Proteinspiegel verringerte. Als METTL3 in menschlichen Synoviozyten stillgelegt wurde, verlor die PINK1-RNA einige dieser Markierungen, überdauerte länger und erzeugte mehr PINK1-Protein. Dies stellte wiederum die Mitophagie wieder her, verbesserte die mitochondriale Funktion und reduzierte mehrere Kennzeichen von Seneszenz und Entzündung. Eine alleinige Überexpression von PINK1 zeigte ähnliche verjüngende Effekte, während die Blockade von PINK1 die Vorteile der METTL3-Stummschaltung abschwächte, was diese Schritte zu einem einzelnen Weg von RNA-Modifikation zur mitochondrialen Reparatur verknüpft.
Von Zellalterung zu Kiefergelenkschäden
Um zu prüfen, ob diese alternden Synoviozyten ein Gelenk in einem lebenden Tier schädigen können, injizierte das Team entweder normale oder seneszente Synoviozyten in gesunde Ratten-Kiefergelenke. Gelenke, die seneszente Zellen erhielten, entwickelten schnell Merkmale der Arthrose: Verlust der Knochenqualität unter dem Knorpel, aufgeraute und verdünnte Knorpeloberflächen, erhöhte Schmerzempfindlichkeit, höhere Spiegel entzündlicher Proteine und deutliche Reduktionen von Markern der Mitophagie. Dieses Experiment verband molekulare Veränderungen innerhalb synovialer Zellen mit vollständiger Gelenkdegeneration und Schmerz.
Was das für die zukünftige Versorgung des Kiefergelenks bedeutet
Einfach gesagt deutet die Studie darauf hin, dass TMJ-Arthrose nicht nur durch mechanische Belastung angetrieben wird, sondern durch vorzeitig alternde gelenkauskleidende Zellen, deren defekte mitochondriale Reinigungssysteme sie in einem destruktiven Modus festhalten. Ein molekularer „Writer“-Protein, METTL3, beschleunigt diesen Prozess, indem es die RNA für PINK1 destabilisiert — einen Schlüsselwächter der mitochondrialen Gesundheit. Das Herunterregulieren von METTL3 oder das Verstärken von PINK1 stellte sauberere, effizientere Mitochondrien her, beruhigte das seneszente Verhalten und schützte den Knorpel in experimentellen Modellen. Während diese Befunde noch bei menschlichen Patient*innen bestätigt werden müssen, weisen sie auf eine neue Therapieoption hin: Anstatt nur Schmerzen zu maskieren oder beschädigtes Gewebe zu ersetzen, könnten wir die Kiefergelenksarthrose verlangsamen, indem wir die Alterung und die Instandhaltung der „Kraftwerke“ synovialer Zellen umprogrammieren.
Zitation: Tian, K., Du, Q., Guo, J. et al. METTL3-mediated fibroblast-like synoviocytes senescence promotes temporomandibular joint osteoarthritis progression. Commun Biol 9, 510 (2026). https://doi.org/10.1038/s42003-026-09773-x
Schlüsselwörter: Kiefergelenksarthrose, zelluläre Seneszenz, Mitophagie, METTL3, PINK1