Clear Sky Science · nl
Door METTL3 veroorzaakte veroudering van fibroblast-achtige synoviocyten bevordert progressie van osteoartritis van het kaakgewricht
Waarom slijtage van het kaakgewricht ertoe doet
Klikkende geluiden, pijn of stijfheid in de kaak zijn meer dan een ergernis; voor veel mensen wijzen ze op osteoartritis van het temporomandibulair gewricht (TMJ), een pijnlijke slijtageaandoening van het kaakgewricht. Deze studie kijkt voorbij het oppervlak van het gewricht en stelt een eenvoudige maar belangrijke vraag: waarom begint het dempende kraakbeen in de kaak af te breken, en zou het vertragen van een specifiek type celdood of -veroudering het kunnen beschermen? De onderzoekers onthullen een moleculaire keten van gebeurtenissen in cellen van het gewrichtsvochtvlies die de deur kan openen naar gerichtere, minder invasieve behandelingen dan huidige medicijnen of chirurgie.
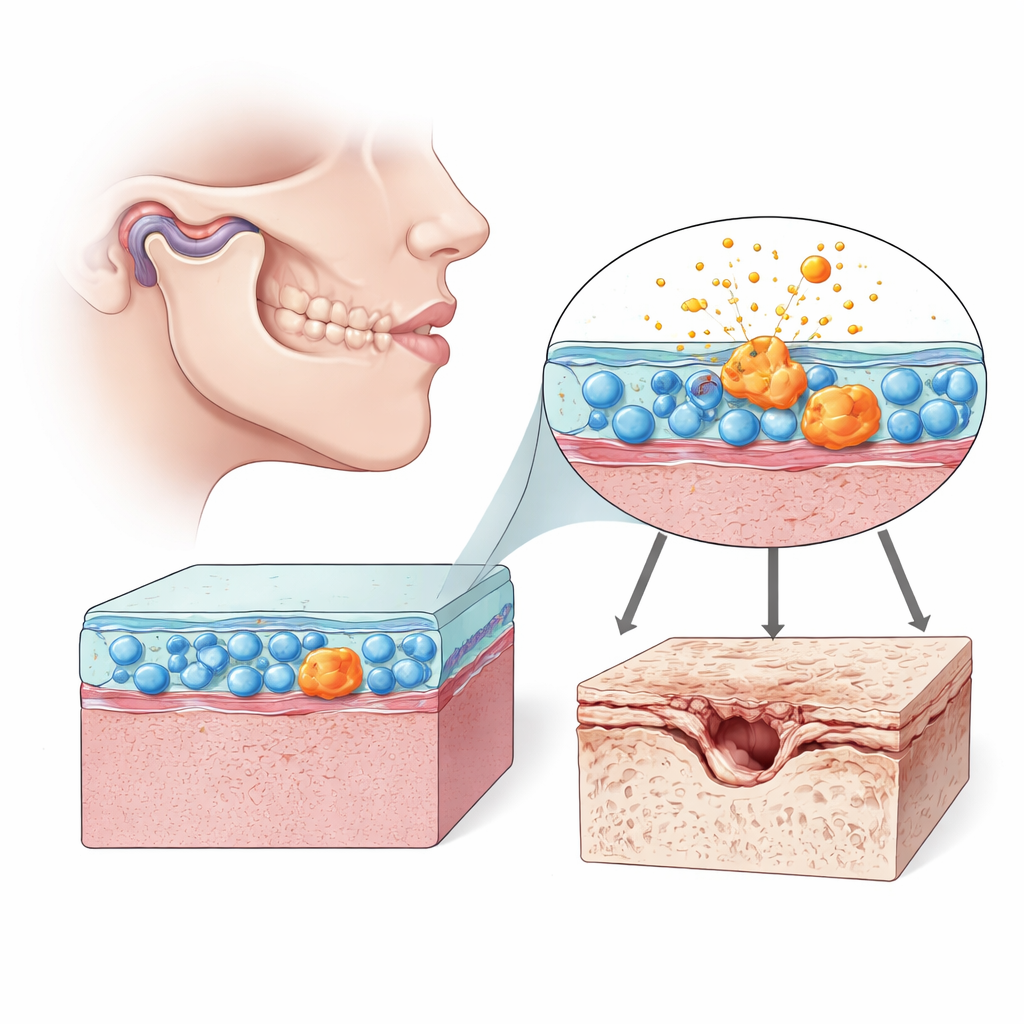
Cellen die geruisloos de gewrichtsgezondheid bepalen
In elk beweeglijk gewricht bevindt zich een zachte voering, het synovium, vol met fibroblast-achtige synoviocyten—cellen die helpen het gewricht te smeren en te voeden. In het temporomandibulair gewricht helpen deze cellen de kleine schijf en kraakbeenoppervlakken soepel te laten glijden tijdens kauwen en praten. Maar wanneer deze synoviale cellen ontsporen, kunnen ze het gewricht overspoelen met ontstekingsmoleculen en enzymen die het kraakbeen afbreken. De auteurs richtten zich op het gedrag van deze cellen bij TMJ-osteoartritis in ratten en in menselijke celkweken, met bijzondere aandacht voor tekenen van cellulaire veroudering, of senescentie, en de gezondheid van hun energiecentrales, de mitochondriën.
Wanneer gewrichtsvliescellen te vroeg verouderen
Met behulp van een chemische trigger om TMJ-osteoartritis bij ratten op te wekken, bevestigde het team klassieke kenmerken van de ziekte: ruw(er) bot onder het kraakbeen, dunner wordend kraakbeen, verhoogde pijngevoeligheid en hogere niveaus van ontstekingsboodschappers. In het gewrichtsvlies toonden veel synoviocyten markers van senescentie—cellen die gestopt zijn met delen maar metabolisch actief en sterk ontstekingsbevorderend blijven. Deze senescente cellen hadden vertraagde interne opruimsystemen en beschadigde mitochondriën. Toen de onderzoekers deze gewrichtsvliescellen isoleerden en samen met menselijke kraakbeencellen lieten groeien, begonnen de kraakbeencellen meer afbraakenzymen en minder structureel collageen te produceren, wat laat zien dat de verouderde synoviale cellen het kraakbeen direct konden beschadigen.
Gebroken cellulaire opruiming en een belangrijke moleculaire schakelaar
Gezonde cellen recyclen voortdurend versleten mitochondriën via een proces dat mitofagie wordt genoemd, waardoor de ophoping van defecte componenten wordt voorkomen. Zowel in rat- als in menselijke synoviocyten die in een senescentietoestand werden geduwd, was mitofagie verzwakt: beschadigde mitochondriën stapelden zich op, de mitochondriale membraanpotentiaal daalde en eiwitten die met mitochondriale recycling samenhangen namen af. Een middel dat mitofagie versterkt keerde deze verouderingskenmerken deels om, wat suggereert dat slechte mitochondriale opruiming helpt deze cellen vast te zetten in een schadelijke, senescente staat. Het team zoomde vervolgens in op een eiwit genaamd METTL3, dat een chemische markering (m6A) aan RNA-moleculen toevoegt en kan veranderen hoe lang die boodschappen in de cel blijven. METTL3-niveaus waren verhoogd in zieke gewrichten en in senescente synoviocyten, samen met een algemene toename van m6A-markeringen.
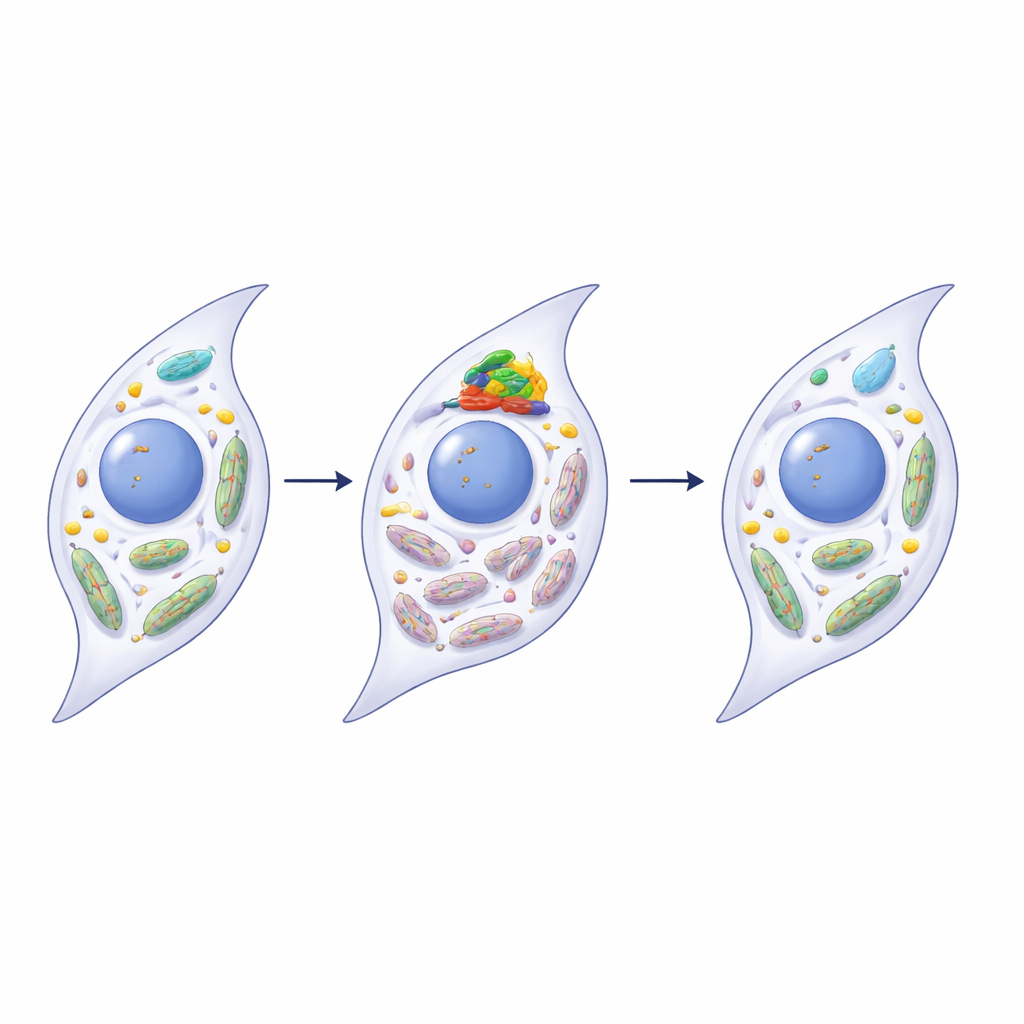
Herstellen van mitochondriale gezondheid via PINK1
De onderzoekers ontdekten dat METTL3 direct invloed uitoefent op een mitochondriale kwaliteitscontrole-eiwit genaamd PINK1, een centrale speler in mitofagie. In zieke gewrichten en in verouderende synoviocyten droeg het RNA voor PINK1 meer m6A-markeringen en werd het minder stabiel, waardoor de PINK1-eiwitniveaus afnamen. Toen METTL3 in menselijke synoviocyten werd uitgezet, verloor PINK1-RNA een deel van deze markeringen, bleef het langer bestaan en produceerde het meer PINK1-eiwit. Dit herstelde op zijn beurt mitofagie, verbeterde de mitochondriale functie en verminderde meerdere kenmerken van senescentie en ontsteking. Alleen PINK1 overexpressie had vergelijkbare verjongende effecten, terwijl het blokkeren van PINK1 de voordelen van METTL3-onderdrukking verminderde, waarmee deze stappen werden verbonden in één pad van RNA-modificatie naar mitochondriale reparatie.
Van celveroudering naar schade aan het kaakgewricht
Om te onderzoeken of deze verouderende synoviocyten een gewricht in een levend dier konden beschadigen, injecteerde het team ofwel normale ofwel senescente synoviocyten in gezonde kaakgewrichten van ratten. Gewrichten die senescente cellen ontvingen ontwikkelden snel kenmerken van osteoartritis: verlies van botkwaliteit onder het kraakbeen, ruwe en verdunne kraakbeenoppervlakken, toegenomen pijngevoeligheid, hogere niveaus van ontstekingsproteïnen en duidelijke verminderingen in markers van mitofagie. Dit experiment koppelde moleculaire veranderingen binnen synoviale cellen aan volledige gewrichtsdegeneratie en pijn.
Wat dit betekent voor toekomstige zorg van het kaakgewricht
In eenvoudige termen suggereert de studie dat TMJ-osteoartritis niet alleen wordt aangedreven door mechanische stress, maar door voortijdig verouderende gewrichtsvliescellen waarvan kapotte mitochondriale opruimsystemen hen vastzetten in een destructieve modus. Een moleculair "schrijver"-eiwit, METTL3, versnelt dit proces door het RNA voor PINK1 te destabiliseren, een sleutelbeschermer van mitochondriale gezondheid. Het verminderen van METTL3 of het versterken van PINK1 herstelde schonere, efficiëntere mitochondriën, kalmeerde senescente eigenschappen en beschermde kraakbeen in experimentele modellen. Hoewel deze bevindingen nog gevalideerd moeten worden bij menselijke patiënten, wijzen ze op een nieuw soort therapie: in plaats van alleen pijn te maskeren of beschadigd weefsel te vervangen, zouden we mogelijk osteoartritis van het kaakgewricht kunnen vertragen door te herprogrammeren hoe synoviale cellen verouderen en hun interne energiecentrales onderhouden.
Bronvermelding: Tian, K., Du, Q., Guo, J. et al. METTL3-mediated fibroblast-like synoviocytes senescence promotes temporomandibular joint osteoarthritis progression. Commun Biol 9, 510 (2026). https://doi.org/10.1038/s42003-026-09773-x
Trefwoorden: osteoartritis van het temporomandibulair gewricht, cellulaire veroudering, mitofagie, METTL3, PINK1