Clear Sky Science · it
La senescenza delle sinoviociti fibroblasto-simili mediata da METTL3 promuove la progressione dell’osteoartrosi dell’articolazione temporomandibolare
Perché l’usura dell’articolazione della mandibola conta
Scrosci, dolore o rigidità della mandibola possono essere più di un fastidio; per molte persone sono il segnale di un’osteoartrosi dell’articolazione temporomandibolare (ATM), una dolorosa degenerazione da usura dell’articolazione mandibolare. Questo studio scava sotto la superficie dell’articolazione per porsi una domanda semplice ma importante: perché la cartilagine ammortizzante della mandibola inizia a deteriorarsi, e rallentare un particolare tipo di invecchiamento cellulare potrebbe aiutare a proteggerla? I ricercatori svelano una catena molecolare di eventi all’interno delle cellule che rivestono l’articolazione, che potrebbe aprire la strada a trattamenti più mirati e meno invasivi rispetto ai farmaci o alla chirurgia attuali.
Cellule che silenziosamente modellano la salute articolare
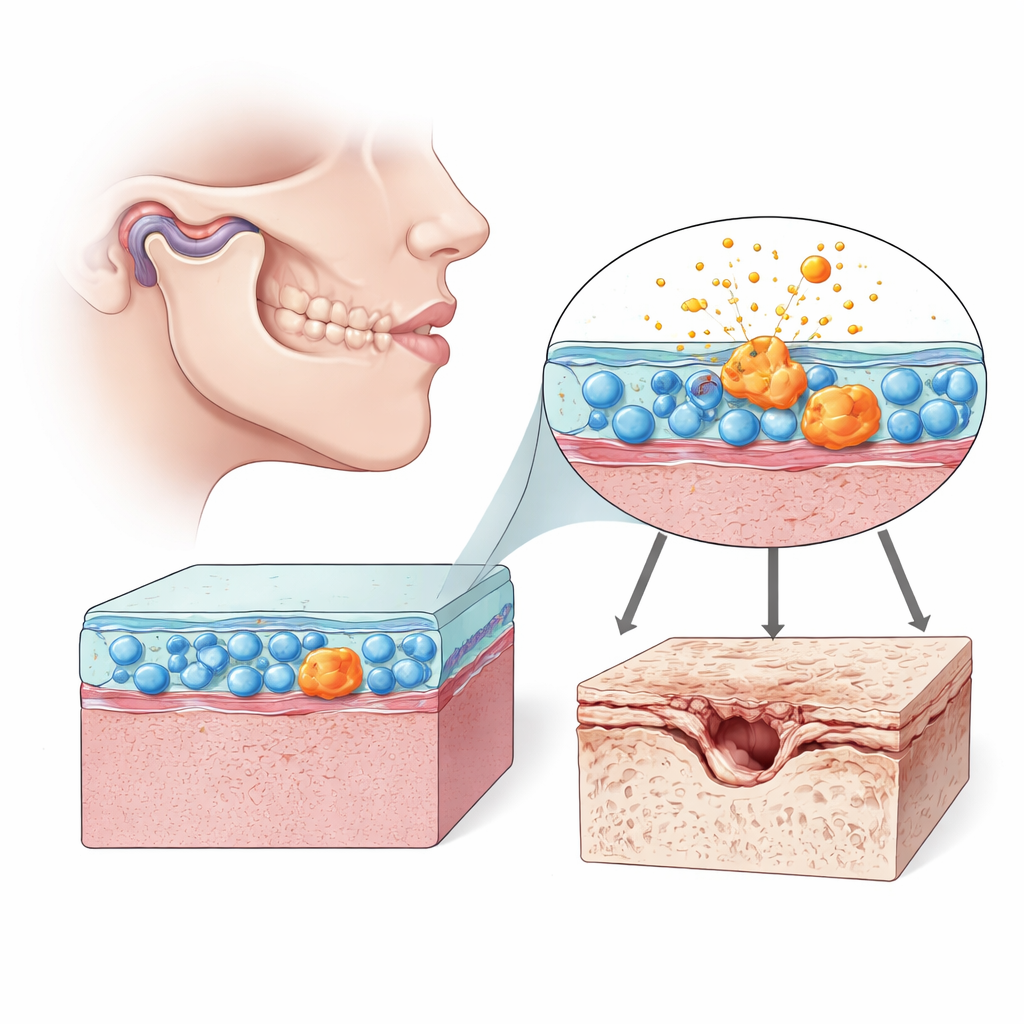
All’interno di ogni articolazione mobile c’è un rivestimento morbido chiamato sinovia, ricco di sinoviociti fibroblasto-simili—cellule che aiutano a lubrificare e nutrire l’articolazione. Nell’articolazione temporomandibolare (ATM), queste cellule mantengono il piccolo disco e le superfici cartilaginee scorrevoli mentre mastichiamo e parliamo. Ma quando queste cellule sinoviali si alterano, possono inondare l’articolazione di molecole infiammatorie ed enzimi che degradano la cartilagine. Gli autori si sono concentrati sul comportamento di queste cellule nell’osteoartrosi dell’ATM nei ratti e in colture cellulari umane, prestando particolare attenzione ai segni dell’invecchiamento cellulare, o senescenza, e alla salute dei loro “forni energetici”, i mitocondri.
Quando le cellule che rivestono l’articolazione invecchiano prima del tempo
Usando una sostanza chimica per indurre l’osteoartrosi dell’ATM nei ratti, il gruppo ha confermato i segni classici della malattia: osso sottostante alla cartilagine irregolare, assottigliamento della cartilagine, maggiore sensibilità al dolore e livelli più elevati di mediatori infiammatori. Nella sinovia molte sinoviociti presentavano marcatori di senescenza—cellule che hanno smesso di dividersi ma restano metabolicamente attive e altamente infiammatorie. Queste cellule senescenti mostravano sistemi di pulizia interni lenti e mitocondri danneggiati. Quando i ricercatori isolavano queste cellule sinoviali e le coltivavano insieme a cellule cartilaginee umane, le cellule cartilaginee cominciavano a produrre più enzimi degradativi e meno collagene strutturale, dimostrando che le sinoviociti invecchiate possono guidare direttamente il danno cartilagineo.
Pulizia cellulare compromessa e un interruttore molecolare chiave
Le cellule sane riciclano costantemente i mitocondri usurati attraverso un processo chiamato mitofagia, evitando l’accumulo di componenti difettosi. Sia nelle sinoviociti di ratto che in quelle umane spinte in uno stato senescente, la mitofagia risultava indebolita: i mitocondri danneggiati si accumulavano, il potenziale di membrana mitocondriale calava e le proteine associate al riciclo mitocondriale diminuivano. Un farmaco che potenzia la mitofagia ha parzialmente invertito questi tratti di invecchiamento, suggerendo che la scarsa pulizia mitocondriale contribuisce a intrappolare queste cellule in uno stato senescente dannoso. Il team si è quindi concentrato su una proteina chiamata METTL3, che aggiunge un’etichetta chimica (m6A) alle molecole di RNA e può modificare la durata di quei messaggi nella cellula. I livelli di METTL3 erano elevati nelle articolazioni malate e nelle sinoviociti senescenti, insieme a un aumento complessivo delle marcature m6A.
Salvare la salute mitocondriale tramite PINK1
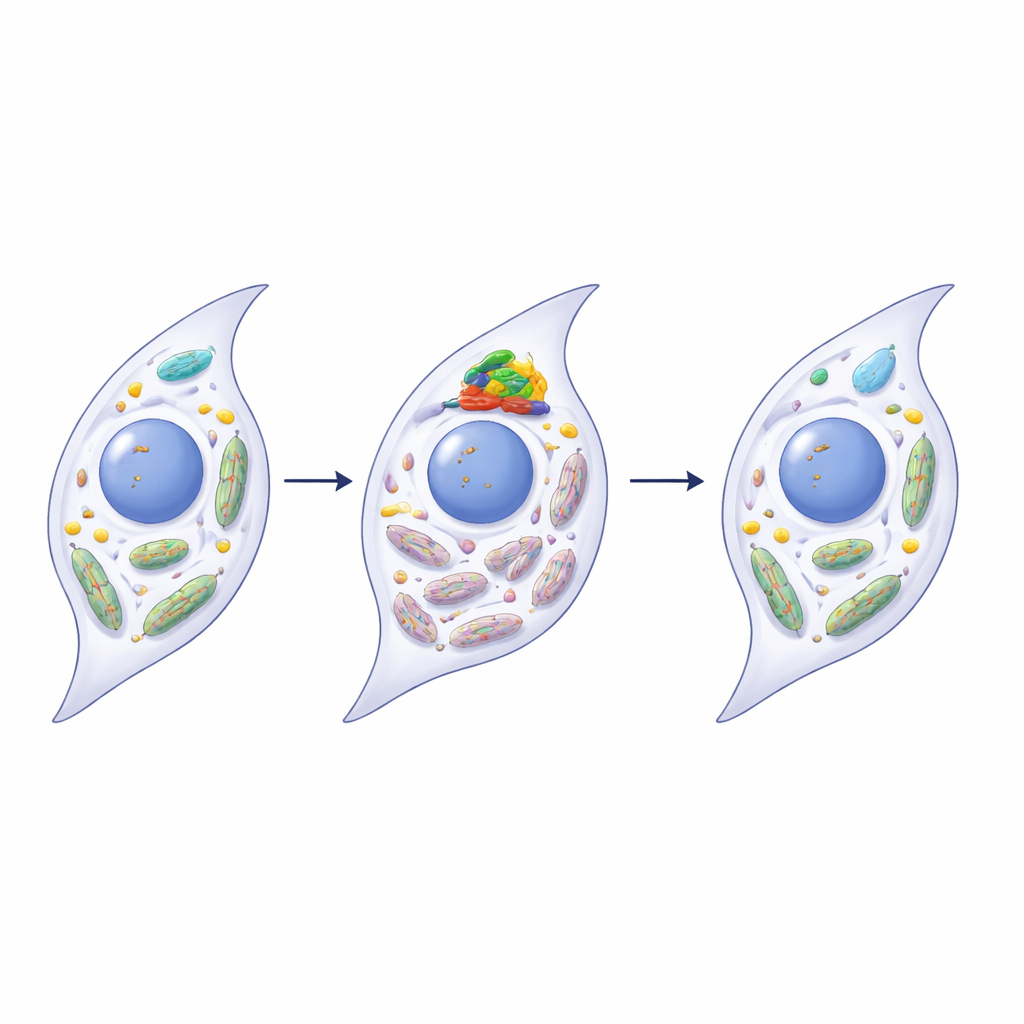
I ricercatori hanno scoperto che METTL3 influenza direttamente una proteina di qualità mitocondriale chiamata PINK1, un attore centrale nella mitofagia. Nelle articolazioni malate e nelle sinoviociti invecchiate, l’RNA per PINK1 portava più marcature m6A e diventava meno stabile, riducendo i livelli della proteina PINK1. Quando METTL3 è stato silenziato nelle sinoviociti umane, l’RNA di PINK1 perdeva parte di queste marcature, sopravviveva più a lungo e produceva più proteina PINK1. Questo, a sua volta, ha ripristinato la mitofagia, migliorato la funzione mitocondriale e ridotto molteplici caratteristiche della senescenza e dell’infiammazione. L’iperespressione di PINK1 da sola ha avuto effetti ringiovanenti simili, mentre il blocco di PINK1 attenuava i benefici del silenziamento di METTL3, collegando questi passaggi in una singola via dal processo di modifica dell’RNA alla riparazione mitocondriale.
Dall’invecchiamento cellulare al danno dell’articolazione mandibolare
Per verificare se queste sinoviociti invecchiate potessero danneggiare un’articolazione in un animale vivo, il team ha iniettato sinoviociti normali o senescenti nelle articolazioni mandibolari sane di ratti. Le articolazioni che ricevevano cellule senescenti hanno sviluppato rapidamente caratteristiche di osteoartrosi: perdita di qualità dell’osso sotto la cartilagine, superfici cartilaginee ruvide e assottigliate, maggiore sensibilità al dolore, livelli più alti di proteine infiammatorie e chiare riduzioni nei marcatori di mitofagia. Questo esperimento ha collegato i cambiamenti molecolari all’interno delle cellule sinoviali alla degenerazione articolare completa e al dolore.
Cosa significa per la cura futura dell’articolazione della mandibola
In termini semplici, lo studio suggerisce che l’osteoartrosi dell’ATM non è alimentata soltanto dallo stress meccanico, ma anche da cellule del rivestimento articolare che invecchiano prematuramente e i cui sistemi di pulizia mitocondriale compromessi le mantengono in uno stato distruttivo. Una proteina “scrittrice” molecolare, METTL3, accelera questo processo destabilizzando l’RNA per PINK1, un guardiano chiave della salute mitocondriale. Abbassare l’attività di METTL3 o potenziare PINK1 ha riportato mitocondri più efficienti, attenuato i comportamenti senescenti e protetto la cartilagine nei modelli sperimentali. Sebbene questi risultati debbano ancora essere validati nei pazienti umani, puntano a un nuovo tipo di terapia: invece di limitarsi a mascherare il dolore o sostituire il tessuto danneggiato, si potrebbe rallentare l’osteoartrosi mandibolare riprogrammando il modo in cui le cellule sinoviali invecchiano e mantengono i loro “impianti energetici” interni.
Citazione: Tian, K., Du, Q., Guo, J. et al. METTL3-mediated fibroblast-like synoviocytes senescence promotes temporomandibular joint osteoarthritis progression. Commun Biol 9, 510 (2026). https://doi.org/10.1038/s42003-026-09773-x
Parole chiave: osteoartrosi dell’articolazione temporomandibolare, senescenza cellulare, mitofagia, METTL3, PINK1