Clear Sky Science · fr
La sénescence des synoviocytes de type fibroblastique médiée par METTL3 favorise la progression de l’arthrose de l’articulation temporo-mandibulaire
Pourquoi l’usure de l’articulation de la mâchoire compte
Les claquements, la douleur ou la raideur de la mâchoire peuvent être plus qu’une gêne ; pour beaucoup, ils signalent une arthrose de l’articulation temporo-mandibulaire (ATM), une maladie douloureuse d’usure de l’articulation de la mâchoire. Cette étude examine ce qui se passe sous la surface de l’articulation pour poser une question simple mais importante : pourquoi le cartilage amortisseur de la mâchoire commence-t-il à se dégrader, et ralentir un type particulier de vieillissement cellulaire pourrait‑il aider à le protéger ? Les chercheurs mettent au jour une chaîne d’événements moléculaires au sein des cellules de la synoviale qui pourrait ouvrir la voie à des traitements plus ciblés et moins invasifs que les médicaments actuels ou la chirurgie.
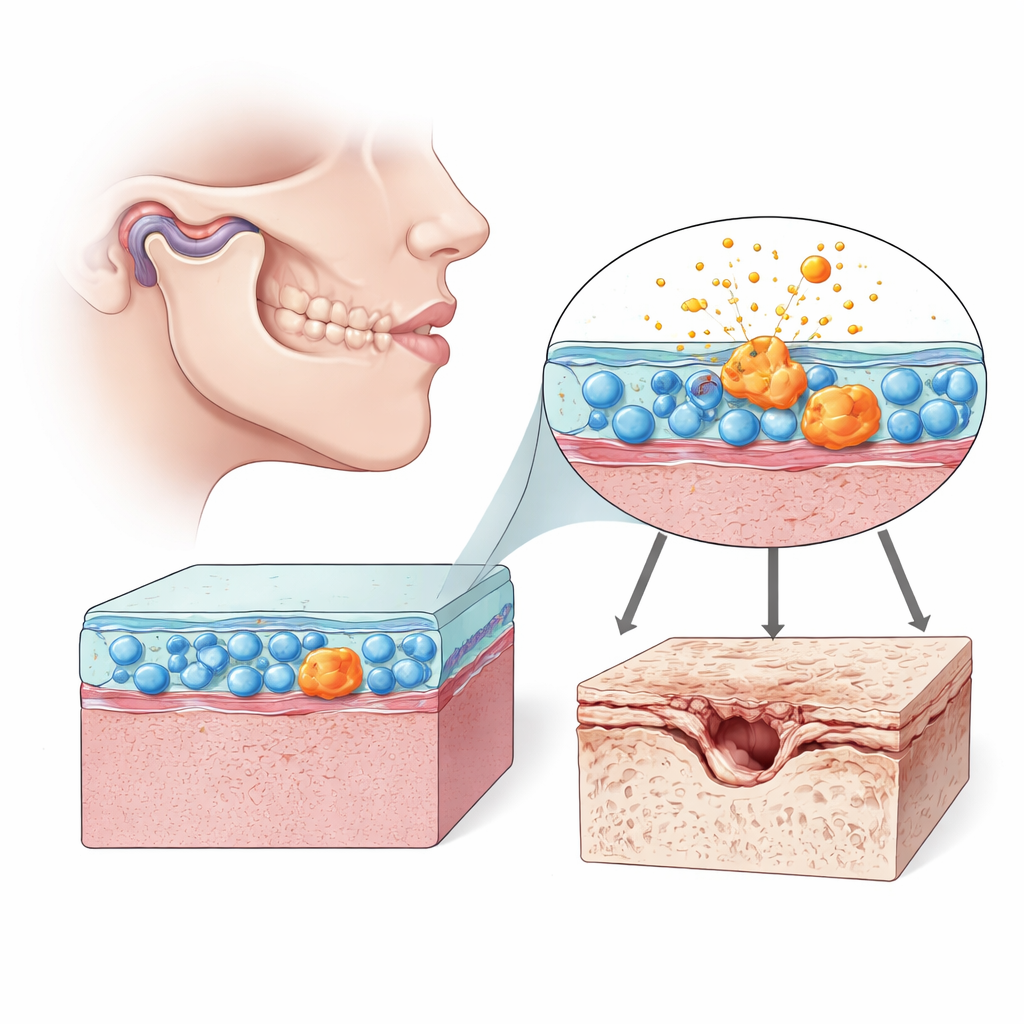
Des cellules qui façonnent discrètement la santé de l’articulation
À l’intérieur de chaque articulation mobile se trouve une couche souple appelée synovie, riche en synoviocytes de type fibroblastique — des cellules qui aident à lubrifier et à nourrir l’articulation. Dans l’ATM, ces cellules participent au bon glissement du petit disque et des surfaces cartilagineuses lorsque nous mâchons et parlons. Mais quand ces cellules synoviales dysfonctionnent, elles peuvent inonder l’articulation de molécules inflammatoires et d’enzymes qui dégradent le cartilage. Les auteurs se sont concentrés sur le comportement de ces cellules dans l’arthrose de l’ATM chez le rat et dans des cultures cellulaires humaines, en portant une attention particulière aux signes de vieillissement cellulaire, ou sénescence, et à la santé de leurs mitochondries, les centrales énergétiques de la cellule.
Lorsque les cellules de la synoviale vieillissent prématurément
En utilisant un produit chimique pour induire une arthrose de l’ATM chez le rat, l’équipe a confirmé les caractéristiques classiques de la maladie : os sous-cartilagineux rugueux, amincissement du cartilage, sensibilité accrue à la douleur et niveaux plus élevés de médiateurs inflammatoires. Dans la membrane synoviale, de nombreux synoviocytes présentaient des marqueurs de sénescence — des cellules qui ont cessé de se diviser mais restent métaboliquement actives et fortement inflammatoires. Ces cellules sénescentes présentaient des systèmes internes de nettoyage lents et des mitochondries endommagées. Lorsque les chercheurs ont isolé ces cellules synoviales et les ont mises en culture avec des chondrocytes humains, les chondrocytes ont commencé à produire davantage d’enzymes de dégradation et moins de collagène structurel, montrant que les cellules synoviales vieillies pouvaient directement entraîner la dégradation du cartilage.
Un nettoyage cellulaire défaillant et un interrupteur moléculaire clé
Les cellules saines recyclent constamment les mitochondries usées par un processus appelé mitophagie, ce qui évite l’accumulation de composants défectueux. Chez les synoviocytes de rat et d’origine humaine poussés en état de sénescence, la mitophagie était affaiblie : les mitochondries endommagées s’accumulaient, le potentiel membranaire mitochondrial chutait et les protéines liées au recyclage mitochondrial diminuaient. Un médicament stimulant la mitophagie a partiellement inversé ces caractéristiques du vieillissement, suggérant qu’un mauvais nettoyage mitochondrial contribue à verrouiller ces cellules dans un état sénescent nocif. L’équipe s’est ensuite intéressée à une protéine appelée METTL3, qui ajoute une balise chimique (m6A) aux molécules d’ARN et peut modifier la durée de vie de ces messages dans la cellule. Les niveaux de METTL3 étaient élevés dans les articulations malades et dans les synoviocytes sénescents, de même que les marques globales m6A.
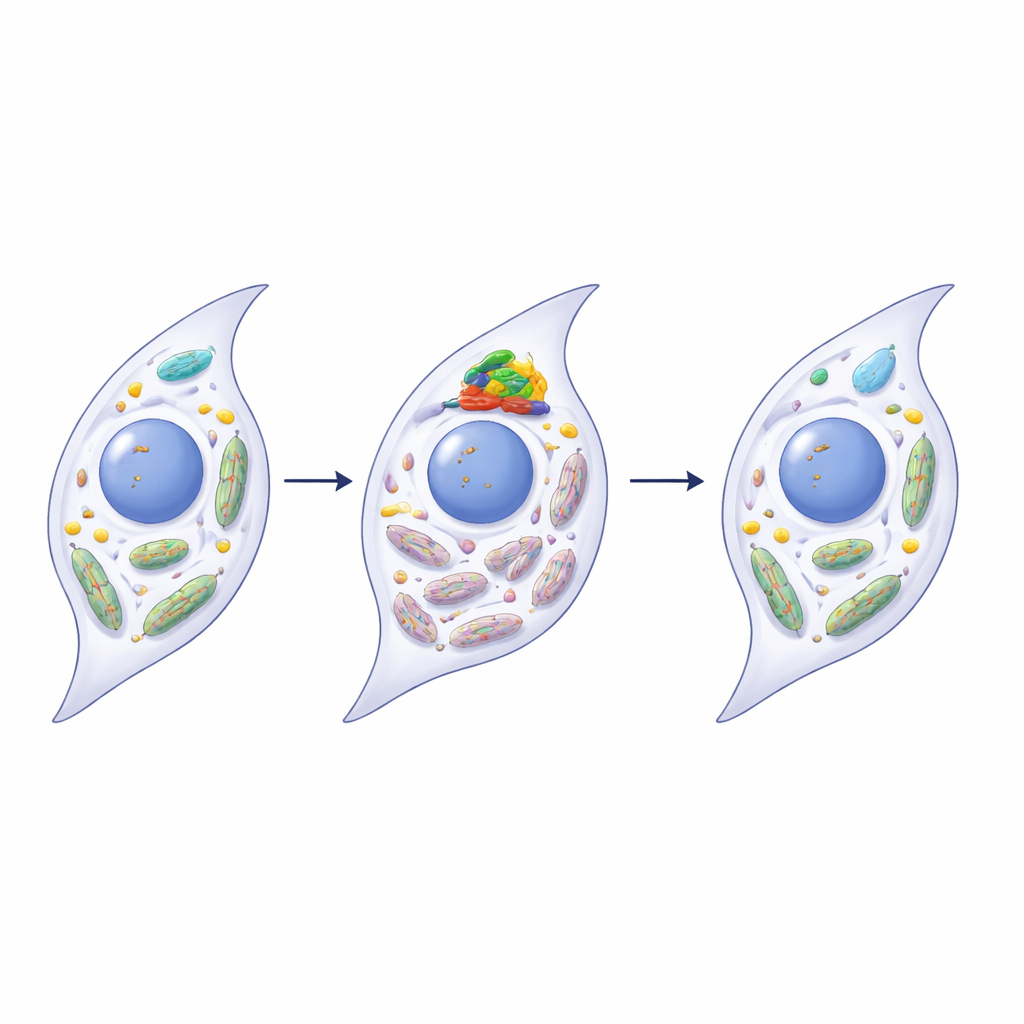
Restaurer la santé mitochondriale via PINK1
Les chercheurs ont découvert que METTL3 influence directement une protéine de contrôle de la qualité mitochondriale appelée PINK1, acteur central de la mitophagie. Dans les articulations malades et chez les synoviocytes vieillissants, l’ARN de PINK1 présentait davantage de marques m6A et devenait moins stable, entraînant une réduction des niveaux de protéine PINK1. Lorsque METTL3 a été inhibé chez des synoviocytes humains, l’ARN de PINK1 a perdu une partie de ces marques, a survécu plus longtemps et a produit davantage de protéine PINK1. Cela a, à son tour, restauré la mitophagie, amélioré la fonction mitochondriale et réduit plusieurs caractéristiques de la sénescence et de l’inflammation. La surexpression de PINK1 seule produisait des effets rajeunissants similaires, tandis que le blocage de PINK1 atténuait les bénéfices de l’inhibition de METTL3, reliant ces étapes dans une seule voie allant de la modification de l’ARN à la réparation mitochondriale.
Du vieillissement cellulaire aux lésions de l’articulation mandibulaire
Pour savoir si ces synoviocytes âgés pouvaient endommager une articulation chez un animal vivant, l’équipe a injecté soit des synoviocytes normaux soit des synoviocytes sénescents dans des articulations mandibulaires de rats sains. Les articulations ayant reçu des cellules sénescentes ont rapidement développé des signes d’arthrose : perte de qualité de l’os sous-cartilagineux, surfaces cartilagineuses rugueuses et amincies, sensibilité accrue à la douleur, niveaux plus élevés de protéines inflammatoires et réductions nettes des marqueurs de mitophagie. Cette expérience a relié les changements moléculaires à l’intérieur des cellules synoviales à une dégénérescence articulaire complète et à la douleur.
Ce que cela signifie pour la prise en charge future de l’ATM
En termes simples, l’étude suggère que l’arthrose de l’ATM n’est pas seulement alimentée par le stress mécanique, mais aussi par des cellules de la synoviale vieillissant prématurément dont les systèmes de nettoyage mitochondrial défaillants les maintiennent dans un mode destructeur. Une protéine « écriteuse » moléculaire, METTL3, accélère ce processus en déstabilisant l’ARN de PINK1, un gardien clé de la santé mitochondriale. Réduire l’activité de METTL3 ou augmenter PINK1 a permis de restaurer des mitochondries plus propres et plus efficaces, d’apaiser le comportement sénescent et de protéger le cartilage dans des modèles expérimentaux. Bien que ces résultats doivent encore être validés chez l’être humain, ils ouvrent la voie à une nouvelle stratégie thérapeutique : au lieu de se contenter de masquer la douleur ou de remplacer les tissus endommagés, on pourrait ralentir l’arthrose de l’ATM en reprogrammant la manière dont les cellules synoviales vieillissent et entretiennent leurs centrales énergétiques internes.
Citation: Tian, K., Du, Q., Guo, J. et al. METTL3-mediated fibroblast-like synoviocytes senescence promotes temporomandibular joint osteoarthritis progression. Commun Biol 9, 510 (2026). https://doi.org/10.1038/s42003-026-09773-x
Mots-clés: arthrose de l’articulation temporo-mandibulaire, sénescence cellulaire, mitophagie, METTL3, PINK1