Clear Sky Science · ar
تقدّم هشاشة المفصل الفكي الصدغي بفعل الشيخوخة المشابهة للليفية للخلايا الزليلية الوسيطة بواسطة METTL3
لماذا يهم تآكل مفصل الفك
قد تكون طقطقة أو ألم أو تيبس في الفك أكثر من مجرد إزعاج؛ لدى كثيرين تشير هذه الأعراض إلى هشاشة مفصل الفك الصدغي، اضطراب مؤلم ناجم عن تآكل المفصل. تبحث هذه الدراسة تحت سطح المفصل لتطرح سؤالاً بسيطاً لكنه مهم: لماذا يبدأ الغضروف الواقي في الفك بالانهيار، وهل يمكن أن يساعد إبطاء نوع معين من شيخوخة الخلايا في حمايته؟ يكشف الباحثون سلسلة جزيئية داخل خلايا بطانة المفصل قد تفتح الباب لعلاجات أكثر دقة وأقل اجتياحاً من الأدوية أو الجراحة الحالية.
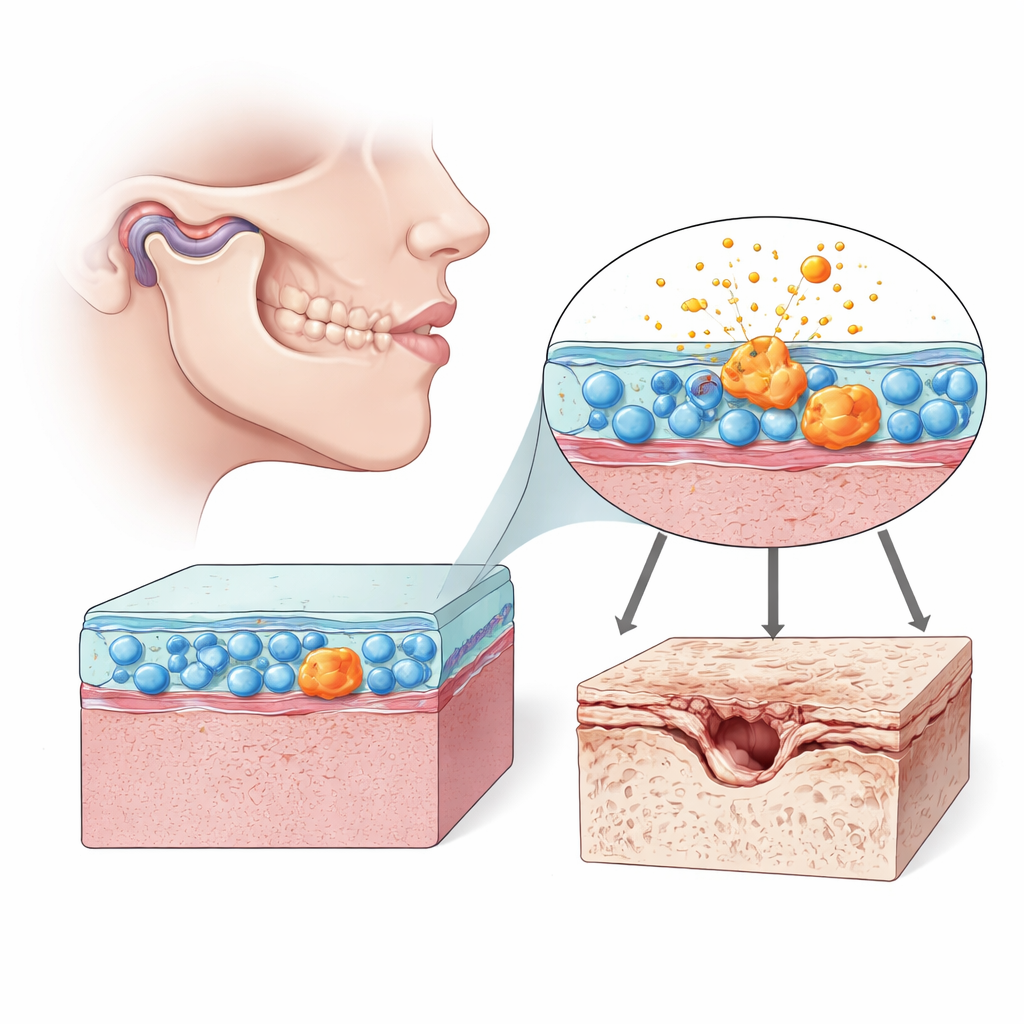
خلايا تساهم بهدوء في صحة المفاصل
داخل كل مفصل متحرك غشاء رقيق يُسمى الزليل، مملوء بخلايا شبيهة بالليف تسمى الخلايا الزليلية الليفية—خلايا تساعد على تزييت وتغذية المفصل. في مفصل الفك الصدغي، تساعد هذه الخلايا في الحفاظ على قرص صغير وسطوح الغضروف على انزلاق سلس أثناء المضغ والكلام. لكن عندما تختل وظيفة هذه الخلايا الزليلية، يمكنها أن تُمطر المفصل بجزيئات التهابية وإنزيمات تهاجم الغضروف. ركز المؤلفون على سلوك هذه الخلايا في هشاشة مفصل الفك الصدغي عند الفئران وفي مزروعات خلايا بشرية، مع إيلاء اهتمام خاص لعلامات الشيخوخة الخلوية، أو التقدّم في السن الخلوي، وصحة مصانع الطاقة داخلها، الميتوكوندريا.
عندما تتقدم خلايا بطانة المفصل في العمر قبل أوانها
باستخدام مادة كيميائية لإحداث هشاشة مفصل الفك الصدغي في الفئران، أكد الفريق سمات كلاسيكية للمرض: خشونة العظم تحت الغضروف، ترقق الغضروف، زيادة حساسية الألم، ومستويات أعلى من المرسلات الالتهابية. في بطانة المفصل أظهرت العديد من الخلايا الزليلية مؤشرات الشيخوخة—خلايا توقفت عن الانقسام لكنها تظل نشطة أيضياً ومشتعلة بالالتهاب. كانت لهذه الخلايا المسنة أنظمة تنظيف داخلية بطيئة وميتوكوندريا تالفة. عندما عزل الباحثون هذه الخلايا الزليلية وزرعواها مع خلايا غضروف بشرية، بدأت خلايا الغضروف بإنتاج إنزيمات تفكك أكثر وكولاجين بنيوي أقل، مما يدل على أن الخلايا الزليلية المسنة يمكن أن تُحدث تلف الغضروف مباشرة.
تعطل نظام التنظيف الخلوي ومفتاح جزيئي مهم
تقوم الخلايا الصحية باستمرار بإعادة تدوير الميتوكوندريا البالية عبر عملية تسمى تحلل الميتوكوندريا (mitophagy)، ما يمنع تراكم الأجزاء المعطوبة. في كل من الخلايا الزليلية للفئران والبشر التي دُفعت إلى حالة مسنة، كان تحلل الميتوكوندريا ضعيفاً: تراكمت ميتوكوندريا تالفة، انخفض الجهد الغشائي الميتوكوندري، وتراجعت البروتينات المرتبطة بإعادة تدوير الميتوكوندريا. أدخل دواء يعزز تحلل الميتوكوندريا عكس جزئياً هذه السمات الشيخوخية، ما يشير إلى أن ضعف تنظيف الميتوكوندريا يساعد على حبْس هذه الخلايا في حالة مسنة ضارة. ثم ركز الفريق على بروتين يسمى METTL3، الذي يضيف علامة كيميائية (m6A) إلى جزيئات الرنا ويمكنه تغيير مدة بقاء رسائلها داخل الخلية. كانت مستويات METTL3 مرتفعة في المفاصل المريضة وفي الخلايا الزليلية المسنة، إلى جانب علامات m6A العامة.
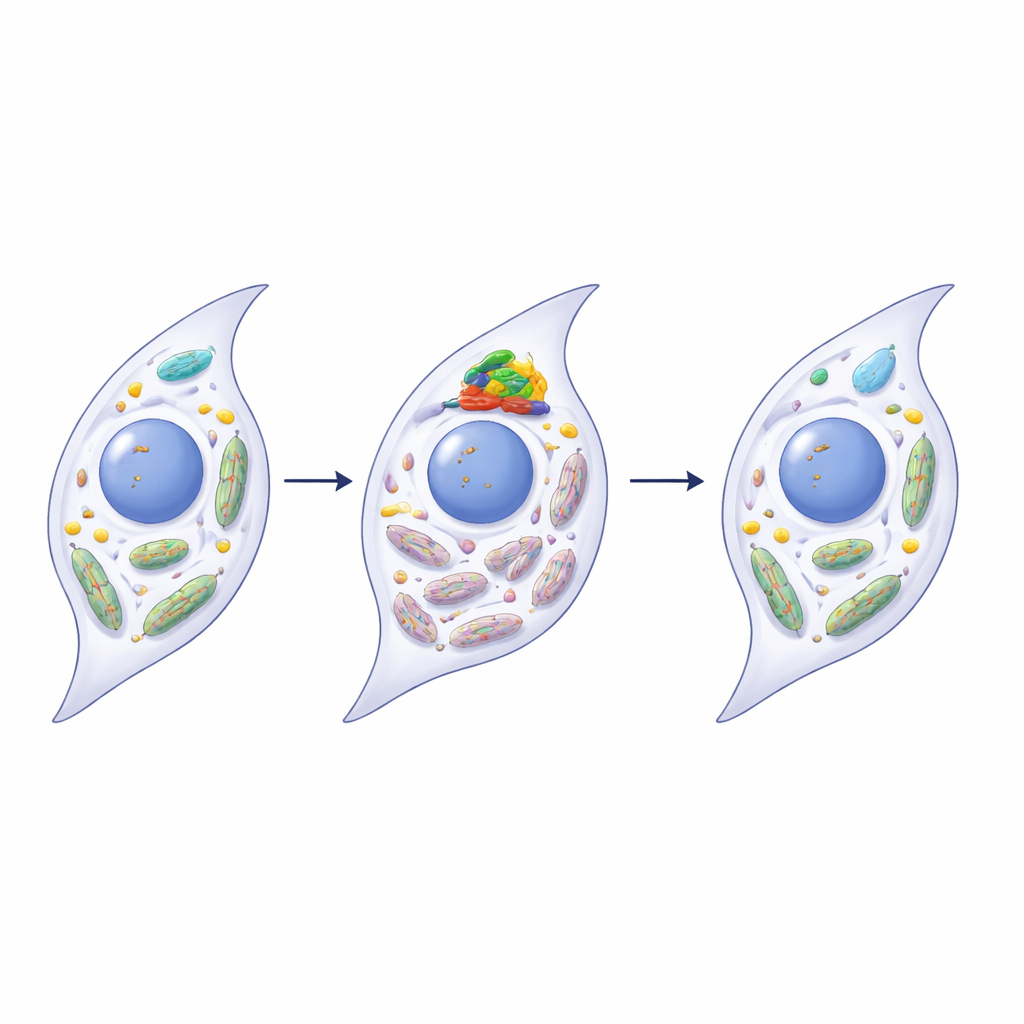
إنقاذ صحة الميتوكوندريا عبر PINK1
اكتشف الباحثون أن METTL3 يؤثر مباشرة على بروتين مراقبة جودة الميتوكوندريا المسمى PINK1، وهو لاعب مركزي في تحلل الميتوكوندريا. في المفاصل المريضة وفي الخلايا الزليلية المسنة، كانت الرنا الخاصة بـPINK1 تحمل مزيداً من علامات m6A وأصبحت أقل استقراراً، ما خفّض مستويات بروتين PINK1. عندما قمع الباحثون METTL3 في خلايا زليلية بشرية، فقدت رنا PINK1 بعض هذه العلامات، ودامت لفترة أطول، وأنتجت مزيداً من بروتين PINK1. هذا بدوره أعاد تحلل الميتوكوندريا، وحسّن وظيفة الميتوكوندريا، وقلّل من علامات الشيخوخة والالتهاب المتعددة. كان لزيادة تعبير PINK1 وحده آثار متجددة مشابهة، بينما أخَّمَد حجب PINK1 فوائد قمع METTL3، رابطاً هذه الخطوات في مسار واحد من تعديل الرنا إلى إصلاح الميتوكوندريا.
من شيخوخة الخلايا إلى تلف مفصل الفك
لاختبار ما إذا كانت هذه الخلايا الزليلية المسنة قد تضر المفصل في كائن حي، حقن الفريق إما خلايا زليلية طبيعية أو مسنة في مفاصل فك فئران صحية. طورت المفاصل التي تلقت الخلايا المسنة سريعاً سمات هشاشة المفصل: فقدان جودة العظم تحت الغضروف، أسطح غضروفية خشنة ومرققة، زيادة حساسية الألم، مستويات أعلى من البروتينات الالتهابية، وتراجعات واضحة في علامات تحلل الميتوكوندريا. ربطت هذه التجربة التغيرات الجزيئية داخل الخلايا الزليلية بتدهور المفصل الكامل والألم.
ماذا يعني هذا لرعاية مفاصل الفك في المستقبل
بعبارات بسيطة، تقترح الدراسة أن هشاشة مفصل الفك الصدغي يغذيها ليس الضغط الميكانيكي وحده، بل خلايا بطانة المفصل التي تتقدم في العمر مبكراً والتي يبقيها تعطل تنظيف الميتوكوندريا محبوسة في نمط مدمر. يسرّع بروتين «الكاتب» الجزيئي METTL3 هذه العملية عبر زعزعة استقرار رنا PINK1، الحارس الأساسي لصحة الميتوكوندريا. إخماد METTL3 أو تعزيز PINK1 أعاد ميتوكوندريا أنظف وأكثر كفاءة، هدأ سلوكيات الشيخوخة، وحمى الغضروف في النماذج التجريبية. وبينما لا تزال هذه النتائج بحاجة إلى التحقق منها في المرضى البشر، فإنها تشير إلى نوع جديد من العلاجات: بدل أن نكتفي بتخفيف الألم أو استبدال الأنسجة التالفة، قد نتمكن من إبطاء هشاشة مفصل الفك عن طريق إعادة برمجة كيفية شيخوخة الخلايا الزليلية وصيانتها لمصانع طاقتها الداخلية.
الاستشهاد: Tian, K., Du, Q., Guo, J. et al. METTL3-mediated fibroblast-like synoviocytes senescence promotes temporomandibular joint osteoarthritis progression. Commun Biol 9, 510 (2026). https://doi.org/10.1038/s42003-026-09773-x
الكلمات المفتاحية: هشاشة مفصل الفك الصدغي, الشيخوخة الخلوية, تحلل الميتوكوندريا بالتوبيخ, METTL3, PINK1