Clear Sky Science · pt
Senescência de sinoviócitos do tipo fibroblasto mediada por METTL3 promove a progressão da osteoartrite da articulação temporomandibular
Por que o desgaste da articulação da mandíbula importa
Estalos, dor ou rigidez na mandíbula podem ser mais do que um incômodo; para muitas pessoas, são sinais de osteoartrite da articulação temporomandibular, um distúrbio doloroso de desgaste da articulação da mandíbula. Este estudo investiga o que ocorre abaixo da superfície da articulação para fazer uma pergunta simples, porém importante: por que a cartilagem amortecedora da mandíbula começa a se degradar, e seria possível protegê-la retardando um tipo específico de envelhecimento celular? Os pesquisadores descobriram uma cadeia molecular de eventos nas células que revestem a articulação que pode abrir caminho para tratamentos mais direcionados e menos invasivos do que os medicamentos ou cirurgias atualmente usados.
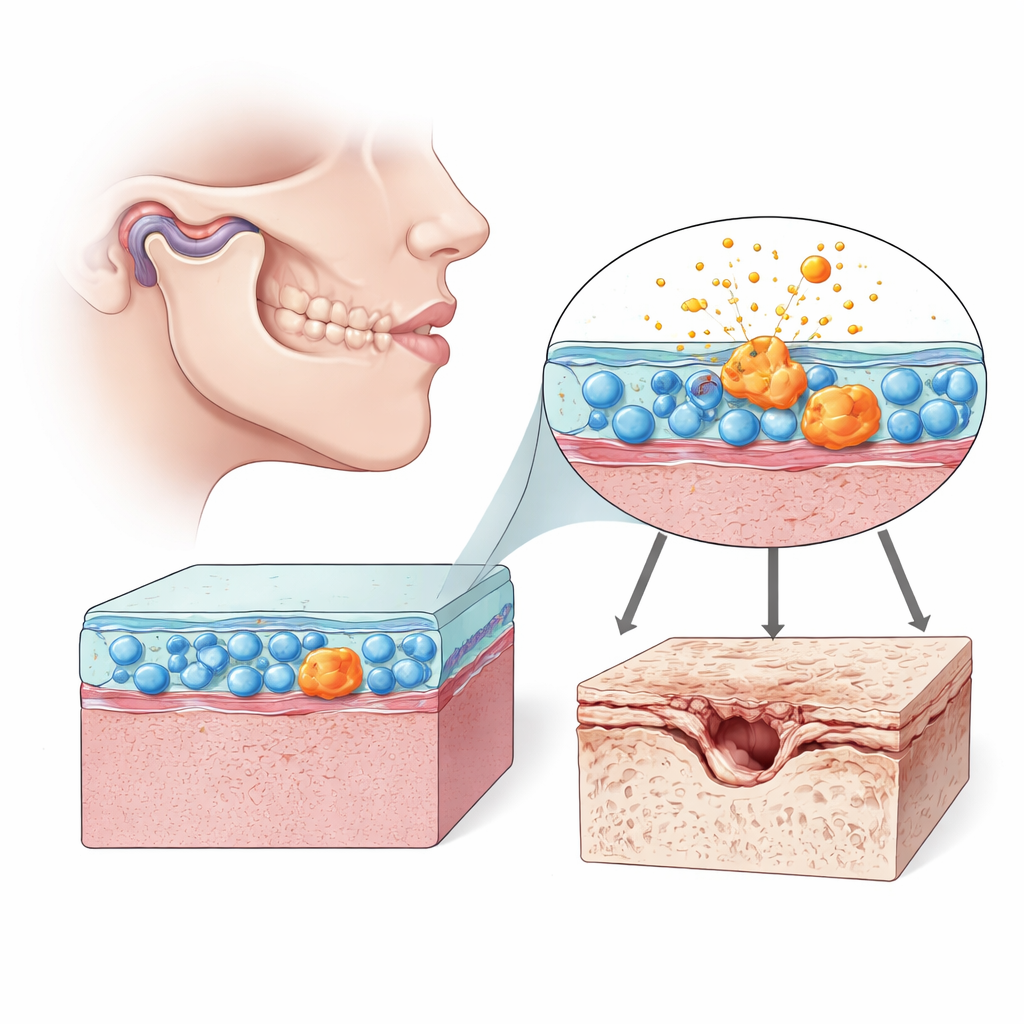
Células que silenciosamente moldam a saúde articular
No interior de toda articulação móvel há um revestimento macio chamado sinóvia, repleto de sinoviócitos do tipo fibroblasto — células que ajudam a lubrificar e nutrir a articulação. Na articulação temporomandibular (ATM), essas células mantêm o pequeno disco e as superfícies cartilaginosas deslizando suavemente enquanto mastigamos e falamos. Mas quando esses sinoviócitos se alteram, podem inundar a articulação com moléculas inflamatórias e enzimas que corroem a cartilagem. Os autores concentraram-se em como essas células se comportam na osteoartrite da ATM em ratos e em culturas de células humanas, dando atenção especial a sinais de envelhecimento celular, ou senescência, e à saúde de suas usinas de energia, as mitocôndrias.
Quando as células do revestimento articular envelhecem antes do tempo
Usando um produto químico para desencadear osteoartrite da ATM em ratos, a equipe confirmou características clássicas da doença: osso rugoso sob a cartilagem, afinamento da cartilagem, maior sensibilidade à dor e níveis elevados de mensageiros inflamatórios. No revestimento articular, muitos sinoviócitos exibiram marcadores de senescência — células que pararam de se dividir, mas permanecem metabolicamente ativas e altamente inflamatórias. Essas células senescentes apresentaram sistemas internos de limpeza lentos e mitocôndrias danificadas. Quando os pesquisadores isolaram esses sinoviócitos e os cultivaram com condrócitos humanos (células da cartilagem), os condrócitos passaram a produzir mais enzimas degradantes e menos colágeno estrutural, mostrando que os sinoviócitos envelhecidos podían diretamente impulsionar o dano à cartilagem.
Limpeza celular comprometida e um interruptor molecular chave
Células saudáveis reciclam constantemente mitocôndrias desgastadas por meio de um processo chamado mitofagia, evitando o acúmulo de componentes defeituosos. Tanto em sinoviócitos de rato quanto humanos induzidos à senescência, a mitofagia estava enfraquecida: mitocôndrias danificadas se acumularam, o potencial de membrana mitocondrial caiu e proteínas ligadas à reciclagem mitocondrial diminuíram. Um fármaco que estimula a mitofagia reverteu parcialmente essas características de envelhecimento, sugerindo que a limpeza mitocondrial deficiente ajuda a manter essas células em um estado senescente e prejudicial. A equipe então concentrou-se numa proteína chamada METTL3, que adiciona uma marca química (m6A) a moléculas de RNA e pode alterar quanto tempo essas mensagens sobrevivem na célula. Os níveis de METTL3 estavam elevados em articulações doentes e em sinoviócitos senescentes, juntamente com um aumento geral das marcas m6A.
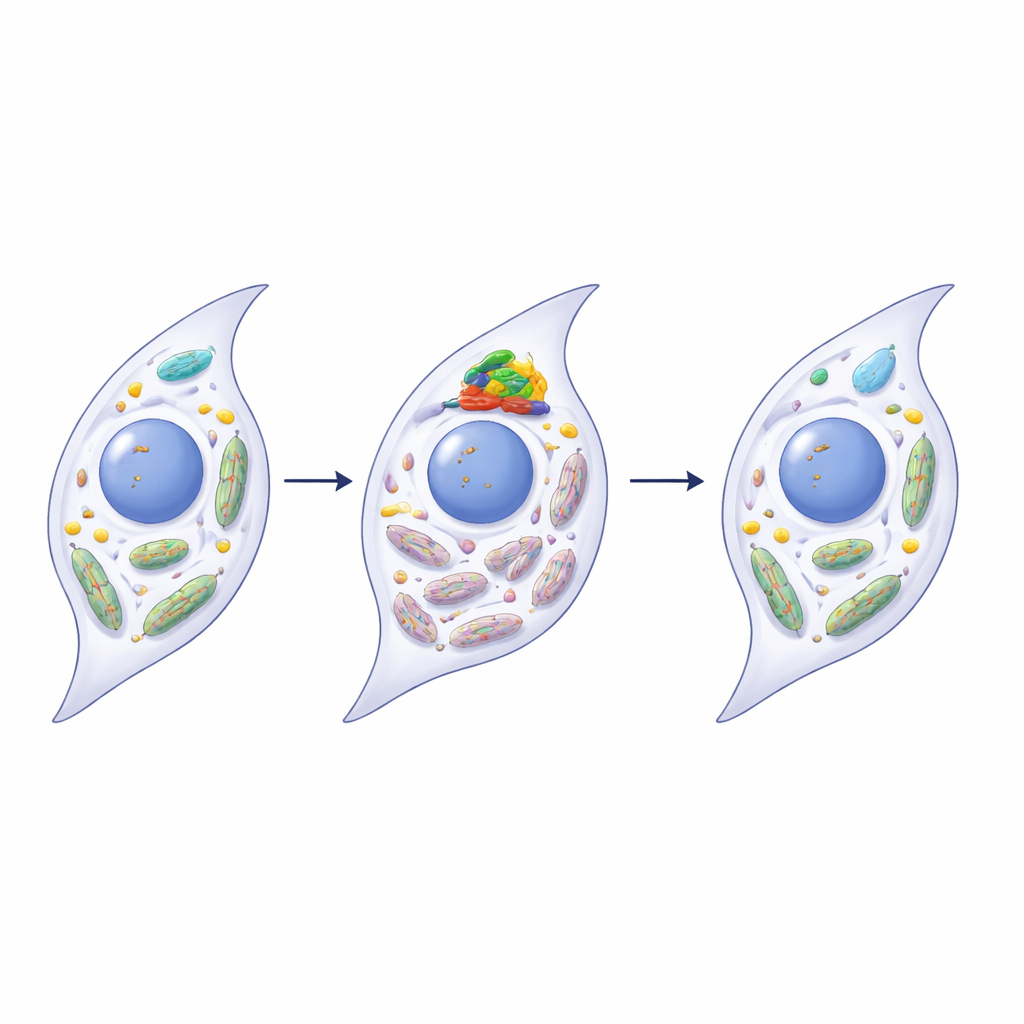
Resgatando a saúde mitocondrial via PINK1
Os pesquisadores descobriram que METTL3 influencia diretamente uma proteína de controle de qualidade mitocondrial chamada PINK1, um elemento central da mitofagia. Em articulações doentes e em sinoviócitos envelhecidos, o RNA de PINK1 apresentava mais marcas m6A e tornava-se menos estável, reduzindo os níveis da proteína PINK1. Quando METTL3 foi silenciado em sinoviócitos humanos, o RNA de PINK1 perdeu parte dessas marcas, sobreviveu por mais tempo e gerou mais proteína PINK1. Isso, por sua vez, restaurou a mitofagia, melhorou a função mitocondrial e reduziu múltiplas características de senescência e inflamação. Superexpressar PINK1 isoladamente teve efeitos rejuvenescedores semelhantes, enquanto bloquear PINK1 atenuou os benefícios do silenciamento de METTL3, conectando essas etapas em uma via única, da modificação do RNA à reparação mitocondrial.
Do envelhecimento celular ao dano da articulação da mandíbula
Para verificar se esses sinoviócitos senescentes poderiam prejudicar uma articulação em um animal vivo, a equipe injetou sinoviócitos normais ou senescentes em articulações mandibulares saudáveis de ratos. As articulações que receberam células senescentes desenvolveram rapidamente características de osteoartrite: perda da qualidade óssea sob a cartilagem, superfícies cartilaginosas rugosas e afinadas, maior sensibilidade à dor, níveis mais altos de proteínas inflamatórias e reduções claras em marcadores de mitofagia. Esse experimento vinculou mudanças moleculares dentro dos sinoviócitos à degeneração articular completa e à dor.
O que isso significa para o cuidado futuro da articulação mandibular
Em termos simples, o estudo sugere que a osteoartrite da ATM é alimentada não apenas pelo estresse mecânico, mas por células do revestimento articular que envelhecem prematuramente e cujos sistemas de limpeza mitocondrial defeituosos as mantêm presas a um modo destrutivo. Uma proteína “escritora” molecular, METTL3, acelera esse processo ao desestabilizar o RNA de PINK1, um guardião chave da saúde mitocondrial. Reduzir METTL3 ou aumentar PINK1 restaurou mitocôndrias mais limpas e eficientes, acalmou o comportamento senescente e protegeu a cartilagem em modelos experimentais. Embora essas descobertas ainda precisem ser validadas em pacientes humanos, elas apontam para um novo tipo de terapia: em vez de apenas mascarar a dor ou substituir tecido danificado, poderíamos retardar a osteoartrite da mandíbula reprogramando como os sinoviócitos envelhecem e mantêm suas usinas internas de energia.
Citação: Tian, K., Du, Q., Guo, J. et al. METTL3-mediated fibroblast-like synoviocytes senescence promotes temporomandibular joint osteoarthritis progression. Commun Biol 9, 510 (2026). https://doi.org/10.1038/s42003-026-09773-x
Palavras-chave: osteoartrite da articulação temporomandibular, senescência celular, mitofagia, METTL3, PINK1