Clear Sky Science · pl
Starzenie się podobnych do fibroblastów synowiocytów zależne od METTL3 przyspiesza postęp choroby zwyrodnieniowej stawu skroniowo‑żuchwowego
Dlaczego zużycie stawu szczękowego ma znaczenie
Klikanie, ból czy sztywność w obrębie szczęki to nie tylko utrudnienie — dla wielu osób są to objawy choroby zwyrodnieniowej stawu skroniowo‑żuchwowego (TMJ), bolesnej choroby zużyciowej stawu szczękowego. Badanie zagląda pod powierzchnię stawu, by postawić proste, lecz istotne pytanie: dlaczego amortyzująca chrząstka w stawie zaczyna się rozpadać i czy spowolnienie określonego rodzaju starzenia komórek mogłoby ją chronić? Naukowcy odsłaniają łańcuch molekularnych wydarzeń w komórkach wyściełających staw, który może otworzyć drogę do bardziej ukierunkowanych, mniej inwazyjnych terapii niż obecne leki czy operacje.
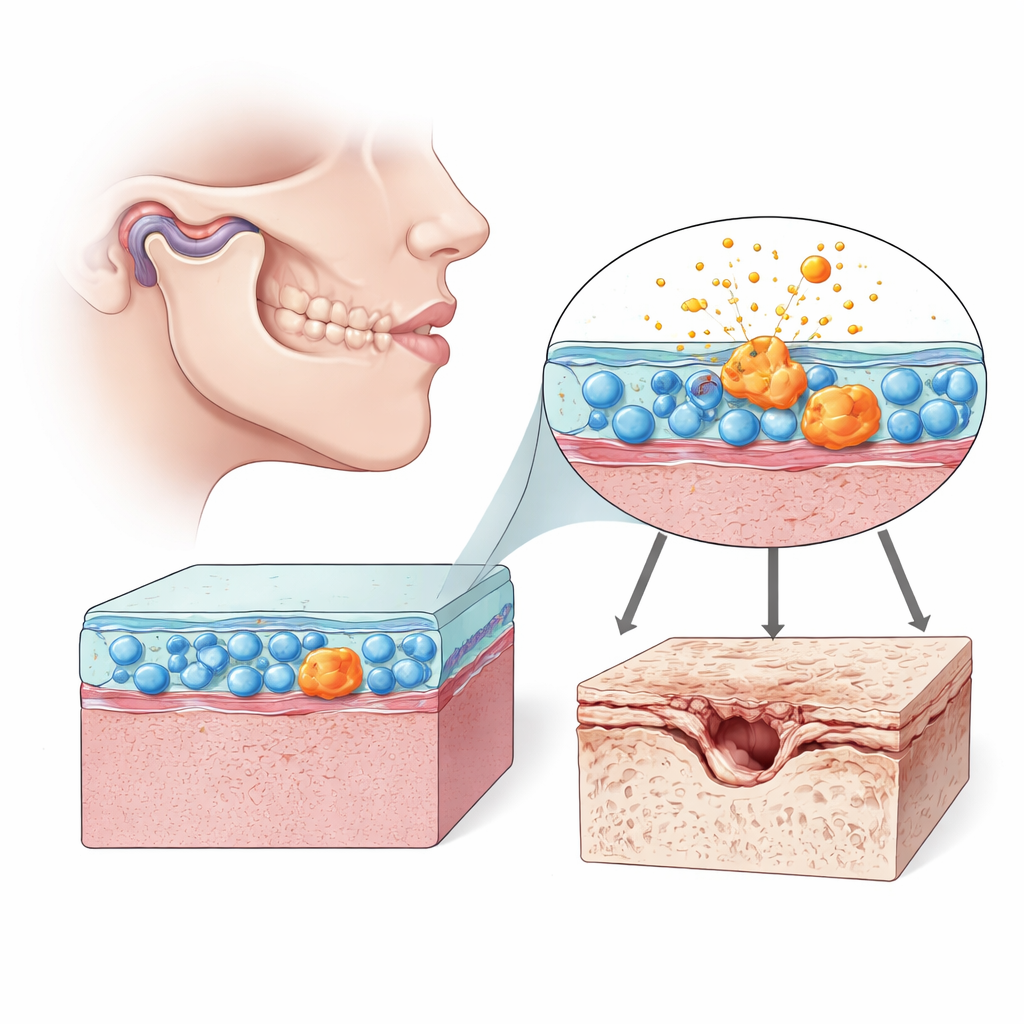
Komórki, które dyskretnie kształtują zdrowie stawu
W każdym ruchomym stawie znajduje się miękka wyściółka zwana błoną maziową, wypełniona komórkami podobnymi do fibroblastów — synowiocytami — które pomagają smarować i odżywiać staw. W stawie skroniowo‑żuchwowym komórki te utrzymują gładkie ślizganie się niewielkiego dysku i powierzchni chrząstki podczas żucia i mówienia. Gdy jednak synowiocy się „rozregulują”, mogą zalewać staw cząsteczkami zapalnymi i enzymami rozkładającymi chrząstkę. Autorzy skoncentrowali się na zachowaniu tych komórek w TMJ u szczurów oraz w hodowlach komórek ludzkich, zwracając szczególną uwagę na oznaki starzenia komórkowego (senescencji) i stan mitochondriów — ich „elektrowni”.
Kiedy komórki wyściełające staw starzeją się przedwcześnie
Używając związku chemicznego do wywołania TMJ u szczurów, zespół potwierdził typowe cechy choroby: postrzępione kości pod chrząstką, przerzedzenie chrząstki, zwiększoną wrażliwość na ból oraz wyższe poziomy mediatorów zapalnych. W błonie maziowej wiele synowiocytów wykazywało markery senescencji — komórki, które przestały się dzielić, lecz pozostają metabolicznie aktywne i wysoce zapalne. Te senescentne komórki miały spowolnione wewnętrzne systemy oczyszczania i uszkodzone mitochondria. Gdy badacze wyizolowali te komórki i hodowali je razem z ludzkimi komórkami chrząstki, komórki chrząstki zaczęły produkować więcej enzymów rozkładających i mniej strukturalnego kolagenu, co pokazuje, że „starzejące się” komórki maziowe mogą bezpośrednio powodować uszkodzenie chrząstki.
Zawiedzione komórkowe oczyszczanie i kluczowy przełącznik molekularny
Zdrowe komórki stale recyklingują zużyte mitochondria poprzez proces zwany mitofagią, zapobiegając kumulacji wadliwych elementów. Zarówno w synowiocytach szczurzych, jak i ludzkich wprowadzonych w stan senescencji, mitofagia była osłabiona: uszkodzone mitochondria się kumulowały, potencjał błony mitochondrialnej spadał, a białka związane z recyklingiem mitochondriów malały. Lek pobudzający mitofagię częściowo odwrócił te cechy starzenia, sugerując, że niewydolne „sprzątanie” mitochondriów utrwala komórki w szkodliwym, senescentnym stanie. Zespół przyjrzał się następnie białku METTL3, które dodaje chemiczny znacznik (m6A) do cząsteczek RNA i może zmieniać czas trwania tych komunikatów w komórce. Poziomy METTL3 były podwyższone w chorych stawach i w senescentnych synowiocytach, podobnie jak ogólne oznaczenia m6A.
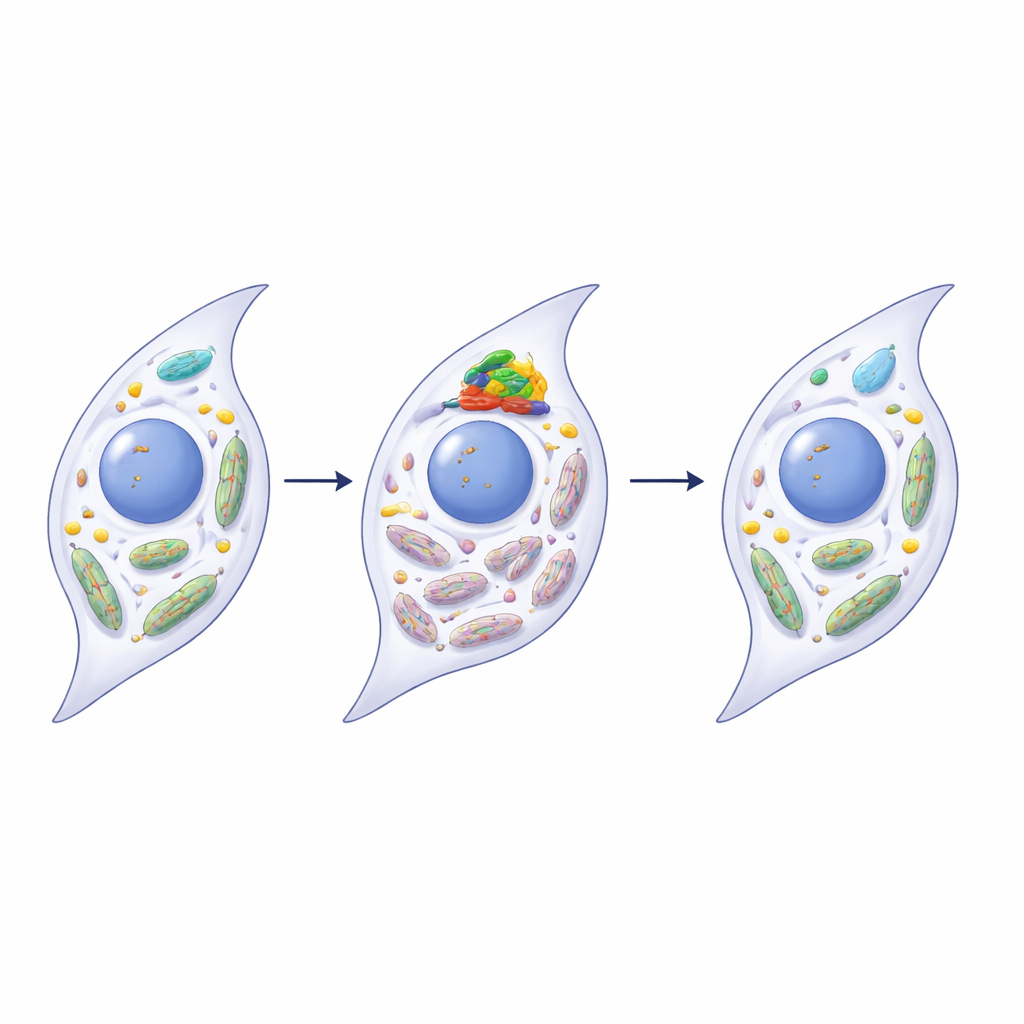
Przywracanie zdrowia mitochondriów przez PINK1
Naukowcy odkryli, że METTL3 wpływa bezpośrednio na białko kontrolujące jakość mitochondriów o nazwie PINK1, kluczowy gracz w mitofagii. W chorych stawach i starzejących się synowiocytach RNA dla PINK1 nosiło więcej znaków m6A i stawało się mniej stabilne, co redukowało poziomy białka PINK1. Gdy METTL3 zostało uciszone w ludzkich synowiocytach, RNA PINK1 utraciło część tych znaków, przetrwało dłużej i wytwarzało więcej białka PINK1. To z kolei przywróciło mitofagię, poprawiło funkcję mitochondriów i zmniejszyło wiele cech senescencji i zapalenia. Nadekspresja samego PINK1 miała podobne odmładzające efekty, zaś zablokowanie PINK1 osłabiło korzyści płynące z uciszenia METTL3, łącząc te kroki w jedną ścieżkę od modyfikacji RNA do naprawy mitochondriów.
Od starzenia komórek do uszkodzenia stawu szczękowego
Aby sprawdzić, czy te starzejące się synowiocy mogą uszkodzić staw w żyjącym organizmie, zespół wstrzyknął do zdrowych stawów szczękowych szczurów albo normalne, albo senescentne synowiocy. Stawy, które otrzymały senescentne komórki, szybko rozwinęły cechy choroby zwyrodnieniowej: pogorszenie jakości kości pod chrząstką, postrzępione i przerzedzone powierzchnie chrząstki, zwiększona wrażliwość na ból, wyższe poziomy białek zapalnych oraz wyraźne obniżenie markerów mitofagii. Ten eksperyment powiązał zmiany molekularne wewnątrz komórek maziowych z pełnoobjawową degeneracją stawu i bólem.
Co to oznacza dla przyszłej opieki nad stawem szczękowym
Mówiąc wprost, badanie sugeruje, że TMJ nie jest napędzany wyłącznie mechanicznym uszkodzeniem, lecz także przedwczesnym starzeniem się komórek wyściełających staw, których uszkodzone systemy oczyszczania mitochondriów utrzymują je w destrukcyjnym trybie. Molekularne „piszące” białko METTL3 przyspiesza ten proces poprzez destabilizację RNA PINK1 — ważnego strażnika zdrowia mitochondriów. Przyciszenie METTL3 lub wzmocnienie PINK1 przywraca czystsze, bardziej wydajne mitochondria, łagodzi zachowania senescentne i chroni chrząstkę w modelach eksperymentalnych. Choć wyniki te wymagają jeszcze potwierdzenia u pacjentów, wskazują na nowy rodzaj terapii: zamiast jedynie tłumić ból czy wymieniać uszkodzone tkanki, moglibyśmy spowolnić chorobę zwyrodnieniową stawu szczękowego, przeprogramowując sposób starzenia się i utrzymania „elektrowni” synowiocytów.
Cytowanie: Tian, K., Du, Q., Guo, J. et al. METTL3-mediated fibroblast-like synoviocytes senescence promotes temporomandibular joint osteoarthritis progression. Commun Biol 9, 510 (2026). https://doi.org/10.1038/s42003-026-09773-x
Słowa kluczowe: choroba zwyrodnieniowa stawu skroniowo‑żuchwowego, starzenie komórkowe, mitofagia, METTL3, PINK1