Clear Sky Science · es
La senescencia de los sinoviocitos tipo fibroblasto mediada por METTL3 promueve la progresión de la artrosis de la articulación temporomandibular
Por qué importa el desgaste de la articulación mandibular
Chasquidos, dolor o rigidez en la mandíbula pueden ser algo más que una molestia; para muchas personas indican artrosis de la articulación temporomandibular, un trastorno doloroso por desgaste de la articulación mandibular. Este estudio examina lo que hay bajo la superficie de la articulación para plantear una pregunta sencilla pero importante: ¿por qué el cartílago amortiguador de la mandíbula comienza a degradarse, y podría protegerse si ralentizamos un tipo concreto de envejecimiento celular? Los investigadores desentrañan una cadena molecular de eventos dentro de las células que recubren la articulación que podría abrir la puerta a tratamientos más dirigidos y menos invasivos que los fármacos o la cirugía actuales.
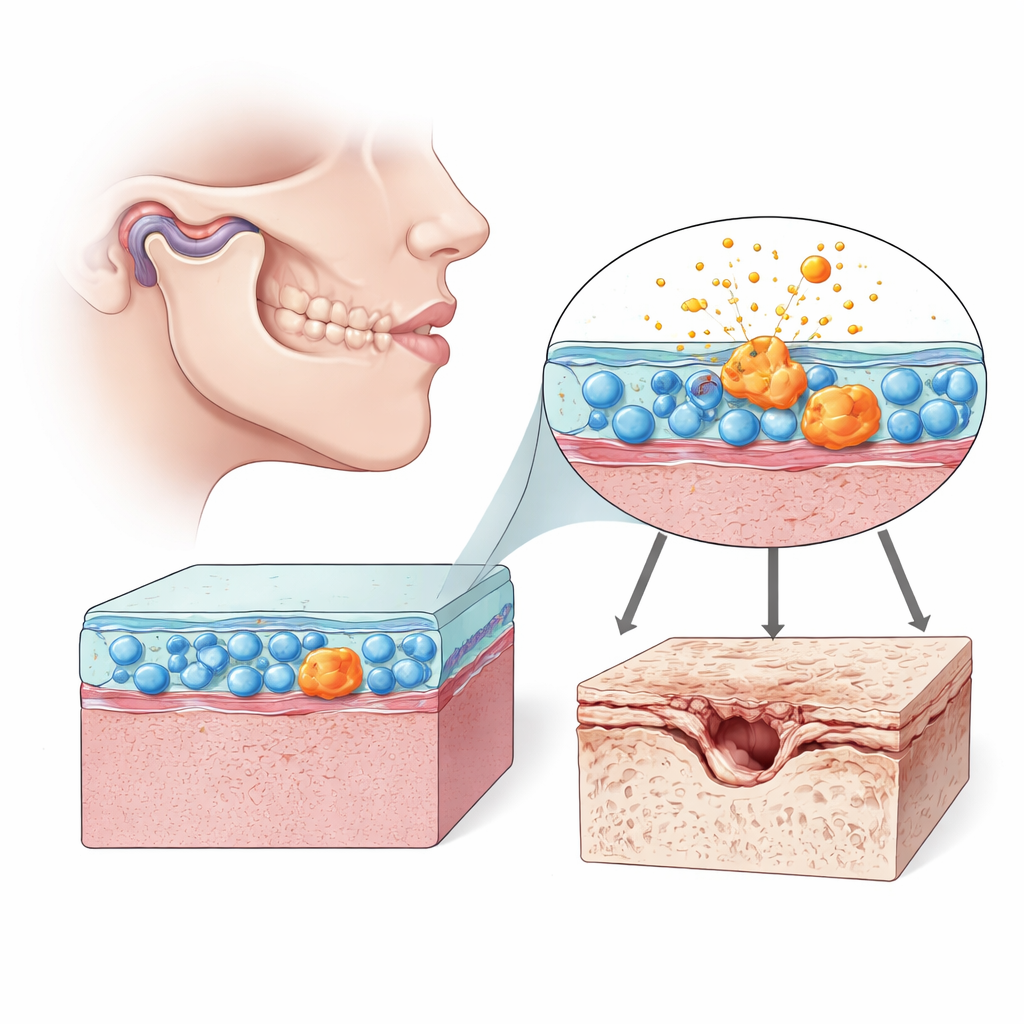
Células que silenciosamente determinan la salud articular
En el interior de cada articulación móvil hay un revestimiento blando llamado sinóvia, repleto de sinoviocitos tipo fibroblasto: células que ayudan a lubricar y nutrir la articulación. En la articulación temporomandibular (ATM), estas células contribuyen a que el pequeño disco y las superficies de cartílago se deslicen con suavidad cuando masticamos y hablamos. Pero cuando estas células sinoviales se descontrolan, pueden inundar la articulación con moléculas inflamatorias y enzimas que degradan el cartílago. Los autores se centraron en cómo se comportan estas células en la artrosis de la ATM en ratas y en cultivos celulares humanos, prestando especial atención a signos de envejecimiento celular, o senescencia, y a la salud de sus centrales energéticas, las mitocondrias.
Cuando las células del revestimiento articular envejecen antes de tiempo
Usando un compuesto químico para inducir artrosis de la ATM en ratas, el equipo confirmó características clásicas de la enfermedad: hueso poroso bajo el cartílago, adelgazamiento del cartílago, mayor sensibilidad al dolor y niveles elevados de mediadores inflamatorios. En el revestimiento articular, muchos sinoviocitos mostraron marcadores de senescencia: células que han dejado de dividirse pero permanecen metabólicamente activas y altamente inflamatorias. Estas células senescentes presentaban sistemas internos de limpieza lentos y mitocondrias dañadas. Cuando los investigadores aislaron estas células sinoviales y las cultivaron junto con condrocitos humanos, las células del cartílago empezaron a producir más enzimas degradativas y menos colágeno estructural, demostrando que los sinoviocitos envejecidos podían impulsar directamente el daño del cartílago.
Una limpieza celular defectuosa y un interruptor molecular clave
Las células sanas reciclan constantemente las mitocondrias desgastadas mediante un proceso llamado mitofagia, evitando la acumulación de componentes defectuosos. En sinoviocitos de rata y humanos forzados a un estado senescente, la mitofagia estaba debilitada: se acumulaban mitocondrias dañadas, bajaba el potencial de membrana mitocondrial y descendían las proteínas asociadas al reciclaje mitocondrial. Un fármaco que potencia la mitofagia revirtió parcialmente estos rasgos de envejecimiento, lo que sugiere que una limpieza mitocondrial deficiente contribuye a fijar a estas células en un estado senescente y dañino. El equipo se centró entonces en una proteína llamada METTL3, que añade una etiqueta química (m6A) a moléculas de ARN y puede alterar la duración de esos mensajes en la célula. Los niveles de METTL3 estaban elevados en articulaciones enfermas y en sinoviocitos senescentes, junto con un aumento global de marcas m6A.
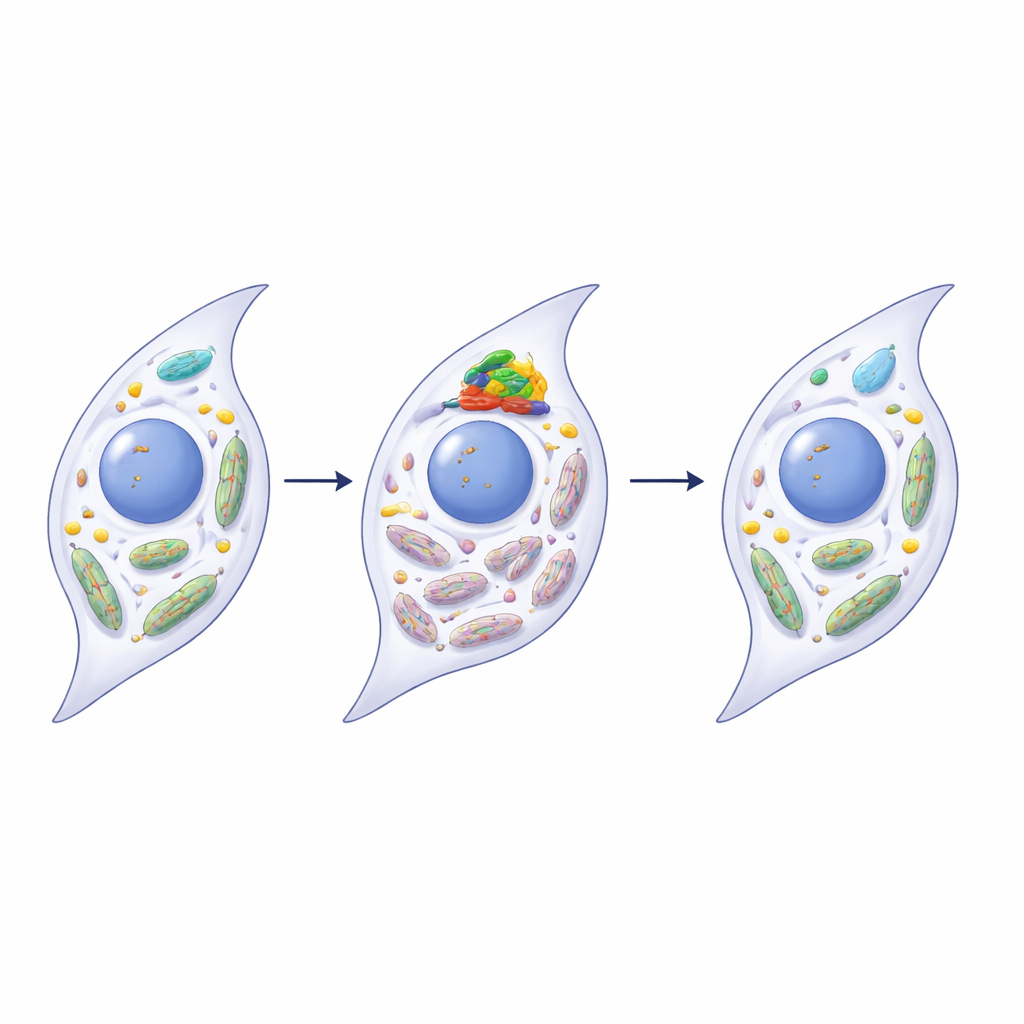
Rescatar la salud mitocondrial a través de PINK1
Los investigadores descubrieron que METTL3 influye directamente en una proteína de control de calidad mitocondrial llamada PINK1, un actor central en la mitofagia. En articulaciones enfermas y en sinoviocitos envejecidos, el ARN de PINK1 presentaba más marcas m6A y se volvía menos estable, reduciendo los niveles de proteína PINK1. Cuando se silenció METTL3 en sinoviocitos humanos, el ARN de PINK1 perdió parte de esas marcas, sobrevivió más tiempo y produjo más proteína PINK1. Esto, a su vez, restauró la mitofagia, mejoró la función mitocondrial y redujo múltiples rasgos de senescencia e inflamación. La sobreexpresión de PINK1 por sí sola tuvo efectos rejuvenecedores similares, mientras que bloquear PINK1 atenuó los beneficios del silenciamiento de METTL3, conectando estos pasos en una vía única desde la modificación del ARN hasta la reparación mitocondrial.
Del envejecimiento celular al daño en la articulación mandibular
Para comprobar si estos sinoviocitos envejecidos podían dañar una articulación en un animal vivo, el equipo inyectó sinoviocitos normales o senescentes en articulaciones mandibulares sanas de rata. Las articulaciones que recibieron células senescentes desarrollaron rápidamente rasgos de artrosis: pérdida de calidad ósea bajo el cartílago, superficies de cartílago ásperas y adelgazadas, mayor sensibilidad al dolor, niveles más altos de proteínas inflamatorias y claras reducciones en marcadores de mitofagia. Este experimento vinculó cambios moleculares dentro de las células sinoviales con una degeneración articular completa y dolor.
Qué significa esto para el cuidado futuro de la articulación mandibular
En términos sencillos, el estudio sugiere que la artrosis de la ATM se alimenta no solo del estrés mecánico, sino de células del revestimiento articular que envejecen prematuramente y cuyos defectuosos sistemas de limpieza mitocondrial las mantienen en un modo destructivo. Una proteína "escritora" molecular, METTL3, acelera este proceso al desestabilizar el ARN de PINK1, un guardián clave de la salud mitocondrial. Reducir METTL3 o potenciar PINK1 restauró mitocondrias más limpias y eficientes, calmó el comportamiento senescente y protegió el cartílago en modelos experimentales. Aunque estos hallazgos deben validarse aún en pacientes humanos, apuntan a una nueva clase de terapia: en lugar de limitarse a enmascarar el dolor o a reemplazar tejido dañado, podríamos frenar la artrosis mandibular reprogramando cómo envejecen las células sinoviales y mantienen sus centrales energéticas.
Cita: Tian, K., Du, Q., Guo, J. et al. METTL3-mediated fibroblast-like synoviocytes senescence promotes temporomandibular joint osteoarthritis progression. Commun Biol 9, 510 (2026). https://doi.org/10.1038/s42003-026-09773-x
Palabras clave: artrosis de la articulación temporomandibular, senescencia celular, mitofagia, METTL3, PINK1