Clear Sky Science · sv
Chromatinaccessibilitetslandskap definierar stromacellidentiteter över vävnader
Varför vävnadernas dolda kod spelar roll
Varje organ i kroppen vet vad det ska göra eftersom dess celler läser genomet på något olika sätt. Denna studie ställer en enkel men kraftfull fråga: kan vi avgöra vilken typ av cell vi tittar på — och från vilket organ den kommer — enbart genom att se vilka delar av dess DNA som är öppna och redo att läsas? Författarna bygger en detaljerad karta över detta ”öppna DNA”-landskap över många musorgan och visar att det tyst registrerar både cellidentitet och vävnadsursprung, med tänkbara tillämpningar inom diagnostik, cancerspårning och regenerativ medicin.
En titt in i öppet DNA i hela kroppen
För att utforska denna dolda kod använde forskarna en teknik kallad single-cell ATAC-seq, som markerar de DNA-avsnitt som är fysiskt tillgängliga i varje kärna. Med frysta prover från nio musorgan, inklusive hjärna, hjärta, lunga, lever, njure, tarm, pankreas, kolon och mjälte, isolerade de kärnorna och profilerade mer än 51 000 enskilda celler. Noggrann finjustering behövdes för varje vävnad så att ömtåliga kärnor från mjuka organ som lunga och hjärna, liksom täta vävnader som hjärta, kunde fångas med hög kvalitet. Efter sekvensering grupperade avancerade beräkningsverktyg cellerna efter hur lika deras åtkomliga DNA-regioner var, och projicerade sedan dessa grupper till tvådimensionella ”kartor” där närstående celler klustrar ihop sig. 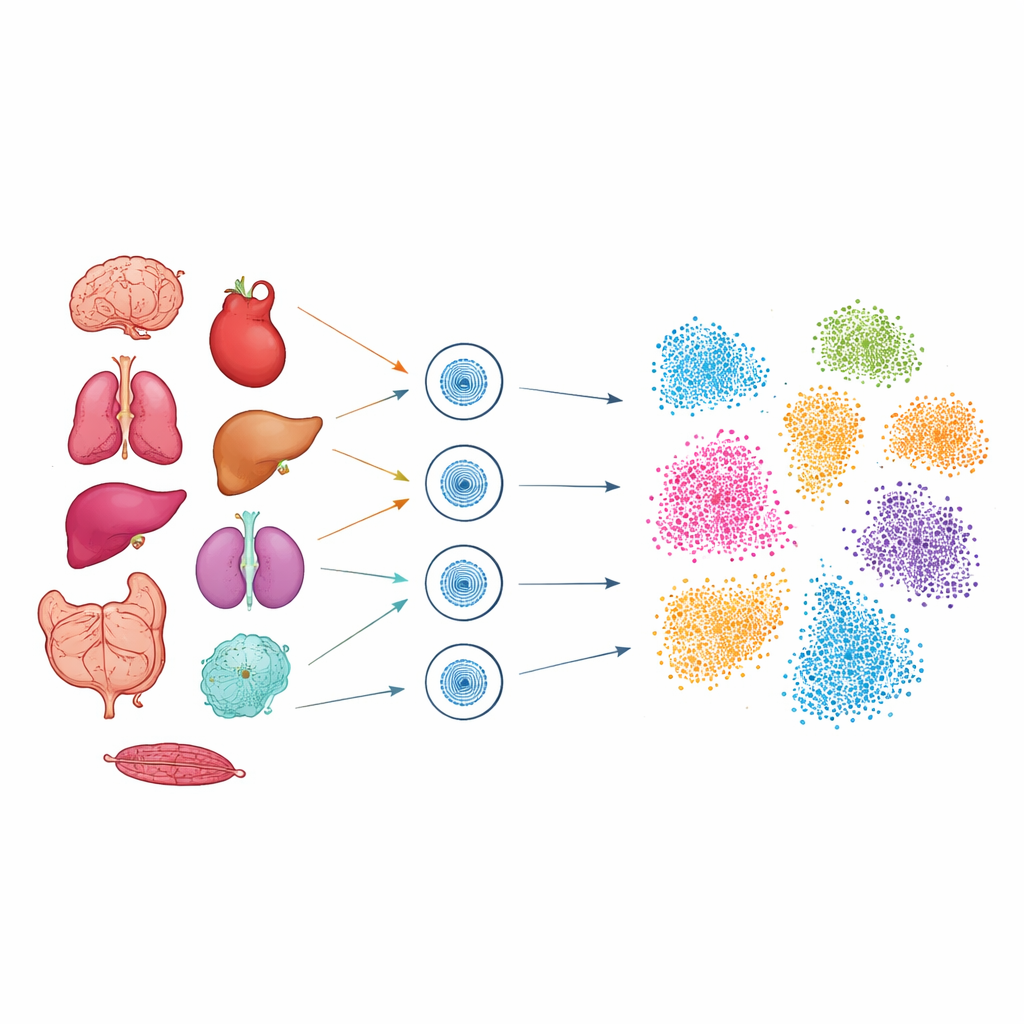
Att känna igen celltyper utifrån deras öppna DNA
Från dessa kartor identifierade teamet 28 huvudsakliga celltyper utspridda över de nio organen, såsom neuroner, kardiomyocyter, immunceller och olika tarm- och leverceller. Även utan att direkt mäta RNA bar varje celltyp ett karaktäristiskt mönster av öppna DNA-toppar kring gener som är viktiga för dess funktion. Till exempel visade T‑celler öppna platser nära gener involverade i immunsignalering, neuroner nära gener nödvändiga för synapser och hjärnaktivitet, och hjärtmuskelceller nära gener kopplade till kontraktion och kalciumhantering. Genom att jämföra sina resultat med stora offentliga referensatlaser bekräftade författarna att de celltyper de fann stämde väl överens med tidigare beskrivna populationer, men nu med ett tillagt lager regulatory detalj: var i genomet kontrollströmbrytarna för dessa celler ligger.
Vävnadsfingeravtryck skrivna i chromatinet
Utöver distinkta celltyper avslöjade studien ett extra organisationslager: celler från samma organ tenderade att dela bredare åtkomlighetsmönster, även när de tillhörde olika typer. Detta var särskilt påtagligt hos ”stromaceller” — stödjeceller som endotelceller, fibroblaster och makrofager som finns i många organ. Även om en endotelcell i hjärtat och en i levern delar en grundläggande identitet, skiljde sig deras öppna DNA-regioner på sätt som speglade deras lokala miljö och uppgifter. I levern var öppna regioner nära gener involverade i avgiftning och metabolism framträdande; i lungendotelet låg öppna regioner nära gener kopplade till gasutbyte och surfaktant; i njuren framhävde åtkomsten gener viktiga för filtrering och jonbalans. Statistiska jämförelser bekräftade att den övergripande likheten i chromatininmönster var högre inom organ än mellan dem.
Inzoomning på kontrollnäten
De öppna DNA-regionerna är inte slumpmässiga — de fungerar som dockningsplatser för transkriptionsfaktorer, de proteiner som slår på eller av gener. Genom att söka efter återkommande sekvensmotif inom åtkomliga regioner kunde författarna härleda vilka transkriptionsfaktorfamiljer som är mest aktiva i olika miljöer. Lungceller visade starka signaturer av Nkx-faktorer som hjälper till att definiera luftvägsidentitet, neuroner var berikade för Rfx-faktorer involverade i hjärnans utveckling, och immunceller bar motiv för regulatorer som Runx1. Footprinting-analyser, som ser hur dessa proteiner skyddar DNA från ATAC‑seq‑enzymet, förstärkte att dessa motiv motsvarar verkliga bindningsevenemang. Tillsammans beskriver mönstren av öppet chromatin och transkriptionsfaktoraktivitet celltyp-specifika regulatoriska program som hjälper till att befästa varje cells roll.
Att spåra stromaceller tillbaka till deras hemorgan
För att testa om chromatininmönster ensamma kunde fungera som en ”returadress” för delade stromaceller grupperade forskarna liknande enskilda celler i kompakta enheter kallade metaceller. Inom makrofager och fibroblaster som hittades i flera organ upptäckte de moduler av öppet DNA som stämde nära överens med vävnadsursprung: mjältmakrofager skiljde sig från levermakrofager, och hjärtfibroblaster från lungfibroblaster, trots att alla tillhörde samma breda cellklass. Endotelceller visade samma princip. Genom att kombinera en generell endotelmarkörregion med en lever‑specifik åtkomlig region kunde teamet tydligt plocka ut leverns sinusoida endotelceller ur blandningen. 
Vad denna atlas betyder för hälsa och sjukdom
I vardagliga termer visar detta arbete att celler inte bara bär en generisk etikett som ”blodkärl” eller ”stödjecell.” Deras DNA är packat på sätt som kommer ihåg vilket organ de tjänar och vilka uppgifter de utför där. Eftersom chromatintillstånd kan bestå när celler rör sig eller omvandlas — till exempel under cancerspridning — kan sådana kartor så småningom hjälpa till att spåra var en tumör började eller skilja skadliga från friska celltillstånd. Atlasen som författarna tillhandahåller är en referens för normala musvävnader, som erbjuder en baslinje mot vilken sjuka eller experimentellt manipulerade celler kan jämföras, och som framhäver hur ett delat genom formas till olika organ genom öppnandet och stängandet av regulatoriskt DNA.
Citering: Nooranikhojasteh, A., Tavallaee, G., Khuu, N. et al. Chromatin accessibility landscapes define stromal cell identities across tissues. Commun Biol 9, 480 (2026). https://doi.org/10.1038/s42003-026-09720-w
Nyckelord: chromatinaccessibilitet, stromaceller, single-cell epigenomik, vävnadsidentitet, genreglering