Clear Sky Science · de
Chromatin- Zugänglichkeit definiert stromale Zellidentitäten in verschiedenen Geweben
Warum der versteckte Code unserer Gewebe wichtig ist
Jedes Organ weiß, was zu tun ist, weil seine Zellen das Genom auf leicht unterschiedliche Weise „lesen“. Diese Studie stellt eine einfache, aber kraftvolle Frage: Lassen sich Art einer Zelle — und aus welchem Organ sie stammt — allein daraus ableiten, welche Bereiche ihrer DNA offen und lesbar sind? Die Autorinnen und Autoren erstellen eine detaillierte Karte dieser „offenen DNA“-Landschaft über viele Mausorgane hinweg und zeigen, dass sie stillschweigend sowohl die Zellidentität als auch das Gewebe der Herkunft dokumentiert, mit möglichen Anwendungen in Diagnostik, Tumornachverfolgung und regenerativer Medizin.
Ein Blick auf offene DNA im ganzen Körper
Um diesen verborgenen Code zu erforschen, verwendeten die Forschenden eine Methode namens Single-Cell ATAC-seq, die die DNA-Abschnitte markiert, die innerhalb jedes Kerns physikalisch zugänglich sind. Mit gefrorenen Proben aus neun Mausorganen — darunter Gehirn, Herz, Lunge, Leber, Niere, Darm, Pankreas, Kolon und Milz — isolierten sie die Kerne und profilierten mehr als 51.000 einzelne Zellen. Für jedes Gewebe war eine sorgfältige Feinabstimmung nötig, damit fragile Kerne aus weichen Organen wie Lunge und Gehirn sowie dichte Gewebe wie das Herz in hoher Qualität erfasst werden konnten. Nach der Sequenzierung gruppierten fortschrittliche Rechenwerkzeuge Zellen nach der Ähnlichkeit ihrer zugänglichen DNA-Regionen und projizierten diese Gruppen in zweidimensionale „Karten“, auf denen verwandte Zellen zusammenklustern. 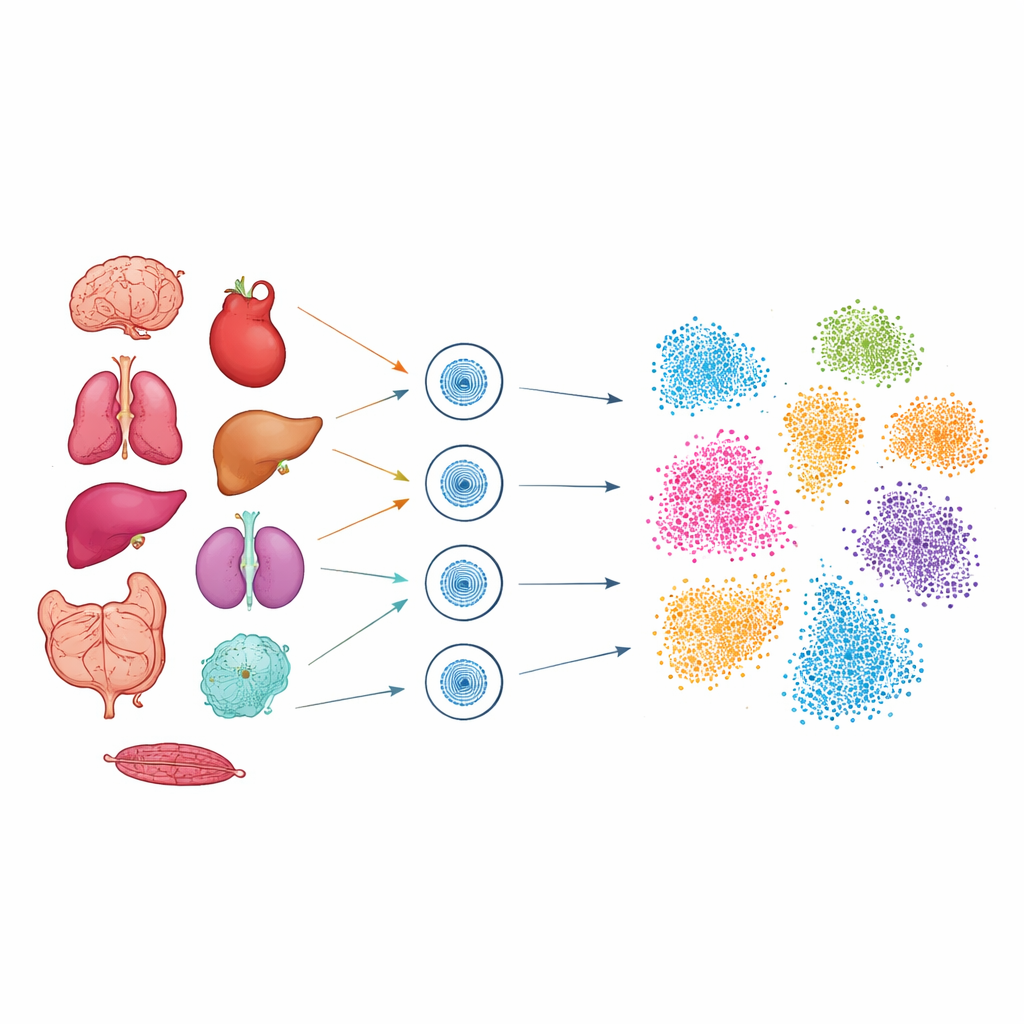
Zelltypen an ihrer offenen DNA erkennen
Aus diesen Karten identifizierte das Team 28 große Zelltypen, verteilt über die neun Organe, etwa Neuronen, Kardiomyozyten, Immunzellen sowie verschiedene Darm- und Leberzellen. Selbst ohne direkte RNA-Messung trug jeder Zelltyp ein charakteristisches Muster offener DNA-Peaks um Gene, die für seine Funktion wichtig sind. Beispielsweise zeigten T‑Zellen offene Stellen in der Nähe von Genen, die an der Immun‑Signalgebung beteiligt sind, Neuronen in der Nähe von Genen für Synapsen und Gehirnaktivität, und Herzmuskelzellen in der Nähe von Genen für Kontraktion und Kalzium‑Regulation. Durch den Vergleich mit großen öffentlichen Referenzatlanten bestätigten die Autorinnen und Autoren, dass die wiedergewonnenen Zelltypen gut mit zuvor beschriebenen Populationen übereinstimmen — nun allerdings mit einer zusätzlichen regulatorischen Ebene: an welchen Stellen im Genom die Schalter für diese Zellen liegen.
Gewebe-Fingerabdrücke in Chromatin
Über die klar unterscheidbaren Zelltypen hinaus enthüllte die Studie eine zusätzliche Organisationsebene: Zellen desselben Organs teilten tendenziell breitere Zugänglichkeitsmuster, selbst wenn sie unterschiedlichen Typen angehörten. Besonders auffällig war dies bei stromalen Zellen — unterstützenden Zellen wie Endothelzellen, Fibroblasten und Makrophagen, die in vielen Organen vorkommen. Obwohl eine Endothelzelle im Herz und eine in der Leber eine gemeinsame Kernidentität besitzen, divergieren ihre offenen DNA‑Regionen in einer Weise, die ihre lokale Umgebung und Aufgaben widerspiegelt. In der Leber waren zugängliche Regionen nahe Genen für Entgiftung und Stoffwechsel prominent; in der Lungenendothelzeile lagen offene Regionen bei Genen für Gasaustausch und Surfactant; in der Niere hoben Zugänglichkeiten Gene hervor, die für Filtration und Ionenbalance wichtig sind. Statistische Vergleiche bestätigten, dass die Gesamtähnlichkeit der Chromatinmuster innerhalb eines Organs höher war als zwischen Organen.
Einblick in die Steuerungsnetzwerke
Die offenen DNA-Regionen sind nicht zufällig — sie dienen als Andockstellen für Transkriptionsfaktoren, die Proteine, die Gene ein- oder ausschalten. Durch die Suche nach wiederkehrenden Sequenzmotiven innerhalb zugänglicher Regionen konnten die Autorinnen und Autoren ableiten, welche Transkriptionsfaktorfamilien in verschiedenen Kontexten besonders aktiv sind. Lungenzellen zeigten starke Signaturen von Nkx‑Faktoren, die bei der Definition der Atemweg‑Identität helfen, Neuronen waren für Rfx‑Faktoren, die an der Gehirnentwicklung beteiligt sind, angereichert, und Immunzellen trugen Motive für Regulatoren wie Runx1. Footprinting‑Analysen, die untersuchen, wie diese Proteine die DNA vor dem ATAC‑seq‑Enzym schützen, untermauerten, dass diese Motive echten Bindungsereignissen entsprechen. Zusammengenommen zeichnen die Muster offener Chromatinbereiche und die Aktivität von Transkriptionsfaktoren zelltypspezifische Regulationsprogramme nach, die dazu beitragen, die Rolle jeder Zelle zu festigen.
Stromale Zellen zu ihrem Herkunftsorgan zurückverfolgen
Um zu testen, ob Chromatinmuster allein als „Rücksendeadresse“ für gemeinsame stromale Zellen dienen können, bündelten die Forschenden ähnliche Einzelzellen in kompakte Einheiten, sogenannte Metazellen. Innerhalb von Makrophagen und Fibroblasten, die in mehreren Organen vorkamen, entdeckten sie Module zugänglicher DNA, die eng mit dem Gewebe der Herkunft übereinstimmten: Milzmakrophagen unterschieden sich von Lebermakrophagen, und Herzfibroblasten von Lungenfibroblasten, obwohl alle zur gleichen breiten Zellklasse gehörten. Endothelzellen zeigten dasselbe Prinzip. Durch die Kombination einer allgemeinen endothelalen Markerlregion mit einer leberspezifischen zugänglichen Region konnte das Team Leber‑sinusoide Endothelzellen klar aus dem Gemisch herausfiltern. 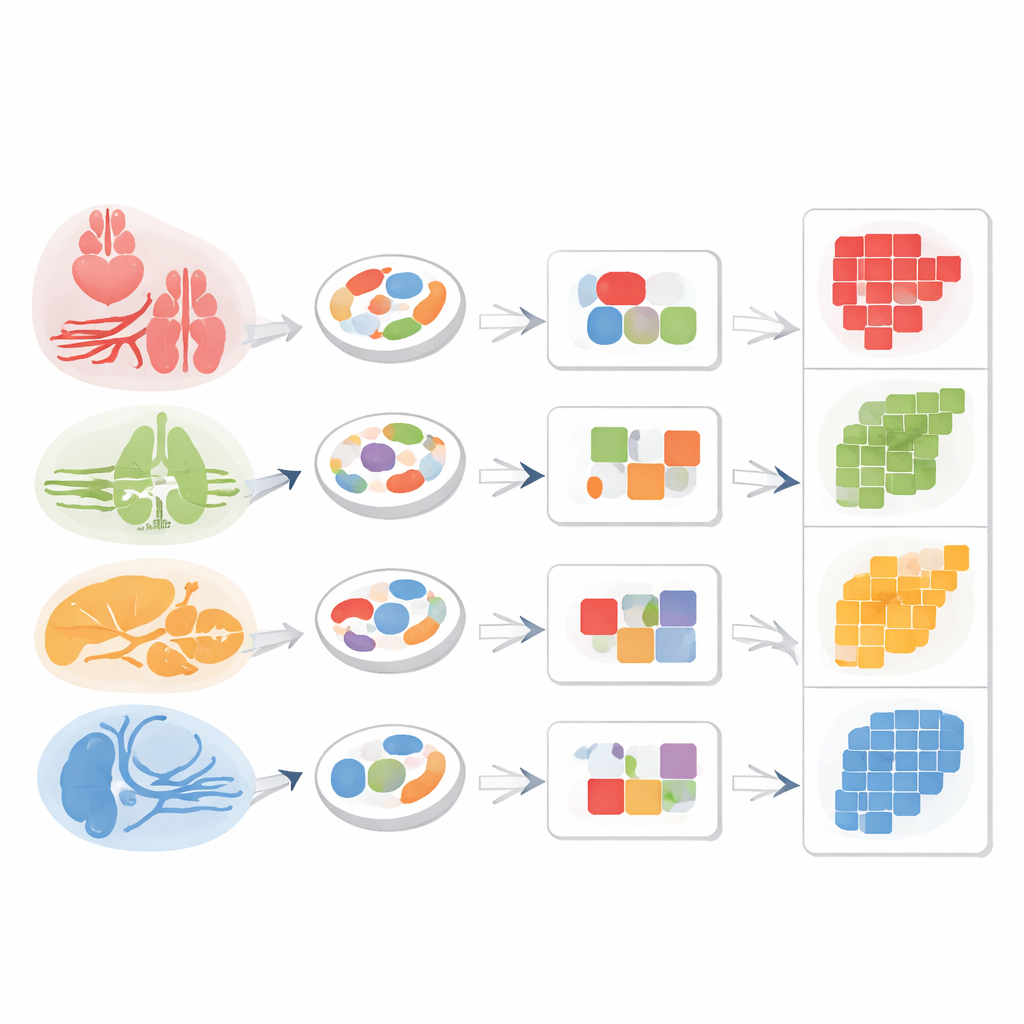
Was dieses Atlaswerk für Gesundheit und Krankheit bedeutet
Alltäglich formuliert zeigt diese Arbeit, dass Zellen nicht nur ein generisches Etikett wie „Blutgefäß“ oder „Stützzelle“ tragen. Ihre DNA ist so verpackt, dass sie sich daran erinnert, welchem Organ sie dienen und welche Aufgaben sie dort erfüllen. Da Chromatinzustände bestehen bleiben können, wenn Zellen wandern oder sich verwandeln — etwa während der Ausbreitung von Krebs — könnten solche Karten schließlich helfen, den Ursprung eines Tumors nachzuverfolgen oder schädliche von gesunden Zellzuständen zu unterscheiden. Der bereitgestellte Atlas ist eine Referenz für normale Mausgewebe, die als Ausgangsbasis dient, um krankhafte oder experimentell veränderte Zellen zu vergleichen, und zeigt, wie ein gemeinsames Genom durch das Öffnen und Schließen regulatorischer DNA in vielfältige Organe geformt wird.
Zitation: Nooranikhojasteh, A., Tavallaee, G., Khuu, N. et al. Chromatin accessibility landscapes define stromal cell identities across tissues. Commun Biol 9, 480 (2026). https://doi.org/10.1038/s42003-026-09720-w
Schlüsselwörter: Chromatinzugänglichkeit, stromale Zellen, Einzelzell-Epigenomik, Gewebeidentität, Genregulation