Clear Sky Science · fr
Les paysages d'accessibilité de la chromatine définissent les identités des cellules stromales à travers les tissus
Pourquoi le code caché de nos tissus importe
Chaque organe du corps sait quoi faire parce que ses cellules lisent le génome de manières légèrement différentes. Cette étude pose une question simple mais puissante : peut-on déterminer quel type de cellule nous observons — et de quel organe elle provient — simplement en regardant quelles régions de son ADN sont ouvertes et prêtes à être lues ? Les auteurs construisent une carte détaillée de ce paysage d’« ADN ouvert » à travers de nombreux organes de souris et montrent qu’il enregistre discrètement à la fois l’identité cellulaire et le tissu d’origine, avec des usages potentiels en diagnostic, traçage des cancers et médecine régénérative.
Observer l’ADN accessible à l’échelle du corps
Pour explorer ce code caché, les chercheurs ont utilisé une technique appelée ATAC-seq unicellulaire, qui marque les segments d’ADN physiquement accessibles à l’intérieur de chaque noyau. Travaillant sur des échantillons congelés provenant de neuf organes de souris, notamment cerveau, cœur, poumon, foie, rein, intestin, pancréas, côlon et rate, ils ont isolé les noyaux et profilé plus de 51 000 cellules individuelles. Un ajustement minutieux a été nécessaire pour chaque tissu afin que les noyaux fragiles d’organes mous comme le poumon et le cerveau, ainsi que les tissus denses comme le cœur, puissent tous être capturés avec une grande qualité. Après le séquençage, des outils computationnels avancés ont groupé les cellules selon la similarité de leurs régions d’ADN accessibles, puis projeté ces groupes en « cartes » bidimensionnelles où les cellules apparentées forment des amas. 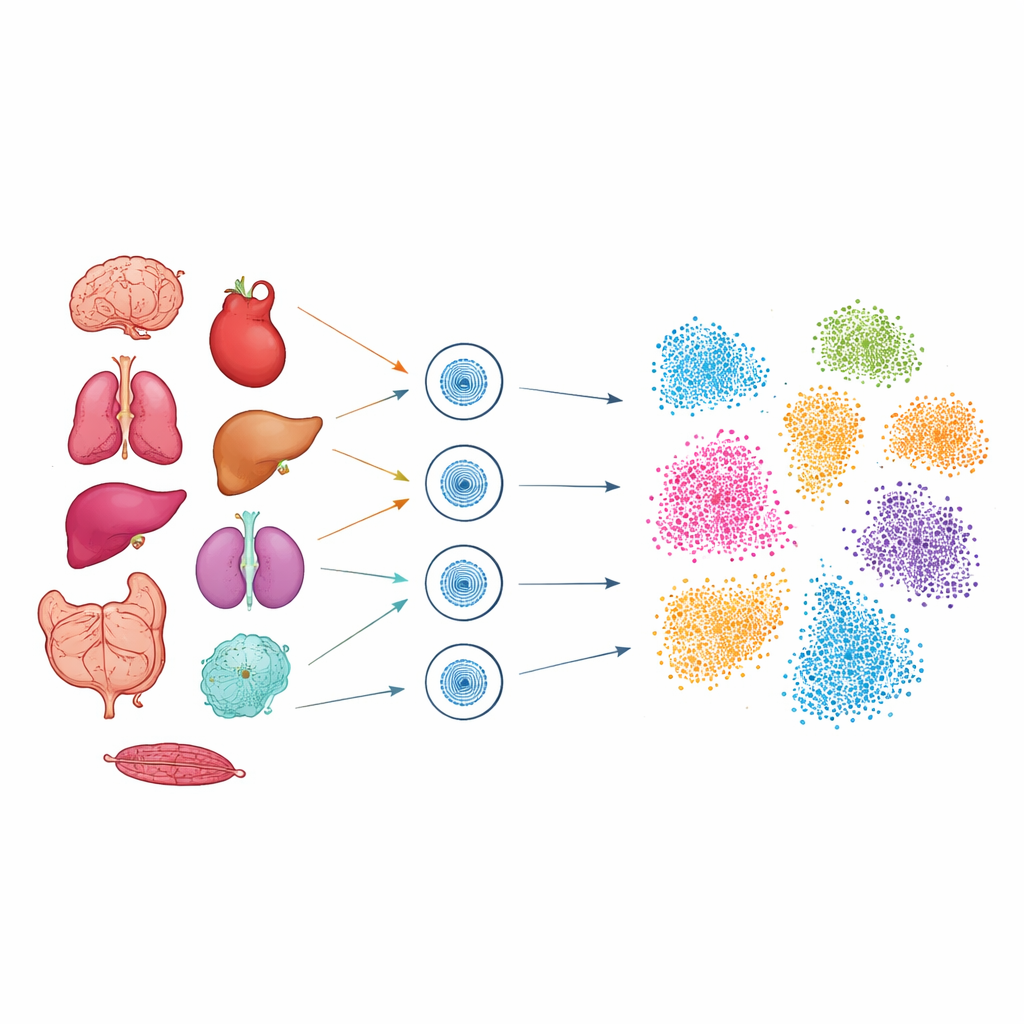
Reconnaître les types cellulaires à partir de leur ADN ouvert
À partir de ces cartes, l’équipe a identifié 28 principaux types cellulaires répartis dans les neuf organes, tels que neurones, cardiomyocytes, cellules immunitaires et diverses cellules intestinales et hépatiques. Même sans mesurer directement l’ARN, chaque type cellulaire présentait un motif caractéristique de pics d’accessibilité autour de gènes connus pour être importants à sa fonction. Par exemple, les lymphocytes T présentaient des sites ouverts près de gènes impliqués dans la signalisation immunitaire, les neurones près de gènes nécessaires aux synapses et à l’activité cérébrale, et les cellules musculaires cardiaques près de gènes liés à la contraction et à la gestion du calcium. En comparant leurs résultats à de grands atlas de référence publics, les auteurs ont confirmé que les types cellulaires qu’ils ont retrouvés correspondaient bien aux populations déjà décrites, mais avec une couche supplémentaire d’information régulatrice : où dans le génome se situent les « interrupteurs » de contrôle pour ces cellules.
Empreintes tissulaires écrites dans la chromatine
Au‑delà des types cellulaires distincts, l’étude a révélé une couche d’organisation supplémentaire : les cellules du même organe avaient tendance à partager des schémas d’accessibilité plus larges, même lorsqu’elles appartenaient à des types différents. Cela était particulièrement frappant pour les cellules « stromales » — cellules de soutien comme les cellules endothéliales, les fibroblastes et les macrophages qui existent dans de nombreux organes. Bien qu’une cellule endothéliale du cœur et une du foie partagent une identité de base, leurs régions d’ADN ouvertes divergent de manière à refléter leur environnement local et leurs fonctions. Dans le foie, les régions accessibles proches de gènes impliqués dans la détoxification et le métabolisme étaient proéminentes ; dans l’endothélium pulmonaire, des régions ouvertes étaient situées près de gènes liés aux échanges gazeux et au surfactant ; dans le rein, l’accessibilité mettait en évidence des gènes importants pour la filtration et l’équilibre des ions. Des comparaisons statistiques ont confirmé que la similarité globale des motifs de chromatine était plus élevée au sein d’un organe que d’un organe à l’autre.
Zoom sur les réseaux de contrôle
Les régions d’ADN accessibles ne sont pas aléatoires — elles servent de sites d’amarrage pour les facteurs de transcription, les protéines qui activent ou répriment les gènes. En recherchant des motifs de séquence récurrents dans ces régions accessibles, les auteurs ont pu déduire quelles familles de facteurs de transcription sont les plus actives selon les contextes. Les cellules pulmonaires montraient de fortes signatures des facteurs Nkx qui contribuent à définir l’identité des voies aériennes, les neurones étaient enrichis pour des facteurs Rfx impliqués dans le développement cérébral, et les cellules immunitaires portaient des motifs pour des régulateurs tels que Runx1. Des analyses de footprinting, qui examinent comment ces protéines protègent l’ADN de l’enzyme ATAC-seq, ont renforcé l’idée que ces motifs correspondent à de véritables événements de liaison. Ensemble, les motifs d’accessibilité de la chromatine et l’activité des facteurs de transcription dessinent des programmes régulateurs spécifiques aux types cellulaires qui aident à verrouiller le rôle de chaque cellule.
Retrouver l’organe d’origine des cellules stromales
Pour tester si les motifs de chromatine seuls pouvaient servir de « adresse de retour » pour des cellules stromales partagées, les chercheurs ont regroupé des cellules similaires en unités compactes appelées métacellules. Parmi les macrophages et les fibroblastes présents dans plusieurs organes, ils ont découvert des modules d’ADN accessible qui s’alignaient étroitement avec le tissu d’origine : les macrophages de la rate différaient des macrophages du foie, et les fibroblastes cardiaques des fibroblastes pulmonaires, bien qu’appartenant tous à la même grande classe cellulaire. Les cellules endothéliales ont montré le même principe. En combinant une région d’accessibilité générale marquant l’endothélium avec une région accessible spécifique au foie, l’équipe a pu isoler de manière propre les cellules endothéliales sinusoidales hépatiques dans le mélange. 
Que signifie cet atlas pour la santé et la maladie
Concrètement, ce travail montre que les cellules ne portent pas seulement une étiquette générique comme « vaisseau sanguin » ou « cellule de soutien ». Leur ADN est empaqueté de façons qui gardent mémoire de l’organe qu’elles servent et des tâches qu’elles y accomplissent. Parce que les états de chromatine peuvent persister lorsque les cellules migrent ou se transforment — par exemple lors de la dissémination d’un cancer — de telles cartes pourraient à terme aider à retracer l’origine d’une tumeur ou à distinguer des états cellulaires nocifs de ceux qui sont sains. L’atlas fourni par les auteurs constitue une référence pour les tissus murins normaux, offrant une base de comparaison pour des cellules malades ou manipulées expérimentalement et soulignant comment un génome partagé est sculpté en organes divers par l’ouverture et la fermeture de l’ADN régulateur.
Citation: Nooranikhojasteh, A., Tavallaee, G., Khuu, N. et al. Chromatin accessibility landscapes define stromal cell identities across tissues. Commun Biol 9, 480 (2026). https://doi.org/10.1038/s42003-026-09720-w
Mots-clés: accessibilité de la chromatine, cellules stromales, épi-génomique unicellulaire, identité tissulaire, régulation génique