Clear Sky Science · ar
مظاهر نفاذية الكروماتين تحدد هُوِيّات الخلايا الداعمة عبر الأنسجة
لماذا يهم الكود الخفي في أنسجتنا
يعرف كل عضو في الجسم ما الذي يجب أن يقوم به لأن خلاياه تقرأ الجينوم بطرق تختلف قليلاً. تطرح هذه الدراسة سؤالًا بسيطًا لكنه قويًا: هل يمكننا تحديد نوع الخلية التي ننظر إليها—ومن أي عضو أتت—فقط برؤية أي أجزاء من حمضها النووي مفتوحة وجاهزة للقراءة؟ بنى المؤلفون خريطة مفصّلة لمشهد «الحمض النووي المفتوح» هذا عبر العديد من أعضاء الفأر وأظهروا أنها تسجل بهدوء كلًا من هوية الخلية ونسيج المنشأ، مع استخدامات محتملة في التشخيص، وتتبع السرطان، والطب التجديدي.
إلقاء نظرة على الحمض النووي المفتوح عبر الجسم
لاستكشاف هذا الكود الخفي، استخدم الباحثون تقنية تُدعى ATAC-seq أحادي الخلية، التي تميِّز المقاطع من الحمض النووي المتاحة ماديًا داخل كل نواة. باستخدام عينات مجمدة من تسعة أعضاء في الفأر، بما في ذلك الدماغ، والقلب، والرئتين، والكبد، والكُلى، والأمعاء، والبنكرياس، والقولون، والطحال، عزلوا النوى وقيَّموا أكثر من 51,000 خلية فردية. تطلّب كل نسيج ضبطًا دقيقًا بحيث تُلتقط النوى الهشة من الأعضاء الطرية مثل الرئة والدماغ، وكذلك الأنسجة الكثيفة مثل القلب، بجودة عالية. بعد التسلسل، جمعت أدوات حاسوبية متقدمة الخلايا بحسب تشابه مناطق الحمض النووي المتاحة لديها، ثم عرضت هذه المجموعات في «خرائط» ثنائية البُعد حيث تتجمع الخلايا ذات الصلة معًا. 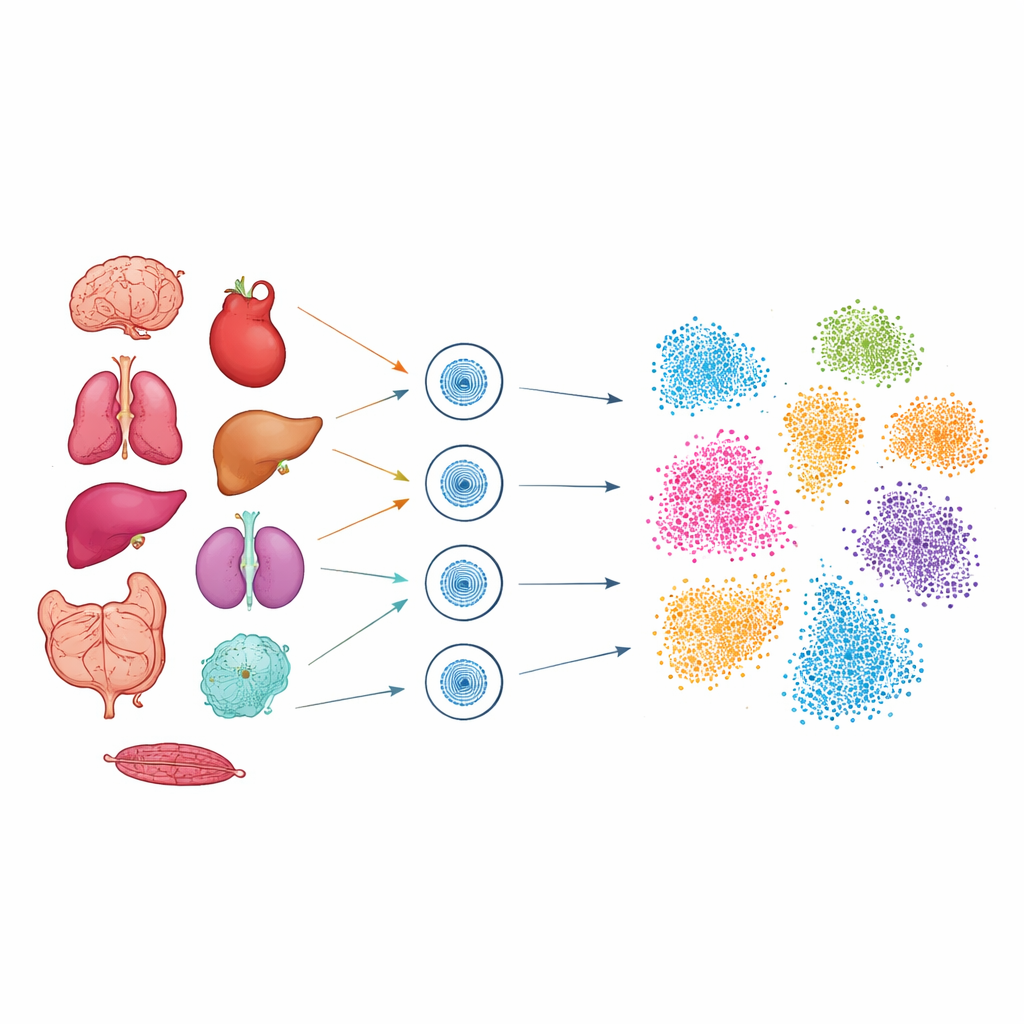
التعرّف على أنواع الخلايا من حمضها النووي المفتوح
من هذه الخرائط، حدَّد الفريق 28 نوعًا رئيسيًا من الخلايا موزعة عبر الأعضاء التسعة، مثل الخلايا العصبية، وخلايا القلب العضلية، وخلايا الجهاز المناعي، ومختلف خلايا الأمعاء والكبد. حتى من دون قياس الـ RNA مباشرة، حمل كل نوع خلية نمطًا مميزًا من قمم النفاذية حول جينات معروفة بأهميتها لوظائفه. على سبيل المثال، أظهرت خلايا T مواقع مفتوحة بالقرب من جينات مشاركة في الإشارات المناعية، والخلايا العصبية بالقرب من جينات مطلوبة للتشابك الوصلي ونشاط الدماغ، وخلايا عضلة القلب بالقرب من جينات مرتبطة بالانقباض والتعامل مع الكالسيوم. بمقارنة نتائجهم مع أطالس مرجعية عامة كبيرة، أكد المؤلفون أن أنواع الخلايا التي استعادوها تطابقت جيدًا مع التجمعات الموصوفة سابقًا، لكن الآن مع طبقة إضافية من التفاصيل التنظيمية: أين في الجينوم تقع مفاتيح التحكم لتلك الخلايا.
بصمات نسيجية مكتوبة في الكروماتين
بعيدًا عن أنواع الخلايا المميزة، كشفت الدراسة طبقة إضافية من التنظيم: تميل الخلايا من نفس العضو إلى مشاركة أنماط أوسع من النفاذية، حتى عندما تنتمي إلى أنواع مختلفة. كان هذا بارزًا بشكل خاص في الخلايا «الداعمة»—الخلايا المساندة مثل الخلايا البطانية، والليفية، والبلعميات التي توجد في العديد من الأعضاء. رغم تشارك خلية بطانية في القلب وأخرى في الكبد بهوية أساسية مشتركة، فإن مناطق الحمض النووي المفتوحة لديهما تتباعد بطرق تعكس بيئتهما المحلية ووظائفهما. في الكبد، كانت المناطق القابلة للوصول قرب جينات مشاركة في إزالة السموم والتمثيل الغذائي بارزة؛ في بطانة الرئة، جلست مناطق مفتوحة بجوار جينات مرتبطة بتبادل الغازات والسطحَيات؛ وفي الكلى، برزت نفاذية قرب جينات مهمة للترشيح وتوازن الأيونات. أكدت المقارنات الإحصائية أن التشابه العام في أنماط الكروماتين كان أعلى داخل الأعضاء منه عبرها.
التدقيق في شبكات التحكم
المناطق المفتوحة من الحمض النووي ليست عشوائية—إنها مواقع ارتكاز لعوامل النسخ، البروتينات التي تشغّل الجينات أو تطفئها. من خلال البحث عن نماذج متكررة في التسلسلات داخل المناطق المتاحة، استطاع المؤلفون استنتاج أي عائلات عوامل النسخ نشطة أكثر في ظروف مختلفة. أظهرت خلايا الرئة توقيعات قوية لعوامل Nkx التي تساعد في تحديد هوية الممرات الهوائية، كانت الخلايا العصبية غنية بعوامل Rfx المشاركة في تطور الدماغ، وحملت الخلايا المناعية أنماطًا لعوامل تنظيمية مثل Runx1. عززت تحليلات «التبصيم»—التي تنظر في كيفية حماية هذه البروتينات لقطع من الحمض النووي من إنزيم ATAC-seq—أن هذه الأنماط تقابل ارتباطات حقيقية. معًا، توضح أنماط الكروماتين المفتوح ونشاط عوامل النسخ برامج تنظيمية خاصة بكل نوع خلية تساهم في تثبيت دور كل خلية.
تتبع الخلايا الداعمة إلى عضوها الأصلي
لاختبار ما إذا كانت أنماط الكروماتين وحدها يمكن أن تعمل كـ«عنوان عودة» للخلايا الداعمة المشتركة، جمع الباحثون الخلايا المفردة المتشابهة في وحدات مُدمجة تُدعى ميتاخلایا (metacells). داخل البلعميات والليفات الموجودة عبر أعضاء متعددة، اكتشفوا وحدات من الحمض النووي القابل للوصول تتماشى عن كثب مع نسيج المنشأ: اختلفت البلعميات الطحالية عن البلعميات الكبدية، والليفات القلبية عن الليفات الرئوية، مع أن جميعها تنتمي إلى نفس الفئة الخلوية الواسعة. أظهرت الخلايا البطانية نفس المبدأ. من خلال دمج منطقة علامة بطانية عامة مع منطقة متاحة خاصة بالكبد، استطاع الفريق تمييز خلايا البطانية الجيبية الكبدية بوضوح من الخليط. 
ماذا يعني هذا الأطلس للصحة والمرض
بعبارة مبسطة، تبين هذه الدراسة أن الخلايا لا تحمل مجرد تسمية عامة مثل «وعاء دموي» أو «خلية داعمة». إن تغليف الحمض النووي لديها يُذكّر بأي عضو تخدمه وما المهام التي تؤديها هناك. ونظرًا لأن حالات الكروماتين يمكن أن تستمر بينما تتحرك الخلايا أو تتغير—على سبيل المثال أثناء انتشار السرطان—فقد تساعد مثل هذه الخرائط في النهاية على تتبع منشأ الورم أو التمييز بين الحالات الخلوية الضارة والصحية. يقدم الأطلس الذي وفره المؤلفون مرجعًا لأنسجة الفأر الطبيعية، ويشكّل خط أساس يمكن مقارنة الخلايا المريضة أو المعالَجة تجريبيًا به، ويسلط الضوء على الكيفية التي يُشكَّل بها جينوم مشترك إلى أعضاء متنوعة عبر فتح وإغلاق الحمض النووي التنظيمي.
الاستشهاد: Nooranikhojasteh, A., Tavallaee, G., Khuu, N. et al. Chromatin accessibility landscapes define stromal cell identities across tissues. Commun Biol 9, 480 (2026). https://doi.org/10.1038/s42003-026-09720-w
الكلمات المفتاحية: نفاذية الكروماتين, الخلايا الداعمة, علم الجينوم أحادي الخلية, هوية النسيج, تنظيم الجينات