Clear Sky Science · sv
Gutmikrobiota-beroende skydd av Lactobacillus reuteri mot njurskada hos hjärndöda råttor
Varför denna forskning är viktig
De flesta njurar som används för transplantation kommer från givare som drabbats av hjärndöd, men dessa organ är ofta skadade redan innan operationen börjar. Denna studie i råttor utforskar en oväntad samarbetspartner i tarmen: en probiotisk bakterie kallad Lactobacillus reuteri. Forskarna visar hur denna mikroorganism kan bidra till att skydda njurarna från skada efter hjärndöd genom att stabilisera tarmfloran, stärka tarmbarriären och dämpa skadliga immunreaktioner som annars skulle försämra organen inför transplantation.
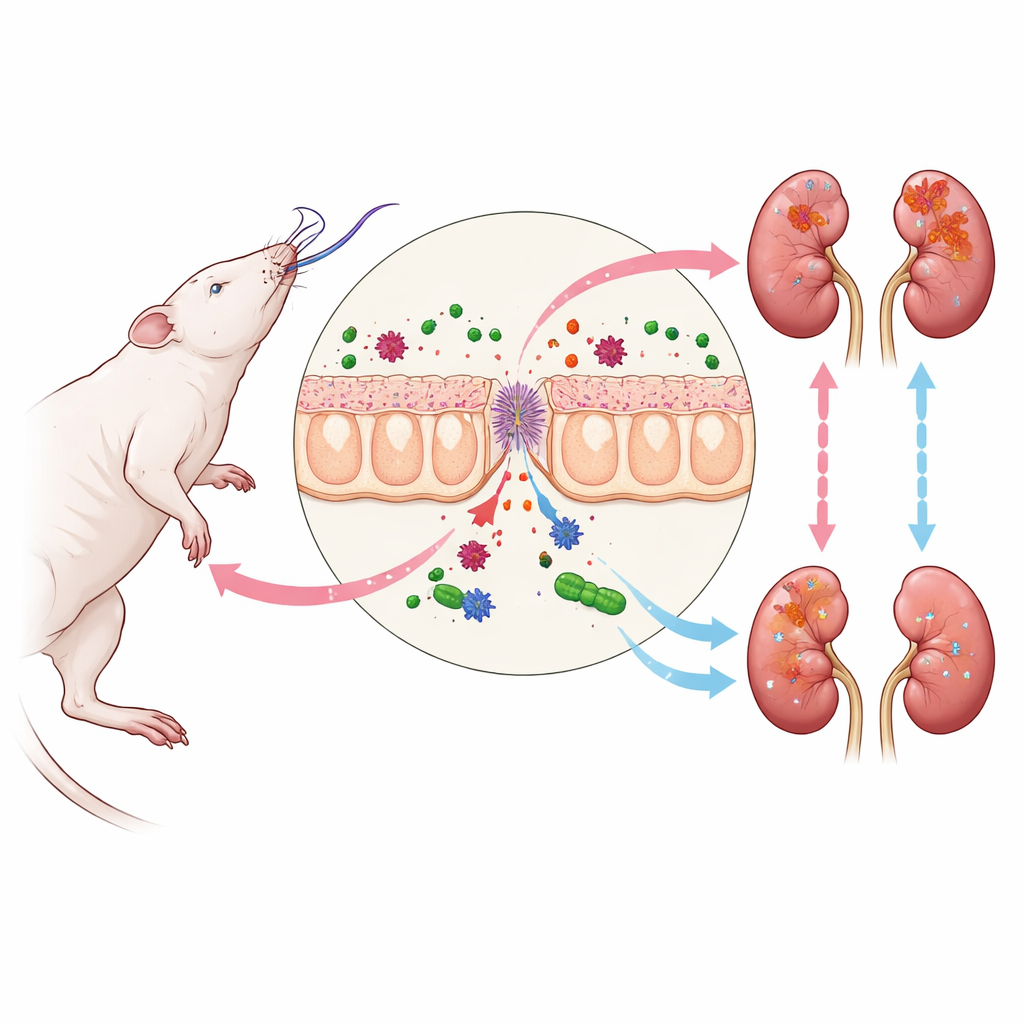
Hjärndöd och kedjereaktionen mot njurarna
När hjärndöd inträffar utsätts kroppen för en storm av hormonella och cirkulatoriska förändringar som sprider sig till många organ. Ett av de första svaga leden är tarmen. Dess skyddande epitel blir läckande, vilket tillåter bakteriella fragment från tarmmikrober att smyga ut i blodomloppet. Bland dessa fragment finns LPS, en komponent i vissa bakteriers cellväggar som starkt aktiverar immunsystemet. När LPS når njurarna binder det till en sensor på njurceller som utlöser TLR4–NF-kappaB-vägen, en signalväg välkänd för att driva inflammation. I den råttmodell som används här ledde denna process till högre nivåer av kreatinin och urea i blodet, ökad uttryckning av njurskademarkören KIM-1 och subtila strukturella skador i njurtubulusceller, även när standardmikroskopiska vyer såg nästan normala ut.
En probiotika omprogrammerar tarmmiljön
Forskargruppen undrade sedan om matning av råttor med Lactobacillus reuteri under en vecka före hjärndöd kunde ändra detta förlopp. De fann att probiotikan omformade tarmens mikrobiella samhälle: skadliga, LPS-rika Proteobacteria minskade, medan Bacteroidota och andra potentiellt gynnsamma grupper blev mer framträdande. Samtidigt förbättrades tarmens fysiska barriär. I ljus- och elektronmikroskop visade de behandlade djuren mer intakta cellförbindelser mellan tarmcellerna och mindre utvidgning av de utrymmen där läckage uppstår. Blodnivåerna av iFABP, en markör för tarmskada och genomsläpplighet, sjönk mot normala nivåer, vilket indikerar en tätare och mer selektiv tarmvägg.
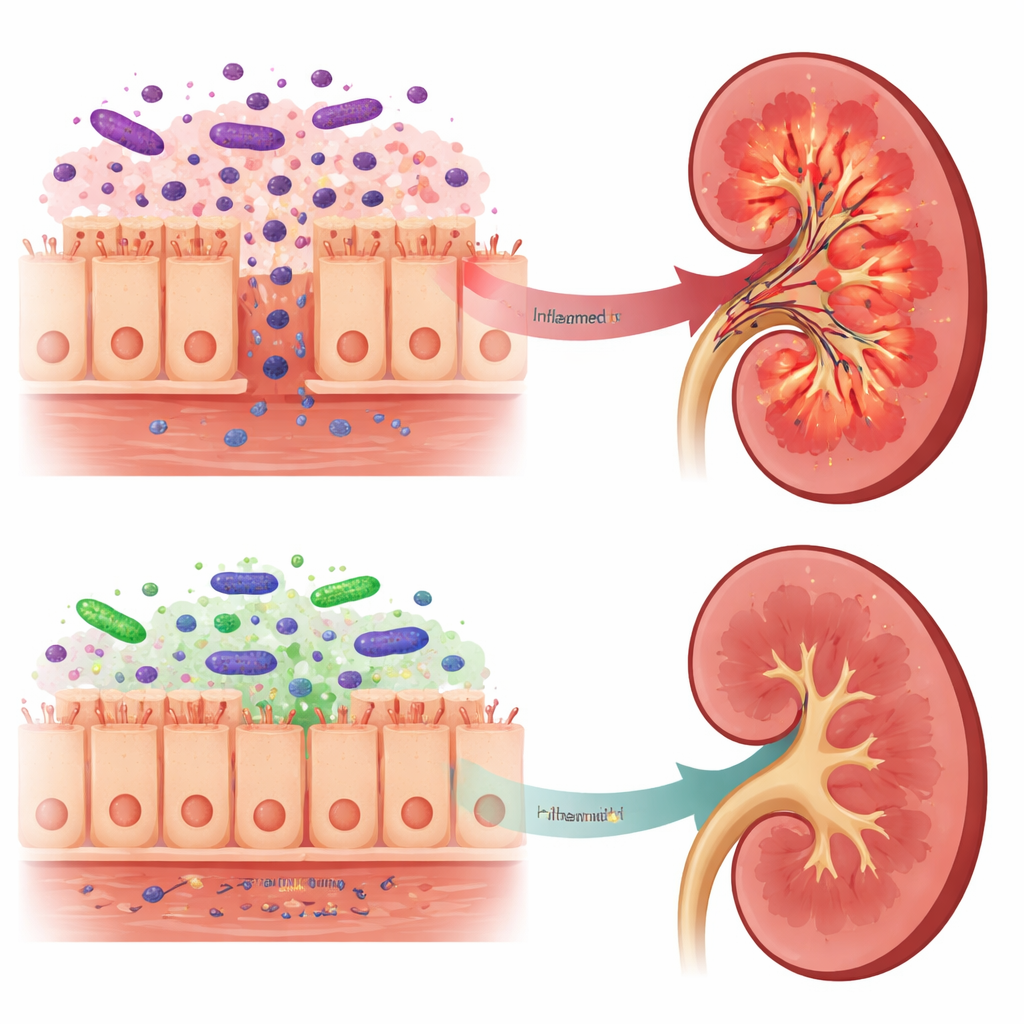
Från toxiska signaler till mildare budskap
Dessa förändringar i tarmen speglades av vad som nådde njurarna. I obehandlade hjärndöda råttor innehöll njurvävnaden mer LPS, högre nivåer av TLR4 och dess hjälpprotein LBP, samt starkare aktivering av NF-kappaB-vägen — alla tecken på ett kraftfullt inflammatoriskt svar. Däremot hade råttor som förbehandlats med Lactobacillus reuteri lägre nivåer av LPS i njurarna, svagare TLR4-signalering och minskad produktion av flera inflammatoriska molekyler, inklusive IL-6 och IFN-gamma. Intressant nog ökade den totala mängden LPS i blodet i probiotikagruppen, men analys av tarmmikroberna antydde att mycket av detta LPS kom från Bacteroidota, vars LPS-strukturer anses vara betydligt mindre inflammatoriska och kan fungera som partiella hämmare av TLR4-sensorn. Författarna föreslår att denna ”mildare” LPS konkurrerar med den mer skadliga formen och minskar njurarnas exponering för de mest toxiska signalerna.
Att balansera immunresponsen längs tarm–njure-axeln
Probiotikan gjorde mer än att bara förändra mikrober och barriärer; den finjusterade också immunsystemet på båda sidor av tarm–njure-förbindelsen. I tarmen var markörer för aktiverade immunceller såsom CD4 och CD25 förhöjda efter hjärndöd, vilket tyder på ett överaktivt svar vid slemhinnan. Lactobacillus reuteri nedskalade denna aktivering i själva epitelet men ökade CD25-positiva celler i de underliggande körtlarna, vilket antyder ett mer kontrollerat och lokaliserat försvar. I njurarna minskade probiotikan tecken på neutrofilansamling och oxidativ stress, samtidigt som den selektivt ökade kemokinen CXCL2, som kan hjälpa till att samordna ett mer balanserat reparationssvar. Korrelationsanalyser kopplade specifika medlemmar av Bacteroidota till dessa immunologiska förändringar, vilket stöder idén om ett tarmdrivet immunnätverk som hjälper till att skydda njurarna.
Vad detta kan innebära för framtida transplantationer
Sammantaget pekar fynden på en dubbel skyddande roll för Lactobacillus reuteri hos hjärndöda donatorråttor: den återbygger ett hälsosammare tarmcommunity och barriär samtidigt som den omformar immuna och inflammatoriska signaler som når njurarna. Som ett resultat utsätts njurceller för mindre av de starkt inflammatoriska LPS och uppvisar bättre funktionell och strukturell hälsa. Även om arbetet är prekliniskt och bygger på förbehandling före hjärndöd, belyser det tarmen och dess mikrober som lovande måltavlor för strategier att förbättra organkvalitet före transplantation, vilket potentiellt kan ge framtida mottagare en bättre utgångspunkt för långsiktig njurfunktion.
Citering: Liu, T., Zhu, G., Li, H. et al. Gut microbiota-dependent protection by Lactobacillus reuteri against renal injury in brain-dead rats. Sci Rep 16, 14709 (2026). https://doi.org/10.1038/s41598-026-47230-1
Nyckelord: tarmmikrobiota, probiotika, njurskada, donatorer med hjärndöd, Lactobacillus reuteri