Clear Sky Science · nl
Door de darmmicrobiota afhankelijke bescherming door Lactobacillus reuteri tegen nierbeschadiging bij hersendode ratten
Waarom dit onderzoek ertoe doet
De meeste nieren die voor transplantatie worden gebruikt, komen van donoren die hersendood hebben geleden, maar deze organen zijn vaak al beschadigd voordat de operatie begint. Deze studie bij ratten onderzoekt een onverwachte bondgenoot in de darm: een probioticum bacterie genaamd Lactobacillus reuteri. De onderzoekers laten zien hoe deze microbe de nieren kan helpen beschermen tegen schade na hersendood door de darmbacteriën te stabiliseren, de darmbarrière te versterken en schadelijke immuunreacties te dempen die anders de organen geschikt voor transplantatie zouden verzwakken.
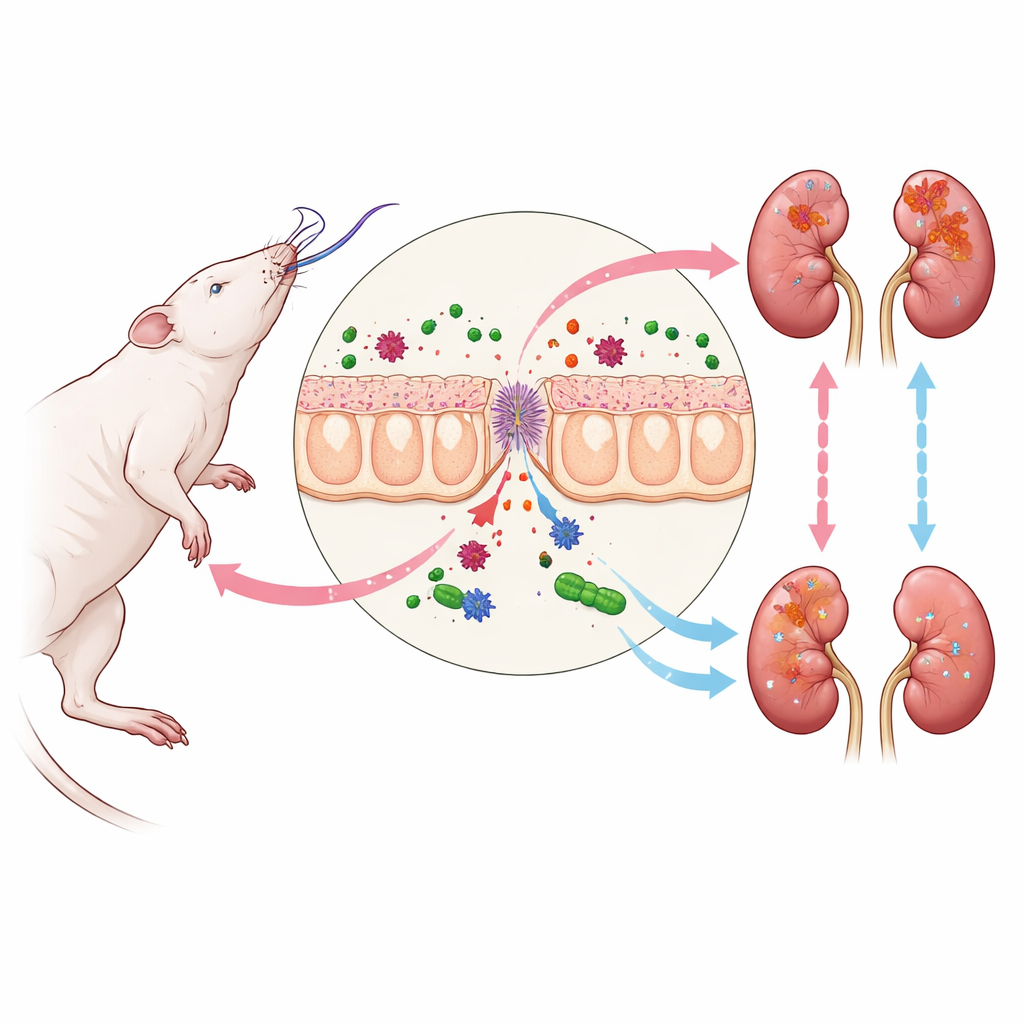
Hersendood en de kettingreactie naar de nieren
Wanneer hersendood optreedt, ervaart het lichaam een storm van hormonale en circulatoire veranderingen die door veel organen heen golven. Een van de eerste zwakke schakels is de darm. De beschermende bekleding wordt lekkend, waardoor bacteriële fragmenten van darmmicroben in de bloedbaan kunnen glippen. Een van die fragmenten is LPS, een component van de celwand van bepaalde bacteriën die het immuunsysteem sterk activeert. Terwijl LPS naar de nieren reist, hecht het zich aan een sensor op niercellen die het TLR4–NF-kappaB-pad activeert, een signaalroute die bekendstaat om het aansturen van ontsteking. In het hier gebruikte rattenmodel leidde dit proces tot hogere bloedniveaus van creatinine en ureum, verhoogde expressie van de nierbeschadigingsmarker KIM-1, en subtiele structurele schade in nierbuiscellen, zelfs wanneer standaard microscopische beelden vrijwel normaal leken.
Een probioticum herbedraad het darmmilieu
Het team vroeg zich vervolgens af of het voeren van ratten met Lactobacillus reuteri gedurende een week vóór hersendood dit verhaal kon veranderen. Zij vonden dat het probioticum de samenstelling van de darmmicrobiota herstructureerde: schadelijke, LPS-rijke Proteobacteria namen af, terwijl Bacteroidota en andere mogelijk gunstige groepen in relatieve overvloed toenamen. Tegelijkertijd verbeterde de fysieke barrière van de darm. Onder de microscoop en in elektronenmicrografieën toonden behandelde dieren meer intacte celverbindingen tussen darmcellen en minder verwijding van de ruimtes waar lekken ontstaan. De bloedspiegels van iFABP, een marker voor darmletsel en -permeabiliteit, daalden richting normaal, wat wijst op een strakkere, selectiever werkende darmwand.
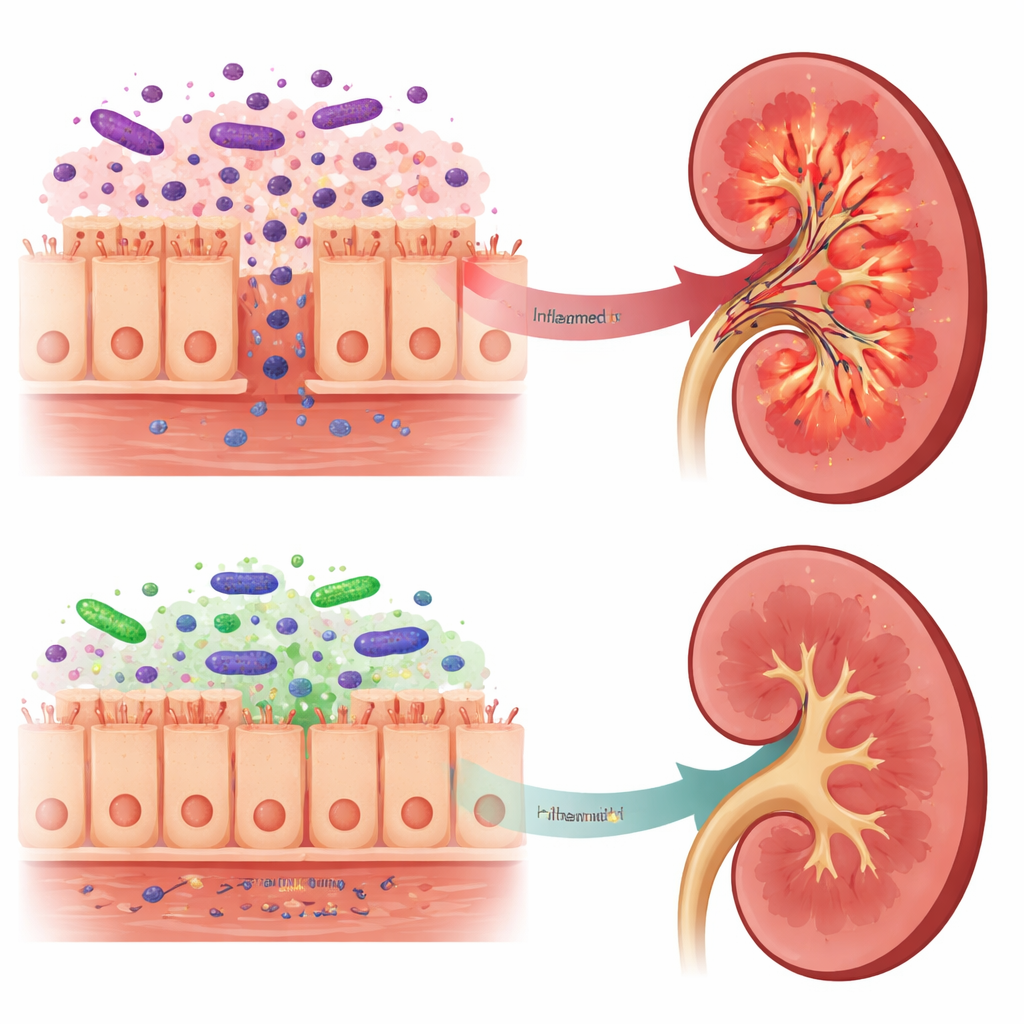
Van toxische signalen naar mildere boodschappen
Deze verschuivingen in de darm weerspiegelden zich in wat de nieren bereikte. Bij onbehandelde hersendode ratten bevatte nierweefsel meer LPS, hogere niveaus van TLR4 en het hulp-eiwit LBP, en sterkere activatie van het NF-kappaB-pad, allemaal tekenen van een robuuste ontstekingsreactie. Daarentegen hadden ratten die vooraf waren behandeld met Lactobacillus reuteri lagere nier-LPS, zwakkere TLR4-signalisatie en verminderde productie van meerdere ontstekingsmoleculen, waaronder IL-6 en IFN-gamma. Interessant genoeg steeg de totale LPS in het bloed juist in de probioticagroep, maar analyse van de darmmicroben suggereerde dat veel van dit LPS afkomstig was van Bacteroidota, waarvan wordt gedacht dat de LPS-structuren veel minder ontstekingsbevorderend zijn en mogelijk zelfs als gedeeltelijke blokkeraars van de TLR4-sensor werken. De auteurs stellen dat deze “mildere” LPS concurreert met de schadelijkere vorm, waardoor de blootstelling van de nier aan de meest toxische signalen afneemt.
Het immuunantwoord in balans langs de darm–nierroute
Het probioticum deed meer dan alleen microben en barrières veranderen; het stemde ook het immuunsysteem af aan beide zijden van de darm–nierverbinding. In de darm waren markers van geactiveerde immuuncellen zoals CD4 en CD25 verhoogd na hersendood, wat wijst op een overactieve reactie aan het mucosale oppervlak. Lactobacillus reuteri temperde deze activatie in het slijmvlies zelf maar verhoogde CD25-positieve cellen in de onderliggende klieren, wat duidt op een meer gecontroleerde en gelokaliseerde verdediging. In de nieren verminderde het probioticum tekenen van neutrofiele ophoping en oxidatieve stress, terwijl het selectief de chemokine CXCL2 versterkte, wat kan bijdragen aan een meer gebalanceerde reparatiereactie. Correlatieanalyses koppelden specifieke Bacteroidota-leden aan deze immuunveranderingen, wat de gedachte ondersteunt van een door de darm gestuurd immuunnetwerk dat de nieren helpt beschermen.
Wat dit voor toekomstige transplantaties zou kunnen betekenen
Gezamenlijk wijzen de bevindingen op een dubbele beschermende rol van Lactobacillus reuteri in hersendode donorratten: het herstelt een gezondere darmgemeenschap en -barrière en herschikt tegelijkertijd immuun- en ontstekingssignalen die de nieren bereiken. Daardoor worden niercellen minder blootgesteld aan sterk ontstekingsbevorderende LPS en vertonen ze betere functionele en structurele gezondheid. Hoewel het werk preklinisch is en steunt op voorbehandeling vóór hersendood, benadrukt het de darm en zijn microben als veelbelovende doelwitten voor strategieën om orgaankwaliteit vóór transplantatie te verbeteren, waardoor ontvangers mogelijk een betere uitgangspositie krijgen voor langdurige nierfunctie.
Bronvermelding: Liu, T., Zhu, G., Li, H. et al. Gut microbiota-dependent protection by Lactobacillus reuteri against renal injury in brain-dead rats. Sci Rep 16, 14709 (2026). https://doi.org/10.1038/s41598-026-47230-1
Trefwoorden: darmmicrobiota, probiotica, nierbeschadiging, hersendode donoren, Lactobacillus reuteri