Clear Sky Science · ar
الحماية المعتمدة على ميكروبيوتا الأمعاء بواسطة Lactobacillus reuteri ضد إصابة الكلى في جرذان ماتت أدمغتهم
لماذا تهم هذه الدراسة
معظم الكُلى المستخدمة في عمليات الزرع تأتي من متبرعين أصيبوا بموت دماغي، لكن هذه الأعضاء غالبًا ما تتعرض للضرر قبل بدء الجراحة. تستكشف هذه الدراسة في الجرذان حليفًا غير متوقع يعيش في الأمعاء: بكتيريا بروبيوتيك تُدعى Lactobacillus reuteri. يوضح الباحثون كيف يمكن لهذه الميكروبيوم أن تساعد في حماية الكُلى من الإصابة بعد موت الدماغ عن طريق استقرار بكتيريا الأمعاء، تقوية حاجز الأمعاء، وتهدئة الاستجابات المناعية الضارة التي قد تضعف الأعضاء الجاهزة للزرع.
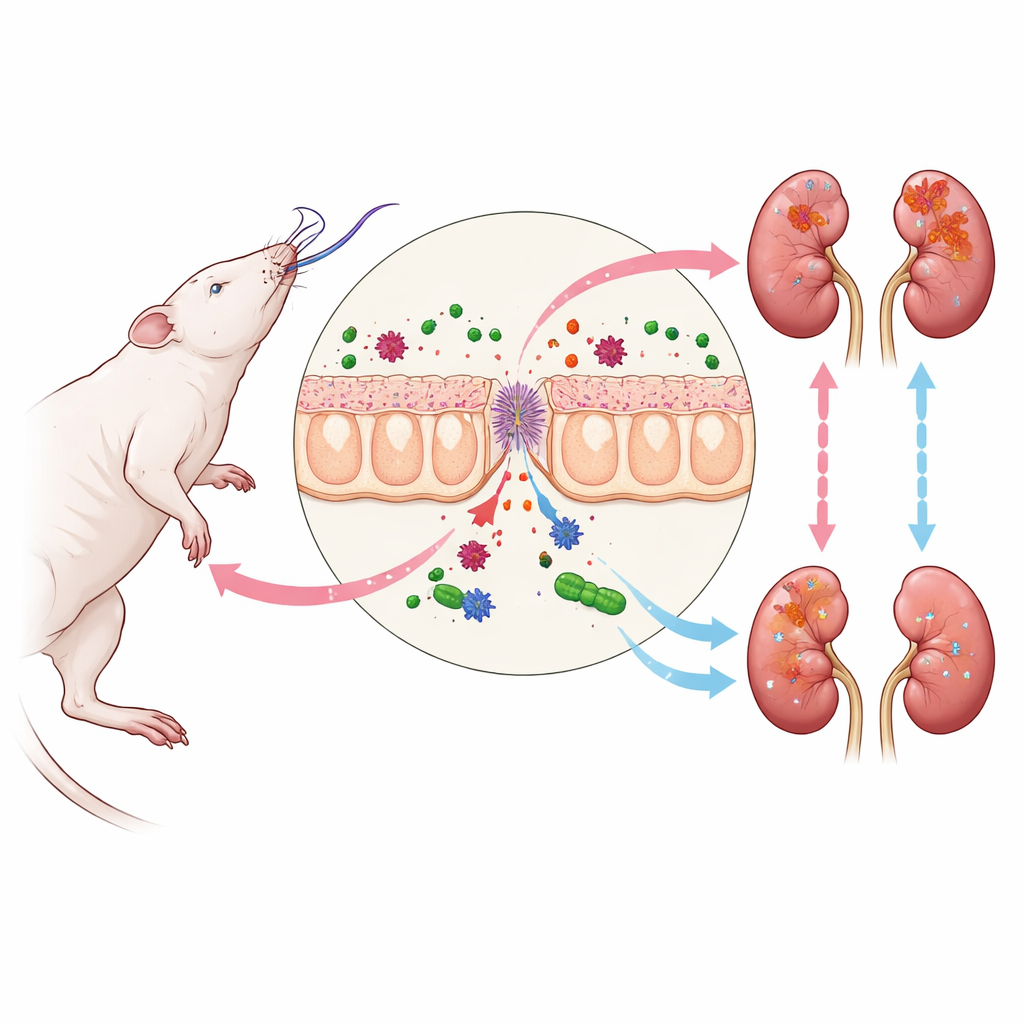
موت الدماغ وسلسلة التفاعلات المؤثرة على الكُلى
عند حدوث موت الدماغ، يمر الجسم بعاصفة من التغيرات الهرمونية والدورانية التي تمتد لتؤثر على عدة أعضاء. أحد أضعف النقاط المبكرة هو الأمعاء. يصبح الغلاف الواقي لها مساميًا، مما يسمح لقطع بكتيرية من ميكروبات الأمعاء بالتسرب إلى مجرى الدم. من بين هذه القطع يوجد LPS، مكوّن في جدران بعض البكتيريا يفعّل الجهاز المناعي بشكل قوي. أثناء انتقال LPS إلى الكُلى، يرتبط بمستشعر على خلايا الكلى الذي يفعّل مسار TLR4–NF-kappaB، وهو طريق إشاري معروف بتحفيز الالتهاب. في نموذج الجرذان المستخدم هنا، أدت هذه السلسلة إلى ارتفاع مستويات الكرياتينين واليوريا في الدم، وزيادة التعبير عن علامة تلف الكلى KIM-1، وأضرار تركيبية دقيقة في خلايا أنابيب الكُلى، حتى عندما بدت الصور المجهريّة العادية قريبة من الطبيعية.
بروبيوتيك يعيد تشكيل بيئة الأمعاء
سأل الفريق بعد ذلك ما إذا كان إطعام الجرذان Lactobacillus reuteri لمدة أسبوع قبل موت الدماغ قد يغيّر مجرى الأحداث هذا. وجدوا أن البروبيوتيك أعاد تشكيل مجتمع الميكروبات المعوية: تراجعت مجموعات ضارة غنية بـ LPS من فصيلة Proteobacteria، بينما ازداد وجود Bacteroidota ومجموعات أخرى قد تكون مفيدة. في الوقت نفسه تحسّن الحاجز المادي للأمعاء. تحت المِجهر وفي الصور الإلكترونية، أظهر الحيوانات المعالجة تقاطعات خلوية أكثر سلامة بين خلايا الأمعاء وتقلصًا في اتساع الفراغات التي تتشكل فيها التسريبات. انخفضت مستويات iFABP في الدم، وهي علامة على إصابة الأمعاء وزيادة نفاذيتها، فتقترب من الطبيعي مما يدل على جدار معوي أكثر إحكامًا وانتقائية.
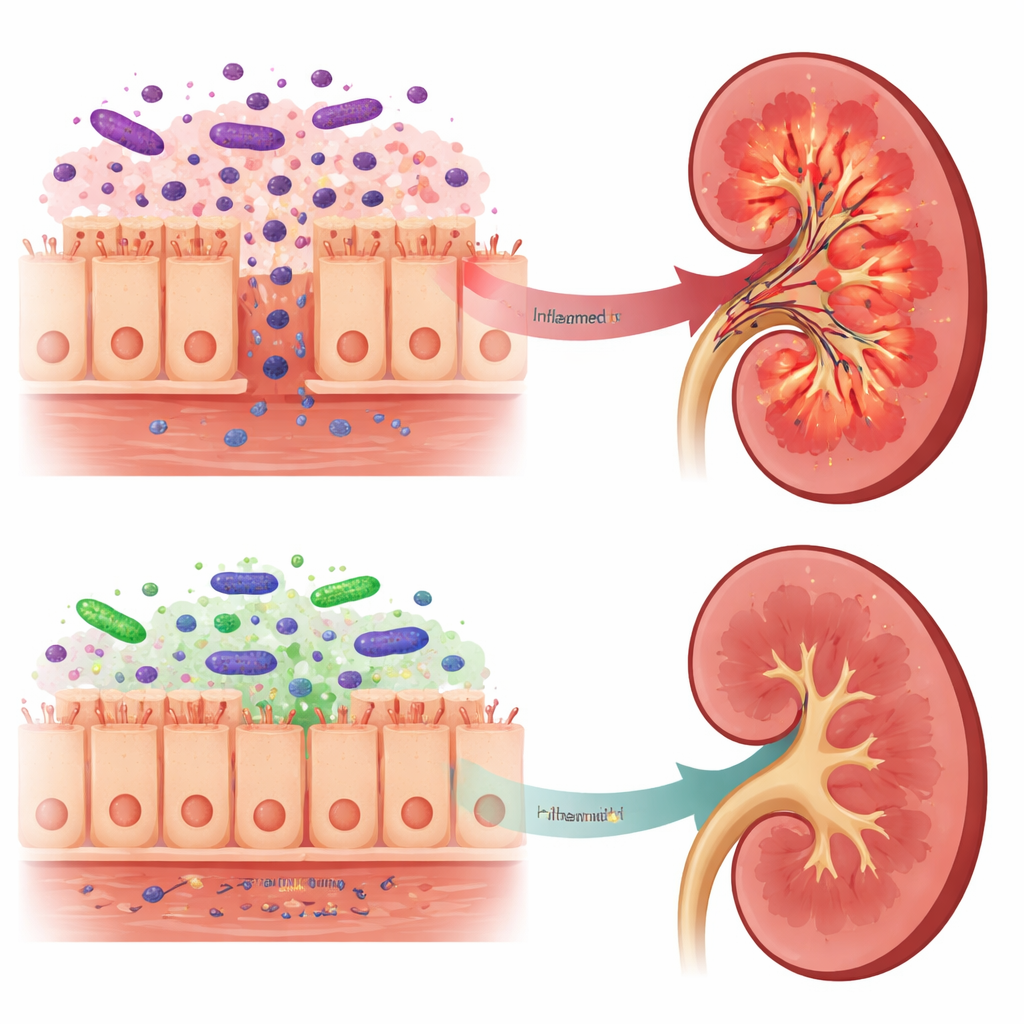
من إشارات سامة إلى رسائل أخف
انعكست هذه التغيّرات المعوية على ما يصل إلى الكُلى. في الجرذان المتوفاة دماغيًا ولم تُعالَج، احتوت أنسجة الكُلى على مستويات أعلى من LPS، ومستويات أعظم من TLR4 وبروتين المساعدة LBP، وتفعيل أقوى لمسار NF-kappaB، وكلها علامات على استجابة التهابية قوية. بالمقابل، كانت الكلى لدى الجرذان المعالجة سابقًا بـ Lactobacillus reuteri أقل احتواءً على LPS، وأضعف في إشارات TLR4، وانخفاضًا في إنتاج عدة جزيئات التهابية بما في ذلك IL-6 وIFN-gamma. ومن المثير للاهتمام أن إجمالي LPS في الدم ارتفع فعليًا في مجموعة البروبيوتيك، لكن تحليل ميكروبات الأمعاء أشار إلى أن جزءًا كبيرًا من هذا LPS مصدره Bacteroidota، التي يُعتقد أن تراكيب LPS فيها أقل التهابًا وقد تعمل حتى كحاجز جزئي لمستشعر TLR4. يقترح المؤلفون أن هذا النوع «الألين» من LPS يتنافس مع الشكل الأكثر ضررًا، مخففًا تعرض الكُلى للإشارات الأكثر سمية.
موازنة الاستجابة المناعية على طول محور الأمعاء–الكُلى
لم يقتصر تأثير البروبيوتيك على تغيير الميكروبات والحواجز؛ بل ضبط أيضًا الجهاز المناعي على جانبي محور الأمعاء–الكُلى. في الأمعاء ارتفعت علامات الخلايا المناعية المنشّطة مثل CD4 وCD25 بعد موت الدماغ، ما يشير إلى استجابة مفرطة على السطح المخاطي. خفف Lactobacillus reuteri هذا التفعيل في البطانة نفسها لكنه زاد الخلايا الموجبة لـ CD25 في الغدد التحتية، مُلمّحًا إلى دفاع أكثر تحكمًا ومحددًا موضعيًا. في الكُلى قلل البروبيوتيك علامات تراكم العدلات والإجهاد التأكسدي، بينما عزّز انتقائيًا الكيموكين CXCL2، الذي قد يساعد على تنسيق استجابة إصلاح أكثر توازنًا. ربطت تحليلات الترابط بين أعضاء محددين من Bacteroidota وهذه التغيرات المناعية، مما يدعم فكرة وجود شبكة مناعية مدفوعة بالأمعاء تساعد على حماية الكُلى.
ماذا قد يعني هذا للزرعات المستقبلية
تشير النتائج مجتمعة إلى دور وقائي مزدوج لـ Lactobacillus reuteri في جرذان المتبرعين بموت الدماغ: يعيد بناء مجتمع معوي وحاجز أفضل بينما يعيد تشكيل الإشارات المناعية والالتهابية التي تصل إلى الكُلى. ونتيجة لذلك تواجه خلايا الكُلى تعرضًا أقل لـ LPS شديد الالتهاب وتظهر صحة وظيفية وتركيبية أفضل. وعلى الرغم من أن العمل ما زال قبل سريري ويعتمد على المعالجة المسبقة قبل موت الدماغ، فإنه يبرز الأمعاء وميكروباتها كأهداف واعدة لاستراتيجيات تحسين جودة الأعضاء قبل الزرع، مما قد يمنح المستقبلين نقطة انطلاق أفضل لوظيفة كلوية طويلة الأمد.
الاستشهاد: Liu, T., Zhu, G., Li, H. et al. Gut microbiota-dependent protection by Lactobacillus reuteri against renal injury in brain-dead rats. Sci Rep 16, 14709 (2026). https://doi.org/10.1038/s41598-026-47230-1
الكلمات المفتاحية: ميكروبيوتا الأمعاء, بروبيوتيك, إصابة الكلى, المتبرعون بموت الدماغ, Lactobacillus reuteri