Clear Sky Science · fr
Protection dépendante du microbiote intestinal par Lactobacillus reuteri contre les lésions rénales chez des rats en état de mort encéphalique
Pourquoi cette recherche est importante
La plupart des reins utilisés pour les greffes proviennent de donneurs en mort encéphalique, mais ces organes sont souvent endommagés avant même le début de l’intervention. Cette étude chez le rat explore un allié inattendu vivant dans l’intestin : une bactérie probiotique appelée Lactobacillus reuteri. Les chercheurs montrent comment ce microbe peut contribuer à protéger les reins des lésions post–mort encéphalique en stabilisant la flore intestinale, en renforçant la barrière intestinale et en calmant les réactions immunitaires nocives qui affaibliraient autrement les organes prêts à la transplantation.
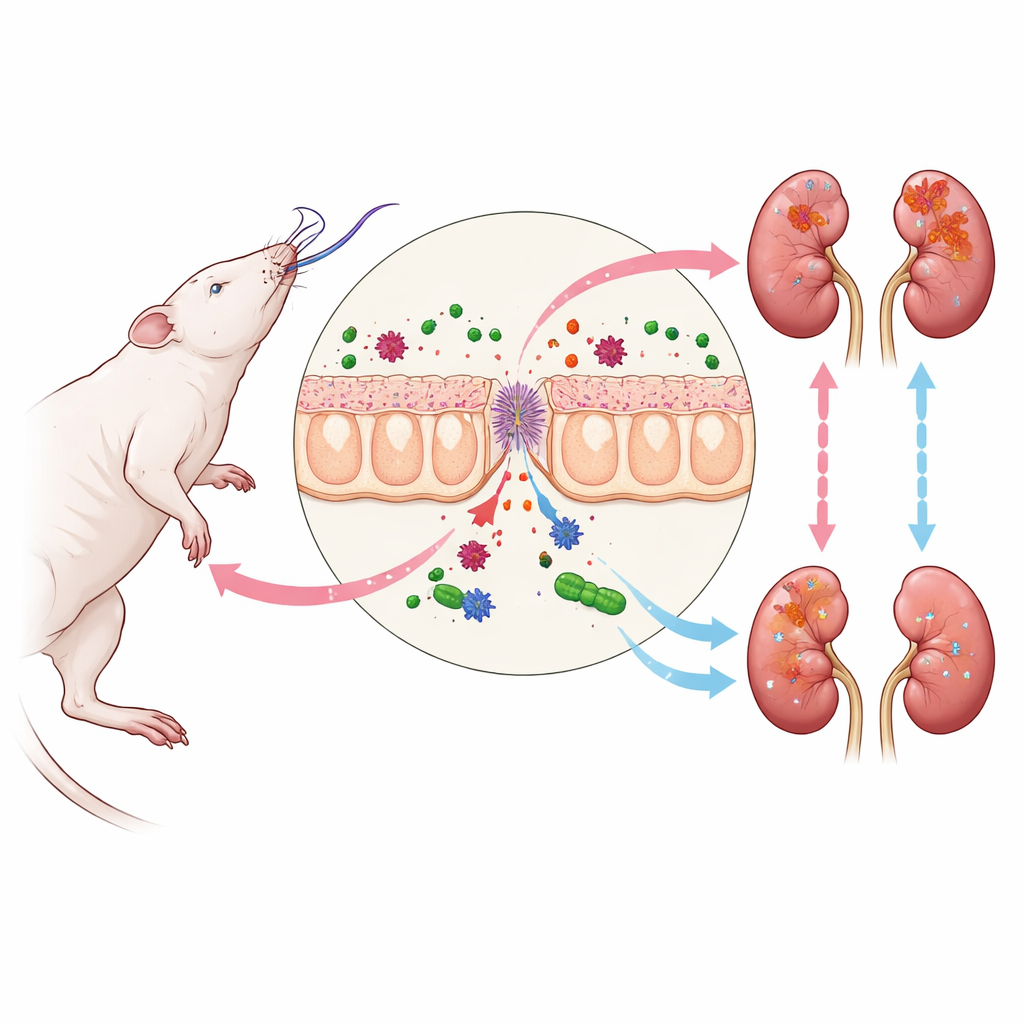
La mort encéphalique et la réaction en chaîne vers les reins
Lorsque la mort encéphalique survient, l’organisme subit une tempête de changements hormonaux et circulatoires qui se propagent à de nombreux organes. L’un des premiers points faibles est l’intestin. Son épithélium protecteur devient perméable, permettant à des fragments bactériens du microbiote intestinal de passer dans la circulation sanguine. Parmi ces fragments se trouve le LPS, un composant de certaines parois bactériennes qui active fortement le système immunitaire. Lorsqu’il atteint les reins, le LPS se lie à un capteur sur les cellules rénales qui déclenche la voie TLR4–NF-kappaB, une voie de signalisation bien connue pour stimuler l’inflammation. Dans le modèle de rat utilisé ici, ce processus a conduit à une augmentation des taux sanguins de créatinine et d’urée, à une élévation de l’expression du marqueur de lésion rénale KIM-1, et à des lésions structurelles subtiles des cellules des tubules rénaux, même lorsque les vues microscopiques standard semblaient presque normales.
Un probiotique reconfigure l’environnement intestinal
L’équipe s’est ensuite demandé si nourrir les rats avec Lactobacillus reuteri pendant une semaine avant la mort encéphalique pouvait changer cette trajectoire. Ils ont constaté que le probiotique remodelait la communauté microbienne de l’intestin : les Proteobacteria nocives riches en LPS diminuaient, tandis que les Bacteroidota et d’autres groupes potentiellement bénéfiques devenaient plus abondants. Parallèlement, la barrière physique de l’intestin s’est améliorée. À l’échelle microscopique et en micrographies électroniques, les animaux traités présentaient des jonctions entre cellules intestinales plus intactes et moins d’élargissement des espaces où se forment les fuites. Les taux sanguins d’iFABP, un marqueur de lésion et de perméabilité intestinale, sont revenus vers la normale, indiquant une paroi intestinale plus serrée et plus sélective.
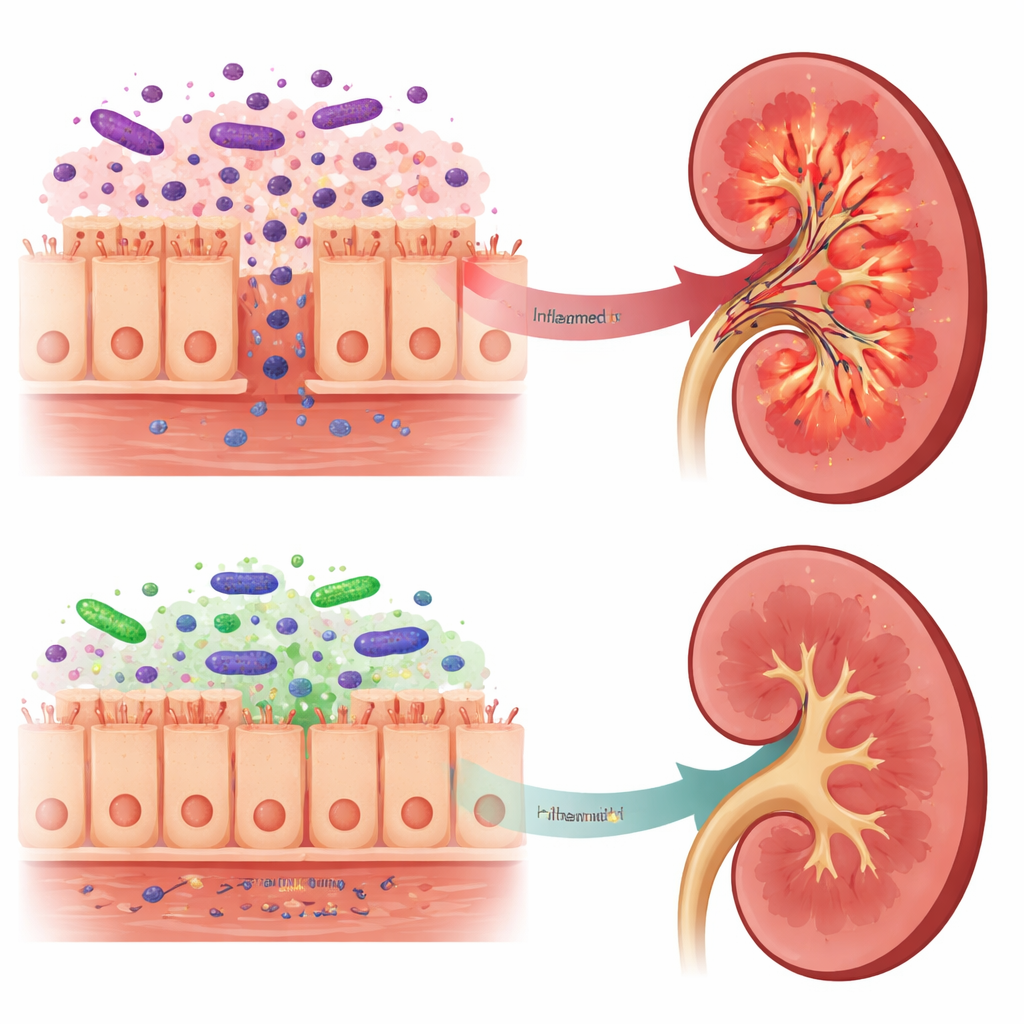
De signaux toxiques à des messages plus doux
Ces changements dans l’intestin se reflétaient dans ce qui atteignait les reins. Chez les rats non traités en mort encéphalique, les tissus rénaux contenaient plus de LPS, des niveaux plus élevés de TLR4 et de sa protéine auxiliaire LBP, et une activation plus forte de la voie NF-kappaB, autant d’indicateurs d’une réponse inflammatoire robuste. En revanche, les rats prétraités par Lactobacillus reuteri présentaient moins de LPS rénal, une signalisation TLR4 plus faible et une production réduite de plusieurs molécules inflammatoires, notamment IL-6 et IFN-gamma. Fait intéressant, la quantité totale de LPS dans le sang augmentait en réalité dans le groupe probiotique, mais l’analyse du microbiote intestinal suggérait qu’une grande partie de ce LPS provenait de Bacteroidota, dont les structures de LPS sont considérées comme beaucoup moins inflammatoires et pourraient même agir comme des bloqueurs partiels du capteur TLR4. Les auteurs proposent que ce LPS « plus doux » entre en compétition avec la forme plus dommageable, réduisant ainsi l’exposition rénale aux signaux les plus toxiques.
Équilibrer la réponse immunitaire le long de l’axe intestin–rein
Le probiotique n’a pas seulement modifié les microbes et la barrière ; il a aussi modulé le système immunitaire des deux côtés de la connexion intestin–rein. Dans l’intestin, des marqueurs de cellules immunitaires activées tels que CD4 et CD25 étaient augmentés après la mort encéphalique, suggérant une réponse excessive à la surface muqueuse. Lactobacillus reuteri a réduit cette activation dans l’épithélium lui-même tout en augmentant les cellules CD25–positives dans les glandes sous-jacentes, ce qui suggère une défense plus contrôlée et localisée. Dans les reins, le probiotique a réduit les signes d’accumulation de neutrophiles et de stress oxydatif, tout en augmentant sélectivement la chimiokine CXCL2, qui pourrait aider à coordonner une réponse de réparation plus équilibrée. Des analyses de corrélation ont relié des membres spécifiques des Bacteroidota à ces modifications immunitaires, appuyant l’idée d’un réseau immunitaire piloté par l’intestin qui contribue à protéger les reins.
Ce que cela pourrait signifier pour les futures transplantations
Globalement, les résultats suggèrent un double rôle protecteur de Lactobacillus reuteri chez les rats donneurs en mort encéphalique : il reconstruit une communauté intestinale et une barrière plus saines tout en remodelant les signaux immunitaires et inflammatoires atteignant les reins. En conséquence, les cellules rénales sont moins exposées à des LPS fortement inflammatoires et présentent une meilleure santé fonctionnelle et structurelle. Bien que ce travail soit préclinique et repose sur un prétraitement avant la mort encéphalique, il met en lumière l’intestin et ses microbes comme des cibles prometteuses pour des stratégies visant à améliorer la qualité des organes avant transplantation, offrant potentiellement aux futurs receveurs de meilleures chances pour une fonction rénale à long terme.
Citation: Liu, T., Zhu, G., Li, H. et al. Gut microbiota-dependent protection by Lactobacillus reuteri against renal injury in brain-dead rats. Sci Rep 16, 14709 (2026). https://doi.org/10.1038/s41598-026-47230-1
Mots-clés: microbiote intestinal, probiotiques, lésion rénale, donneurs en mort encéphalique, Lactobacillus reuteri