Clear Sky Science · es
Protección dependiente de la microbiota intestinal por Lactobacillus reuteri frente a la lesión renal en ratas con muerte cerebral
Por qué importa esta investigación
La mayoría de los riñones utilizados para trasplantes proceden de donantes que han sufrido muerte cerebral, pero esos órganos con frecuencia ya están dañados antes de comenzar la cirugía. Este estudio en ratas explora un aliado inesperado que vive en el intestino: una bacteria probiótica llamada Lactobacillus reuteri. Los investigadores muestran cómo este microbio puede ayudar a proteger los riñones frente a la lesión tras la muerte cerebral al estabilizar la comunidad microbiana intestinal, reforzar la barrera intestinal y atenuar reacciones inmunitarias nocivas que de otro modo debilitarían los órganos listos para el trasplante.
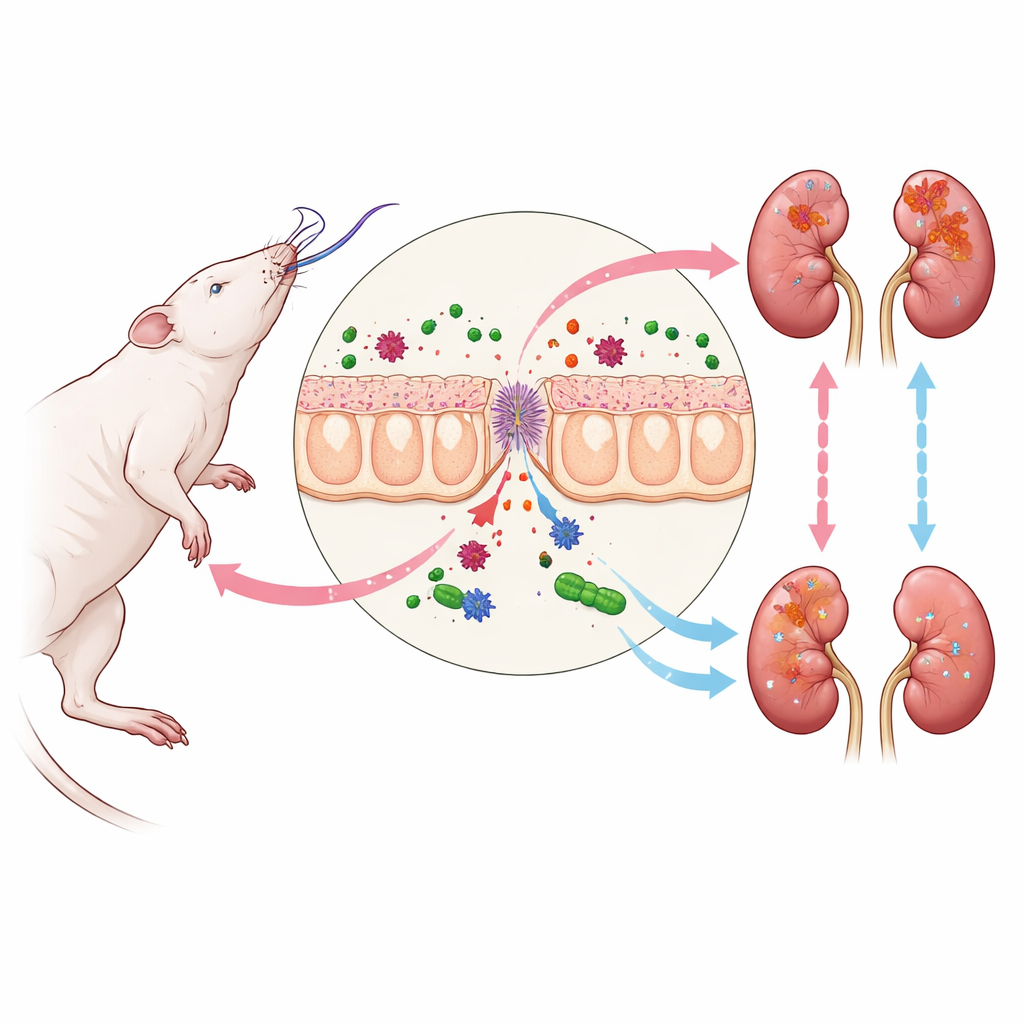
Muerte cerebral y la reacción en cadena hacia los riñones
Cuando ocurre la muerte cerebral, el cuerpo experimenta una tormenta de cambios hormonales y circulatorios que se propagan por muchos órganos. Uno de los primeros puntos débiles es el intestino. Su revestimiento protector se vuelve permeable, permitiendo que fragmentos bacterianos de la microbiota intestinal se filtren al torrente sanguíneo. Entre esos fragmentos está el LPS, un componente de la pared celular de ciertas bacterias que activa fuertemente el sistema inmune. A medida que el LPS llega a los riñones, se une a un sensor en las células renales que desencadena la vía TLR4–NF-kappaB, una ruta de señalización bien conocida por promover la inflamación. En el modelo de rata empleado aquí, este proceso condujo a niveles sanguíneos más altos de creatinina y urea, mayor expresión del marcador de daño renal KIM-1 y daño estructural sutil en las células de los túbulos renales, incluso cuando las vistas microscópicas estándar parecían casi normales.
Un probiótico reconfigura el entorno intestinal
El equipo se preguntó si alimentar a las ratas con Lactobacillus reuteri durante una semana antes de la muerte cerebral podría cambiar este desenlace. Encontraron que el probiótico remodeló la comunidad microbiana intestinal: se redujeron las Proteobacterias ricas en LPS y potencialmente dañinas, mientras que Bacteroidota y otros grupos potencialmente beneficiosos aumentaron en abundancia. Al mismo tiempo, mejoró la barrera física del intestino. Bajo el microscopio y en micrografías electrónicas, los animales tratados mostraron uniones celulares entre enterocitos más intactas y menos ensanchamiento de los espacios por donde se forman las filtraciones. Los niveles sanguíneos de iFABP, un marcador de lesión intestinal y permeabilidad, descendieron hacia valores normales, lo que indica una pared intestinal más hermética y selectiva.
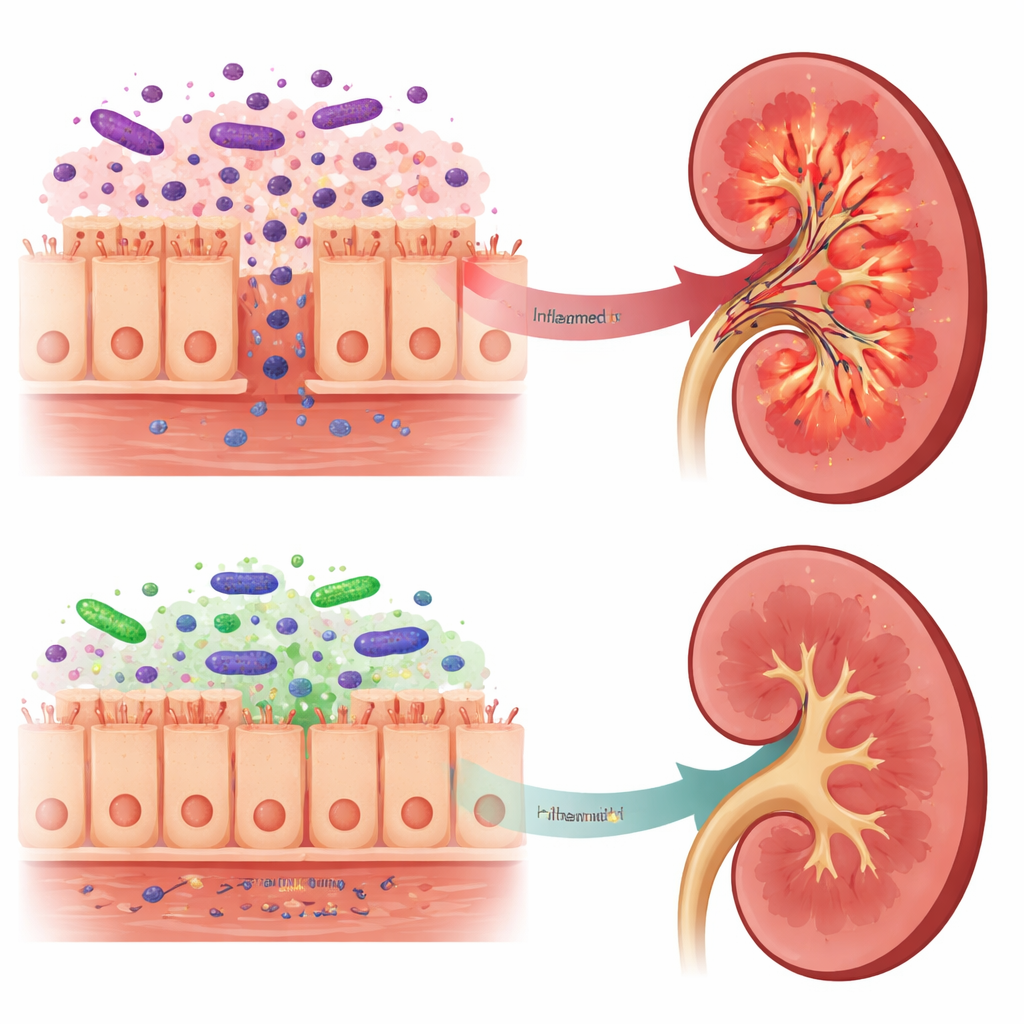
De señales tóxicas a mensajes más suaves
Estos cambios en el intestino se reflejaron en lo que llegaba a los riñones. En ratas con muerte cerebral no tratadas, el tejido renal contenía más LPS, mayores niveles de TLR4 y su proteína ayudante LBP, y una activación más intensa de la vía NF-kappaB, todas señales de una respuesta inflamatoria robusta. En cambio, las ratas pretratadas con Lactobacillus reuteri presentaron menor LPS renal, señalización TLR4 más débil y reducción en la producción de varias moléculas inflamatorias, incluidas IL-6 e IFN-gamma. Curiosamente, el LPS total en sangre aumentó en el grupo probiótico, pero el análisis de la microbiota intestinal sugirió que gran parte de ese LPS procedía de Bacteroidota, cuyos LPS se consideran mucho menos inflamatorios y podrían incluso actuar como bloqueadores parciales del sensor TLR4. Los autores proponen que este LPS “más suave” compite con la forma más dañina, reduciendo la exposición renal a las señales más tóxicas.
Equilibrando la respuesta inmune a lo largo de la ruta intestino–riñón
El probiótico hizo más que alterar microbios y barreras; también moduló el sistema inmune en ambos lados de la conexión intestino–riñón. En el intestino, marcadores de células inmunes activadas como CD4 y CD25 aumentaron tras la muerte cerebral, lo que sugiere una respuesta sobreactivada en la superficie mucosa. Lactobacillus reuteri redujo esta activación en el propio epitelio pero aumentó las células CD25 positivas en las glándulas subyacentes, lo que apunta a una defensa más controlada y localizada. En los riñones, el probiótico disminuyó signos de acumulación de neutrófilos y estrés oxidativo, al tiempo que elevó selectivamente la quimiocina CXCL2, que puede ayudar a coordinar una respuesta de reparación más equilibrada. Los análisis de correlación vincularon miembros específicos de Bacteroidota con estos cambios inmunitarios, apoyando la idea de una red inmune impulsada por el intestino que contribuye a proteger los riñones.
Qué podría significar esto para futuros trasplantes
En conjunto, los hallazgos apuntan a un doble papel protector de Lactobacillus reuteri en ratas donantes con muerte cerebral: reconstruye una comunidad y una barrera intestinal más saludables, a la vez que remodela las señales inmunitarias e inflamatorias que alcanzan los riñones. Como resultado, las células renales experimentan menor exposición a LPS altamente inflamatorio y muestran mejor salud funcional y estructural. Aunque el trabajo es preclínico y se basa en el pretratamiento antes de la muerte cerebral, pone de relieve al intestino y sus microbios como objetivos prometedores para estrategias destinadas a mejorar la calidad de los órganos antes del trasplante, lo que podría ofrecer a los futuros receptores una mejor base para la función renal a largo plazo.
Cita: Liu, T., Zhu, G., Li, H. et al. Gut microbiota-dependent protection by Lactobacillus reuteri against renal injury in brain-dead rats. Sci Rep 16, 14709 (2026). https://doi.org/10.1038/s41598-026-47230-1
Palabras clave: microbiota intestinal, probióticos, lesión renal, donantes con muerte cerebral, Lactobacillus reuteri