Clear Sky Science · ru
Защита от повреждения почек, зависящая от микробиоты кишечника, обеспечиваемая Lactobacillus reuteri у крыс с мозговой смертью
Почему это исследование важно
Большинство почек, используемых для трансплантации, получают от доноров с мозговой смертью, но эти органы часто повреждаются еще до начала операции. В этом исследовании на крысах изучается неожиданный союзник, обитающий в кишечнике: пробиотическая бактерия Lactobacillus reuteri. Авторы демонстрируют, как этот микроорганизм может помочь защитить почки от повреждений после мозговой смерти, стабилизируя состав кишечной микробиоты, укрепляя кишечный барьер и смягчая вредные иммунные реакции, которые в противном случае ослабили бы органы, готовые к трансплантации.
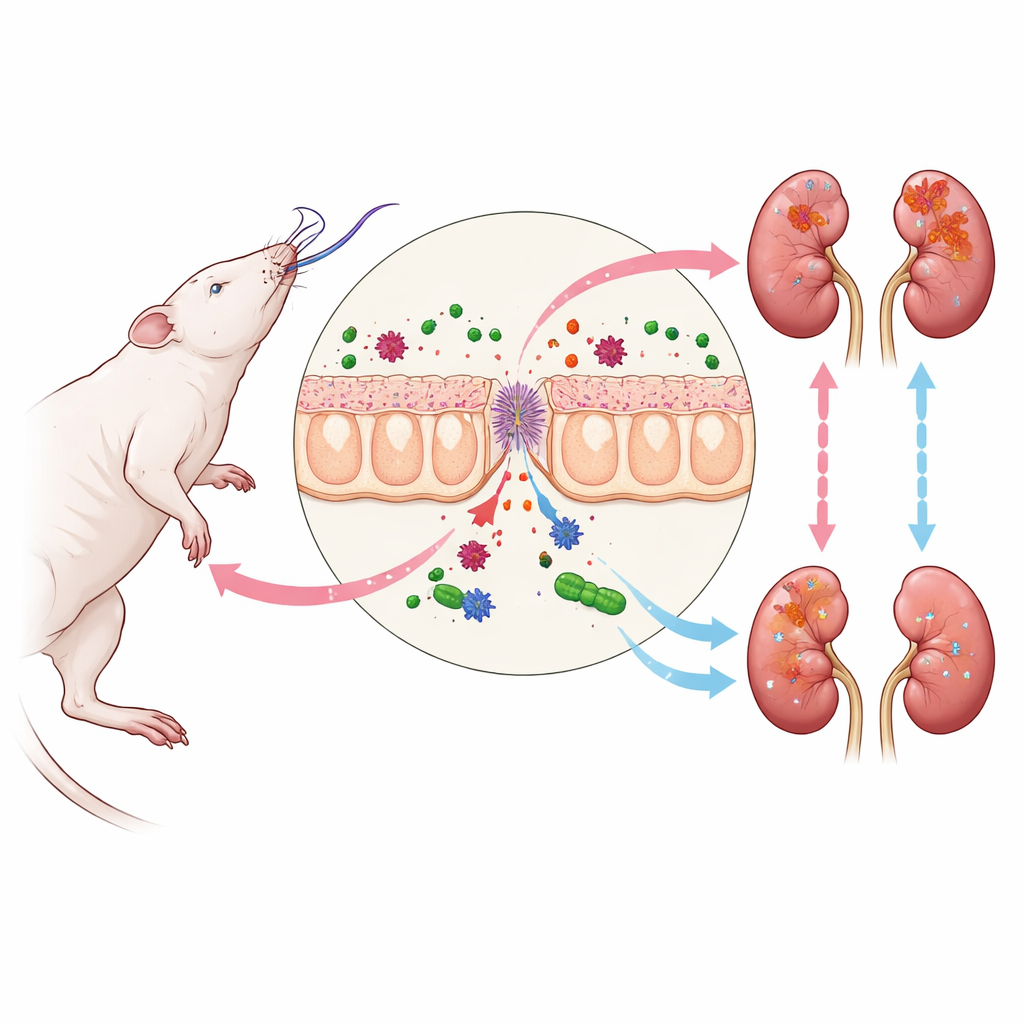
Мозговая смерть и каскадный эффект для почек
При наступлении мозговой смерти организм переживает бурю гормональных и циркуляторных изменений, которые отражаются на многих органах. Одним из первых уязвимых мест оказывается кишечник. Его защитный эпителий становится проницаемым, что позволяет фрагментам бактерий из кишечной микробиоты просачиваться в кровоток. Среди этих фрагментов находится LPS — компонент клеточных стенок некоторых бактерий, который сильно активирует иммунную систему. По мере того как LPS попадает в почки, он связывается с рецептором на почечных клетках, запускающим путь TLR4–NF-kappaB — сигнальную каскаду, известную тем, что способствует воспалению. В примененной модели на крысах этот процесс приводил к повышению уровня креатинина и мочевины в крови, увеличению экспрессии маркера повреждения почек KIM-1 и к тонким структурным нарушениям в клетках канальцев почки, даже когда стандартная микроскопия выглядела почти нормальной.
Пробиотик перестраивает среду кишечника
Затем исследователи выяснили, изменит ли кормление крыс Lactobacillus reuteri в течение недели до наступления мозговой смерти этот сценарий. Они обнаружили, что пробиотик перестраивал микробное сообщество кишечника: вредные LPS-обогащенные протеобактерии уменьшились, тогда как Bacteroidota и другие потенциально полезные группы стали более многочисленными. Одновременно улучшился физический барьер кишечника. При световой и электронной микроскопии у обработанных животных наблюдались более целостные контакты между клетками эпителия и меньшее расширение промежутков, через которые формируются утечки. Уровни iFABP в крови — маркера повреждения и проницаемости кишечника — снизились к нормальным значениям, что указывает на более плотную и селективную стенку кишечника.
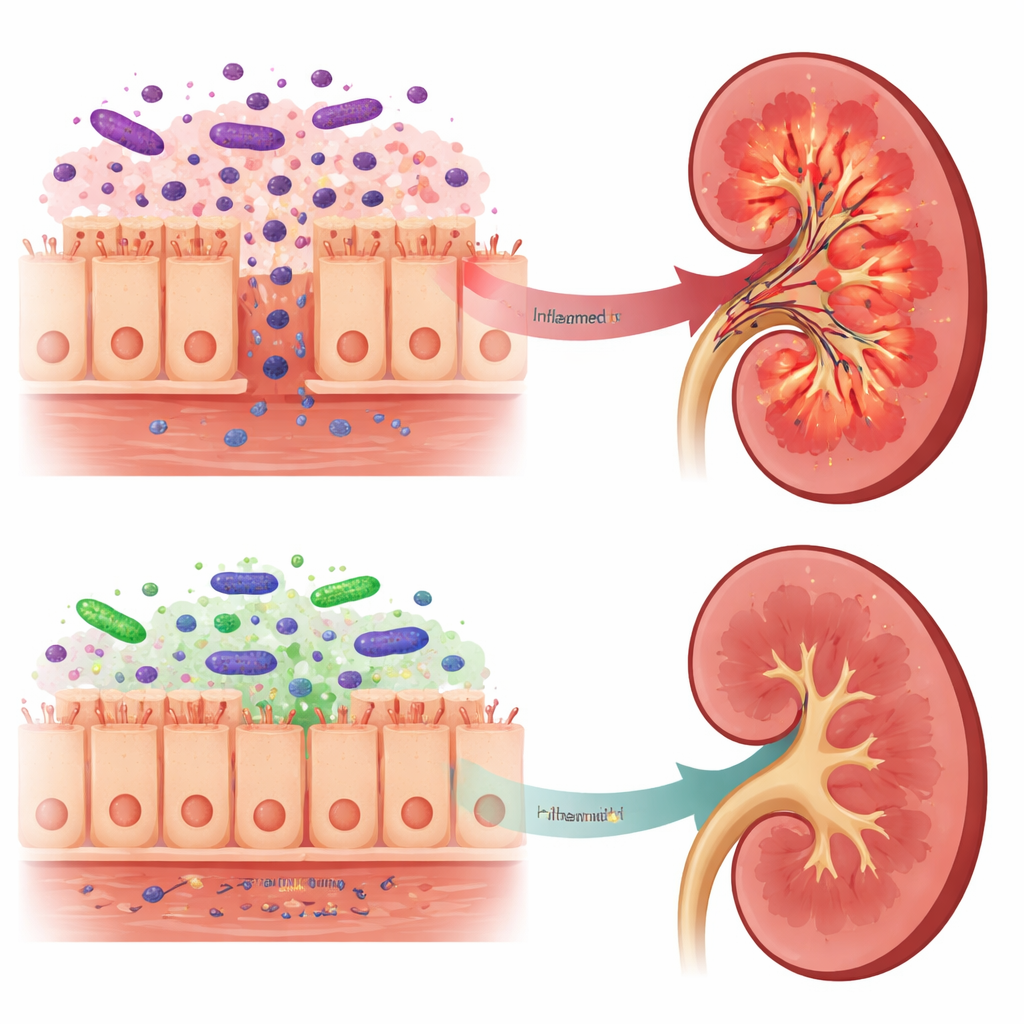
От токсичных сигналов к более мягким посланиям
Эти сдвиги в кишечнике отразились на том, что доходило до почек. У необработанных крыс с мозговой смертью в почечной ткани содержалось больше LPS, повышались уровни TLR4 и его вспомогательного белка LBP, а путь NF-kappaB был сильнее активирован — все признаки выраженного воспалительного ответа. Напротив, у крыс, предварительно получавших Lactobacillus reuteri, в почках было меньше LPS, слабее сигнализация через TLR4 и снижено производство ряда провоспалительных молекул, включая IL-6 и IFN-gamma. Интересно, что общий LPS в крови фактически увеличился в группе пробиотика, но анализ микробов кишечника показал, что большая часть этого LPS исходила от Bacteroidota, чьи структуры LPS считаются значительно менее провоспалительными и даже могут частично блокировать сенсор TLR4. Авторы предполагают, что такое «более мягкое» LPS конкурирует с более вредной формой, снижая экспозицию почек самым токсичным сигналам.
Уравновешивание иммунного ответа по пути кишечник–почка
Пробиотик сделал не только с микробами и барьерами; он также подкорректировал иммунную систему по обе стороны связи кишечник–почка. В кишечнике маркеры активированных иммунных клеток, такие как CD4 и CD25, повышались после мозговой смерти, что указывает на чрезмерную реакцию на слизистой оболочке. Lactobacillus reuteri снизил эту активацию в самом эпителии, но увеличил число CD25-позитивных клеток в подлежащих железах, что намекает на более контролируемую и локализованную защиту. В почках пробиотик уменьшил признаки накопления нейтрофилов и оксидативного стресса, одновременно избирательно повышая уровень хемокина CXCL2, который может способствовать более сбалансированной координации репаративных процессов. Корреляционные анализы связали конкретные представители Bacteroidota с этими иммунными изменениями, что поддерживает идею о кишечной сети иммунного контроля, помогающей защищать почки.
Что это может означать для будущих трансплантаций
В совокупности полученные данные указывают на двойную защитную роль Lactobacillus reuteri у крыс-доноров с мозговой смертью: он восстанавливает более здоровое сообщество и барьер кишечника, а также перестраивает иммунные и воспалительные сигналы, достигающие почек. В результате клетки почек подвергаются меньшему воздействию сильно провоспалительного LPS и демонстрируют лучшую функциональную и структурную сохранность. Хотя работа является доклинической и опирается на предварительное лечение до мозговой смерти, она подчеркивает кишечник и его микробы как перспективные мишени для стратегий улучшения качества органов перед трансплантацией, что потенциально может дать будущим реципиентам лучший старт для долгосрочной функции почек.
Цитирование: Liu, T., Zhu, G., Li, H. et al. Gut microbiota-dependent protection by Lactobacillus reuteri against renal injury in brain-dead rats. Sci Rep 16, 14709 (2026). https://doi.org/10.1038/s41598-026-47230-1
Ключевые слова: микробиота кишечника, пробиотики, повреждение почек, доноры с мозговой смертью, Lactobacillus reuteri