Clear Sky Science · pt
Proteção dependente da microbiota intestinal por Lactobacillus reuteri contra lesão renal em ratos com morte encefálica
Por que esta pesquisa importa
A maioria dos rins usados para transplantes provém de doadores que sofreram morte encefálica, mas esses órgãos frequentemente já estão danificados antes mesmo do início da cirurgia. Este estudo em ratos explora um aliado inesperado que vive no intestino: uma bactéria probiótica chamada Lactobacillus reuteri. Os pesquisadores mostram como esse micro-organismo pode ajudar a proteger os rins contra lesão após a morte encefálica ao estabilizar as bactérias intestinais, reforçar a barreira intestinal e acalmar reações imunes nocivas que, de outra forma, enfraqueceriam órgãos prontos para transplante.
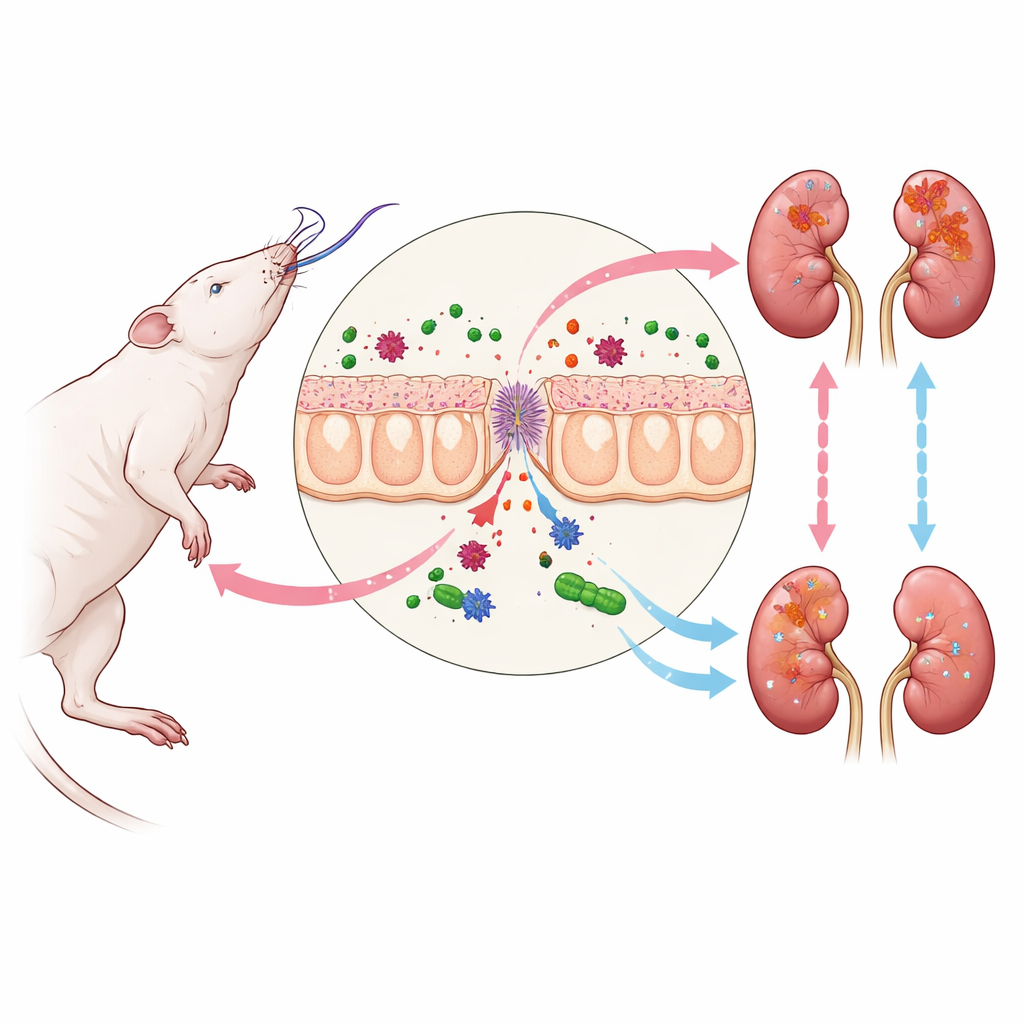
Morte encefálica e a reação em cadeia até os rins
Quando ocorre a morte encefálica, o corpo passa por uma tempestade de alterações hormonais e circulatórias que se espalham por vários órgãos. Um dos primeiros pontos frágeis é o intestino. Seu revestimento protetor fica permeável, permitindo que fragmentos bacterianos dos micróbios intestinais escapem para a corrente sanguínea. Entre esses fragmentos está o LPS, um componente de certas paredes celulares bacterianas que ativa fortemente o sistema imune. À medida que o LPS chega aos rins, ele se liga a um sensor nas células renais que dispara a via TLR4–NF-kappaB, uma rota de sinalização bem conhecida por induzir inflamação. No modelo de rato usado aqui, esse processo levou a níveis mais altos de creatinina e ureia no sangue, aumento da expressão do marcador de dano renal KIM-1 e danos estruturais sutis nas células dos túbulos renais, mesmo quando vistas ao microscópio padrão pareciam quase normais.
Um probiótico reconfigura o ambiente intestinal
Em seguida, a equipe investigou se alimentar os ratos com Lactobacillus reuteri por uma semana antes da morte encefálica poderia mudar essa trajetória. Eles descobriram que o probiótico remodelou a comunidade microbiana intestinal: Proteobacteria nocivas e ricas em LPS foram reduzidas, enquanto Bacteroidota e outros grupos potencialmente benéficos tornaram-se mais abundantes. Ao mesmo tempo, a barreira física do intestino melhorou. Ao microscópio e em micrografias eletrônicas, os animais tratados mostraram junções celulares mais intactas entre as células intestinais e menos alargamento dos espaços onde ocorrem vazamentos. Os níveis sanguíneos de iFABP, um marcador de lesão e permeabilidade intestinal, voltaram em direção ao normal, indicando uma parede intestinal mais firme e seletiva.
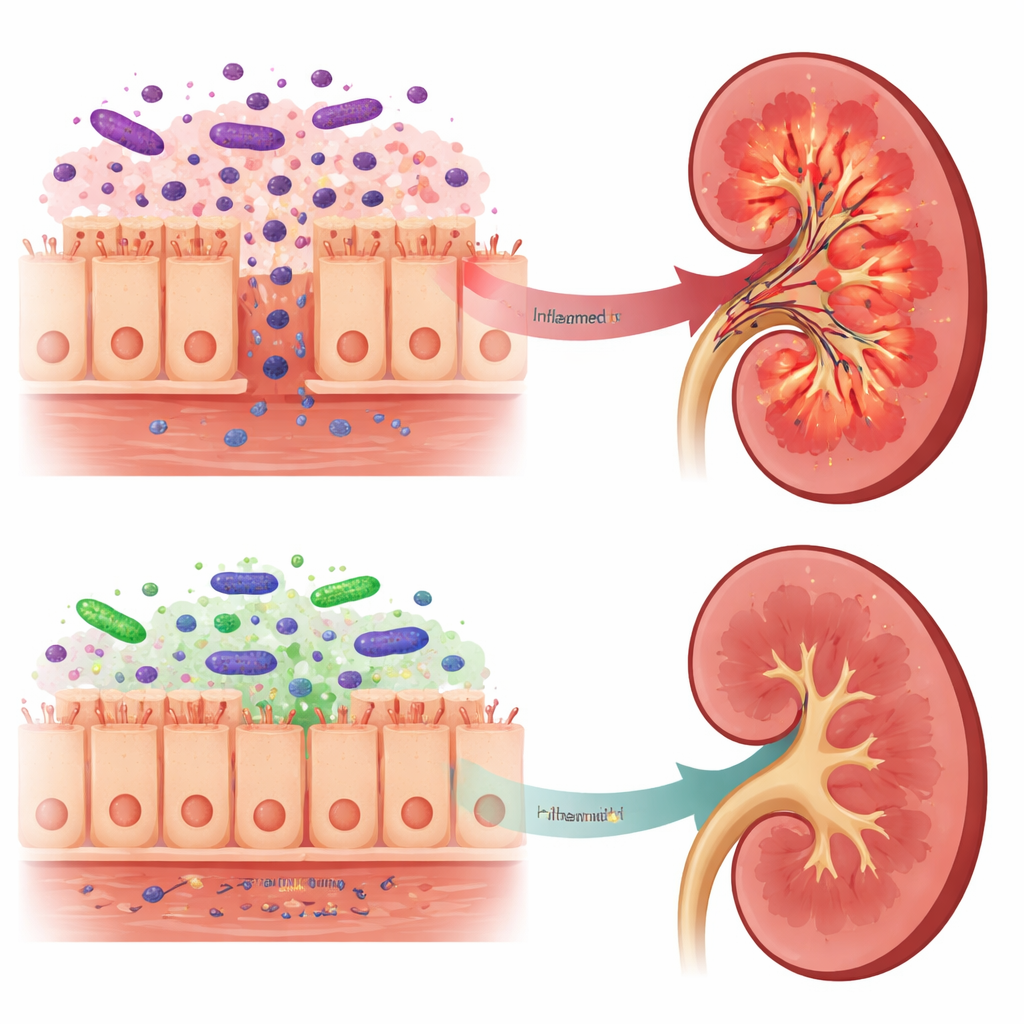
De sinais tóxicos a mensagens mais brandas
Essas mudanças no intestino foram refletidas nas substâncias que alcançaram os rins. Em ratos com morte encefálica não tratados, o tecido renal continha mais LPS, níveis mais altos de TLR4 e de sua proteína auxiliar LBP, e maior ativação da via NF-kappaB, todos sinais de uma resposta inflamatória robusta. Em contraste, ratos pré-tratados com Lactobacillus reuteri apresentaram menor LPS renal, sinalização TLR4 mais fraca e redução na produção de várias moléculas inflamatórias, incluindo IL-6 e IFN-gama. Curiosamente, o LPS total no sangue aumentou no grupo probiótico, mas a análise dos micróbios intestinais sugeriu que grande parte desse LPS vinha de Bacteroidota, cujas estruturas de LPS são consideradas muito menos inflamatórias e podem até agir como bloqueadores parciais do sensor TLR4. Os autores propõem que esse LPS “mais brando” compete com a forma mais danosa, reduzindo a exposição dos rins aos sinais mais tóxicos.
Equilibrando a resposta imune ao longo da rota intestino–rim
O probiótico fez mais do que apenas alterar micróbios e barreiras; ele também modulou o sistema imune em ambos os lados da conexão intestino–rim. No intestino, marcadores de células imunes ativadas, como CD4 e CD25, estavam elevados após a morte encefálica, sugerindo uma resposta exagerada na superfície mucosa. Lactobacillus reuteri reduziu essa ativação no próprio epitélio, mas aumentou células CD25-positivas nas glândulas subjacentes, indicando uma defesa mais controlada e localizada. Nos rins, o probiótico diminuiu sinais de acúmulo de neutrófilos e estresse oxidativo, enquanto aumentou seletivamente a quimiocina CXCL2, que pode ajudar a coordenar uma resposta de reparo mais equilibrada. Análises de correlação vincularam membros específicos de Bacteroidota a essas mudanças imunes, sustentando a ideia de uma rede imune guiada pelo intestino que ajuda a proteger os rins.
O que isso pode significar para transplantes futuros
Em conjunto, os achados apontam para um papel protetor duplo de Lactobacillus reuteri em ratos doadores com morte encefálica: ele reconstrói uma comunidade e uma barreira intestinal mais saudáveis ao mesmo tempo em que remodela sinais imunes e inflamatórios que atingem os rins. Como resultado, as células renais ficam menos expostas a LPS altamente inflamatório e apresentam melhor integridade funcional e estrutural. Embora o trabalho seja pré-clínico e dependa de pré-tratamento antes da morte encefálica, ele destaca o intestino e seus micróbios como alvos promissores para estratégias que melhorem a qualidade dos órgãos antes do transplante, potencialmente oferecendo aos futuros receptores um ponto de partida melhor para a função renal a longo prazo.
Citação: Liu, T., Zhu, G., Li, H. et al. Gut microbiota-dependent protection by Lactobacillus reuteri against renal injury in brain-dead rats. Sci Rep 16, 14709 (2026). https://doi.org/10.1038/s41598-026-47230-1
Palavras-chave: microbiota intestinal, probióticos, lesão renal, doadores com morte encefálica, Lactobacillus reuteri