Clear Sky Science · de
Darmmikrobiota-abhängiger Schutz durch Lactobacillus reuteri vor Nierenschädigung bei hirntoten Ratten
Warum diese Forschung wichtig ist
Die meisten für Transplantationen verwendeten Nieren stammen von Spendern mit Hirntod, doch diese Organe sind oft bereits vor der Operation geschädigt. Diese Studie an Ratten untersucht einen unerwarteten Verbündeten im Darm: ein probiotisches Bakterium namens Lactobacillus reuteri. Die Forschenden zeigen, wie dieser Mikroorganismus die Nieren nach Hirntod schützen kann, indem er die Darmflora stabilisiert, die Darmbarriere stärkt und schädliche Immunreaktionen dämpft, die sonst die transplantationsbereiten Organe schwächen würden.
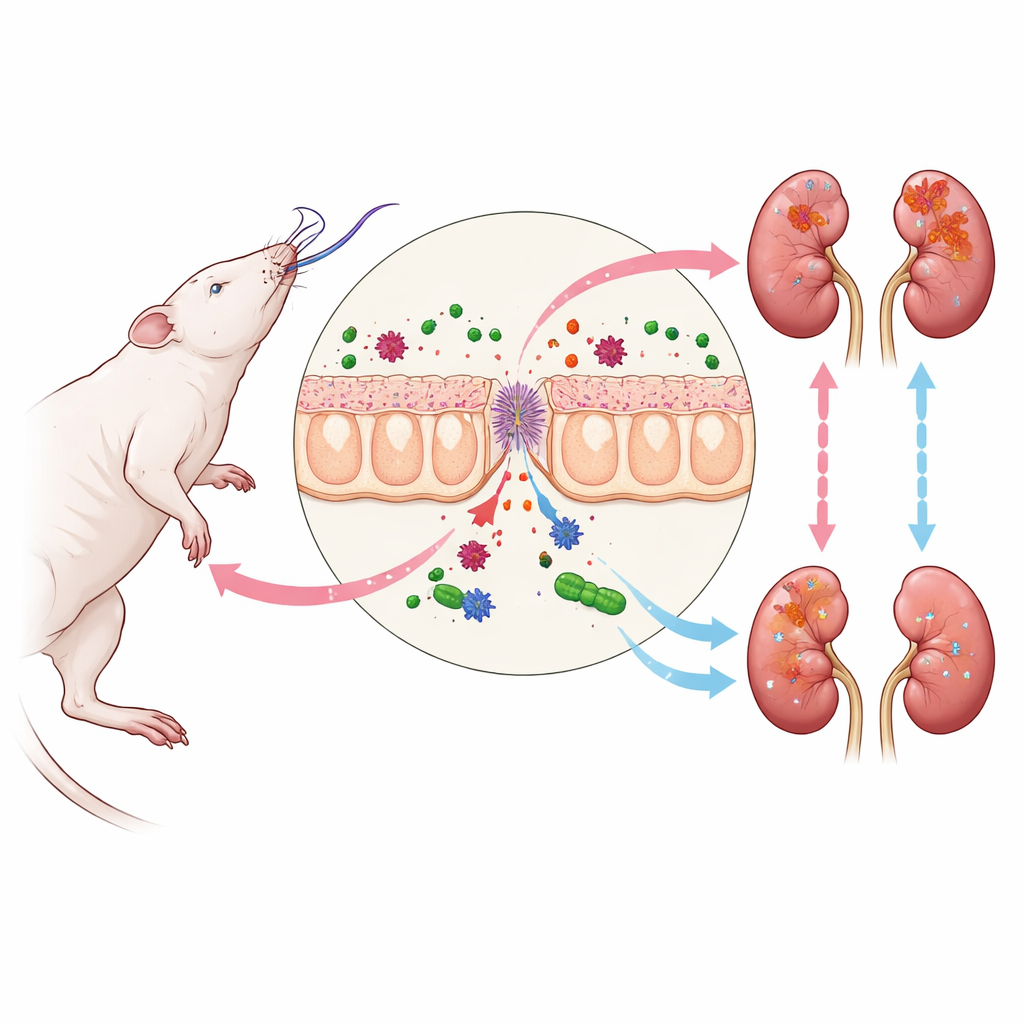
Hirntod und die Kettenreaktion bis zur Niere
Wenn Hirntod eintritt, durchläuft der Körper einen Sturm hormoneller und zirkulatorischer Veränderungen, die viele Organe betreffen. Einer der ersten Schwachpunkte ist der Darm. Seine schützende Schleimhaut wird durchlässig, sodass bakterielle Fragmente aus dem Darm in den Blutkreislauf gelangen können. Unter diesen Fragmenten ist LPS, ein Bestandteil bestimmter bakterieller Zellwände, der das Immunsystem stark aktiviert. Wenn LPS zu den Nieren gelangt, bindet es an einen Sensor auf Nierenzellen und löst den TLR4–NF-kappaB-Weg aus, eine Signalroute, die bekannt dafür ist, Entzündungen voranzutreiben. In dem hier verwendeten Rattenmodell führte dieser Prozess zu erhöhten Blutwerten von Kreatinin und Harnstoff, einer gesteigerten Expression des Nierenschädigungsmarkers KIM-1 und zu subtilen strukturellen Schäden in Nierentubuluszellen, selbst wenn Standard-Blickfelder unter dem Mikroskop fast normal erschienen.
Ein Probiotikum verändert das Darmmilieu
Das Forscherteam fragte dann, ob die Gabe von Lactobacillus reuteri eine Woche vor dem Hirntod die Entwicklung beeinflussen könnte. Sie fanden heraus, dass das Probiotikum die mikrobielle Gemeinschaft im Darm umgestaltete: schädliche, LPS-reiche Proteobakterien wurden reduziert, während Bacteroidota und andere potenziell nützliche Gruppen an Häufigkeit zunahmen. Gleichzeitig verbesserte sich die physische Barriere des Darms. Unter dem Licht- und Elektronenmikroskop zeigten behandelte Tiere intaktere Zellverbindungen zwischen Darmzellen und weniger Erweiterung der Räume, in denen Leckagen entstehen. Die Blutspiegel von iFABP, einem Marker für Darmverletzung und Permeabilität, sanken wieder in Richtung Normalbereich, was auf eine engere, selektivere Darmwand hindeutet.
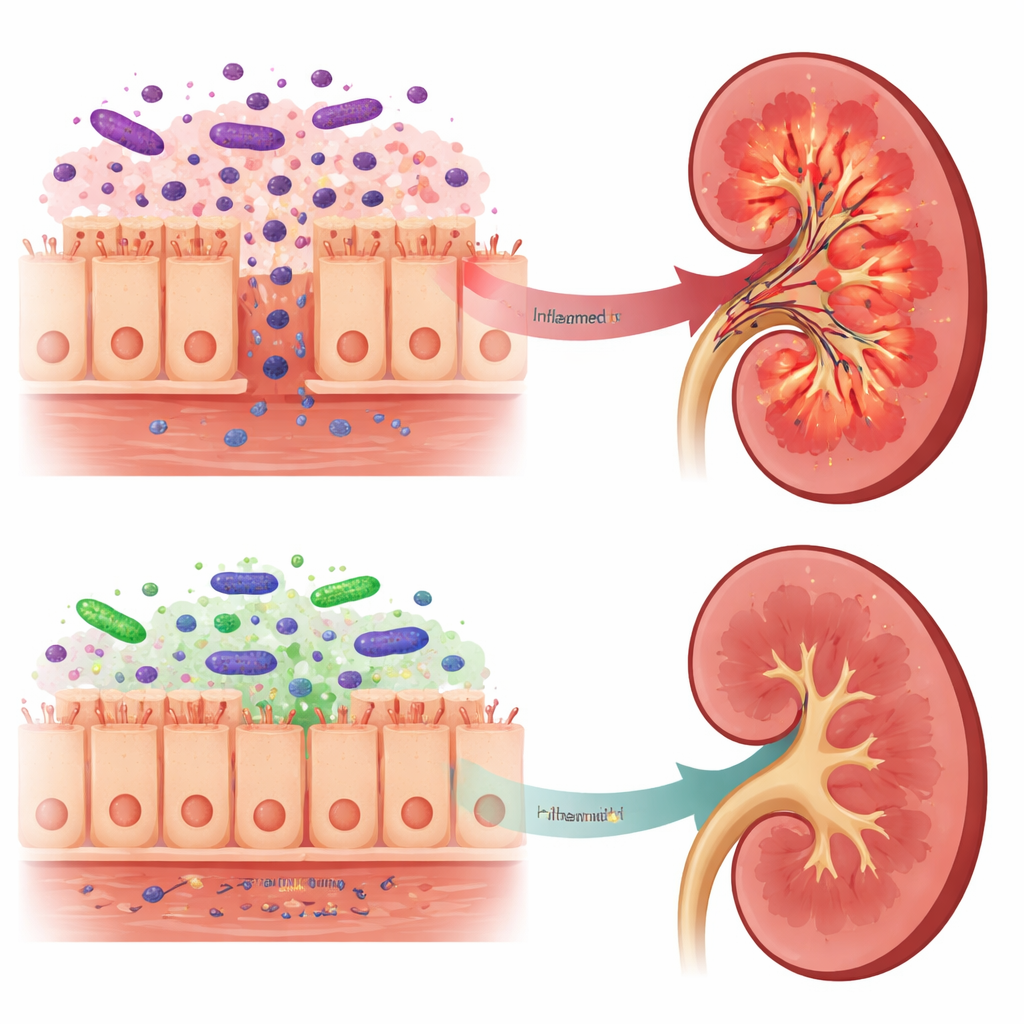
Von toxischen Signalen zu milderen Botschaften
Diese Veränderungen im Darm spiegelten sich in dem, was die Nieren erreichte, wider. In unbehandelten hirntoten Ratten enthielt das Nierengewebe mehr LPS, höhere Mengen an TLR4 und dem Helferprotein LBP sowie eine stärkere Aktivierung des NF-kappaB-Wegs – alles Zeichen einer ausgeprägten Entzündungsreaktion. Dagegen zeigten Ratten, die mit Lactobacillus reuteri vorbehandelt worden waren, geringere LPS-Werte in der Niere, schwächere TLR4-Signale und reduzierte Produktion mehrerer entzündlicher Moleküle, darunter IL-6 und IFN-gamma. Interessanterweise stieg das Gesamtlipopolysaccharid (LPS) im Blut in der Probiotika-Gruppe tatsächlich an, doch die Analyse der Darmmikrobiota deutete darauf hin, dass ein großer Teil dieses LPS von Bacteroidota stammte, deren LPS-Strukturen als deutlich weniger entzündlich gelten und möglicherweise sogar als partielle Blocker des TLR4-Sensors wirken. Die Autorinnen und Autoren schlagen vor, dass dieses „milderere“ LPS mit der schädigeren Form konkurriert und so die Exposition der Niere gegenüber den toxischsten Signalen reduziert.
Balancierung der Immunantwort entlang der Darm–Nieren-Achse
Das Probiotikum bewirkte mehr als nur Veränderungen der Mikroben und der Barriere; es stellte auch das Immunsystem auf beiden Seiten der Darm–Nieren-Verbindung fein. Im Darm waren Marker aktivierter Immunzellen wie CD4 und CD25 nach Hirntod erhöht, was auf eine übermäßige Reaktion an der Schleimhaut hindeutet. Lactobacillus reuteri dämpfte diese Aktivierung in der Schleimhaut selbst, erhöhte jedoch CD25-positive Zellen in den darunterliegenden Drüsen, was auf eine kontrolliertere und lokalisiertere Abwehr schließen lässt. In den Nieren reduzierte das Probiotikum Zeichen von Neutrophilen-Akkumulation und oxidativem Stress, während selektiv das Chemokin CXCL2 gesteigert wurde, das möglicherweise hilft, eine ausgeglichenere Reparaturreaktion zu koordinieren. Korrelationsanalysen verbanden bestimmte Bacteroidota-Mitglieder mit diesen Immunchanges und stützen die Idee eines darmgetriebenen Immunnetzwerks, das die Nieren schützt.
Was das für zukünftige Transplantationen bedeuten könnte
In der Summe deuten die Ergebnisse auf eine doppelte Schutzwirkung von Lactobacillus reuteri bei hirntoten Spenderratten hin: Es stellt eine gesündere Darmgemeinschaft und Barriere wieder her und verändert zugleich die immunologischen und entzündlichen Signale, die die Nieren erreichen. Dadurch sind die Nierenzellen weniger schädlichen, stark entzündungsfördernden LPS-Signalen ausgesetzt und zeigen bessere funktionelle und strukturelle Gesundheit. Obwohl die Arbeit präklinisch ist und auf einer Vorbehandlung vor dem Hirntod beruht, hebt sie den Darm und seine Mikroben als vielversprechende Ziele hervor, um die Organqualität vor einer Transplantation zu verbessern und potenziell Empfängern einen besseren Ausgangspunkt für langfristige Nierenfunktion zu geben.
Zitation: Liu, T., Zhu, G., Li, H. et al. Gut microbiota-dependent protection by Lactobacillus reuteri against renal injury in brain-dead rats. Sci Rep 16, 14709 (2026). https://doi.org/10.1038/s41598-026-47230-1
Schlüsselwörter: Darmmikrobiota, Probiotika, Nierenschädigung, Hirntod-Spender, Lactobacillus reuteri