Clear Sky Science · pl
Ochrona zależna od mikrobioty jelitowej przez Lactobacillus reuteri przed uszkodzeniem nerek u szczurów z śmiercią mózgową
Dlaczego to badanie ma znaczenie
Większość nerek używanych do przeszczepów pochodzi od dawców po stwierdzonej śmierci mózgu, jednak te narządy często są uszkodzone jeszcze przed rozpoczęciem operacji. W badaniu na szczurach zbadano nieoczekiwanego sprzymierzeńca żyjącego w jelitach: bakterię probiotyczną Lactobacillus reuteri. Badacze pokazują, jak ten mikroorganizm może pomóc chronić nerki przed uszkodzeniem po śmierci mózgu, stabilizując skład mikrobioty jelitowej, wzmacniając barierę jelitową i łagodząc szkodliwe reakcje immunologiczne, które w innym przypadku osłabiłyby narządy gotowe do przeszczepu.
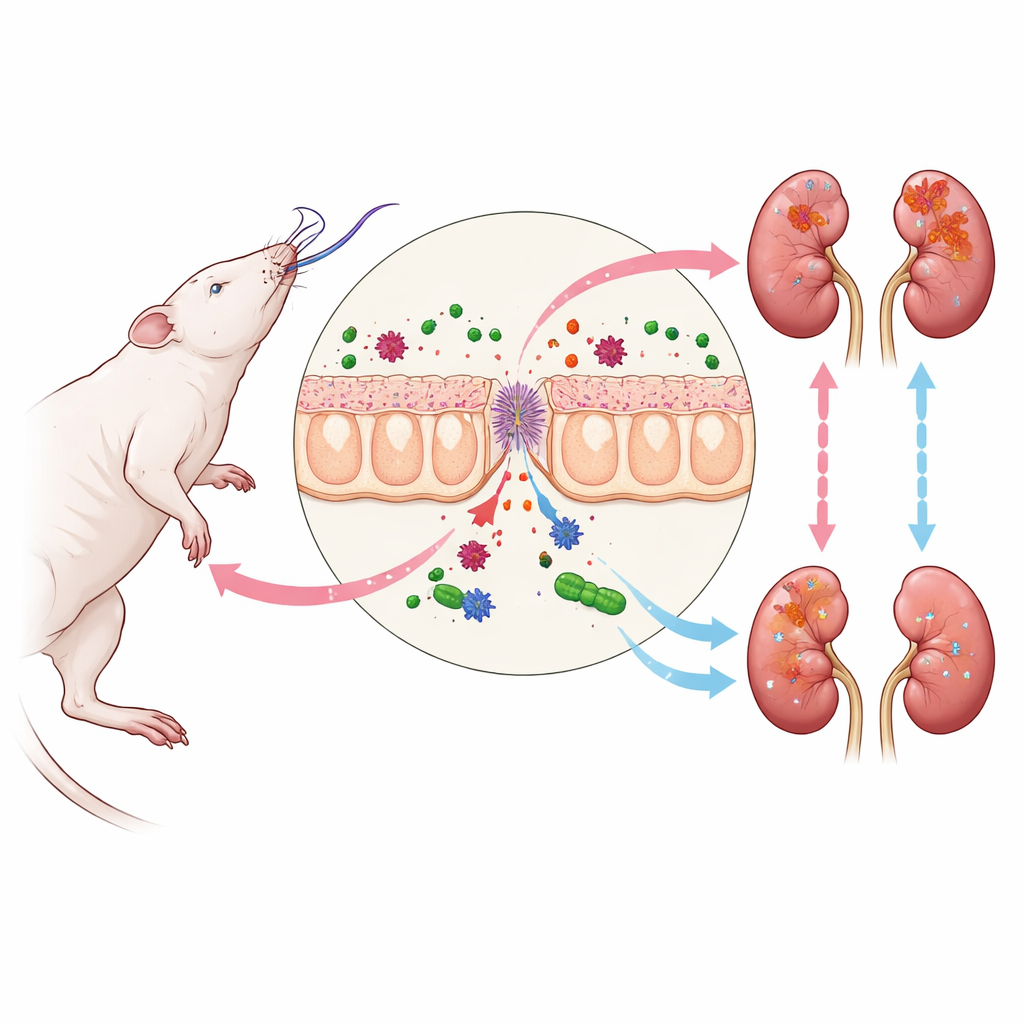
Śmierć mózgu i łańcuch reakcji prowadzący do nerek
Gdy dochodzi do śmierci mózgu, organizm przechodzi burzę zmian hormonalnych i krążeniowych, które rozchodzą się po wielu narządach. Jednym z pierwszych słabych punktów jest jelito. Jego ochronna warstwa staje się nieszczelna, co pozwala fragmentom bakterii z mikrobioty jelitowej przedostać się do krwiobiegu. Wśród tych fragmentów znajduje się LPS, składnik ścian komórkowych niektórych bakterii, który silnie aktywuje układ odpornościowy. Gdy LPS dociera do nerek, wiąże się z czujnikiem na komórkach nerkowych, uruchamiając szlak TLR4–NF-kappaB, dobrze znany z wywoływania stanu zapalnego. W modelu szczura zastosowanym tutaj proces ten prowadził do wzrostu stężenia kreatyniny i mocznika we krwi, zwiększonej ekspresji markera uszkodzenia nerek KIM-1 oraz subtelnych zmian strukturalnych w komórkach kanalików nerkowych, nawet gdy standardowe obrazy mikroskopowe wyglądały niemal normalnie.
Probiotyk przebudowuje środowisko jelitowe
Zespół zapytał następnie, czy podawanie szczurom Lactobacillus reuteri przez tydzień przed śmiercią mózgu może zmienić ten przebieg zdarzeń. Okazało się, że probiotyk przekształcił społeczność mikrobiologiczną jelit: zmniejszyła się liczebność szkodliwych, bogatych w LPS Proteobacteria, podczas gdy Bacteroidota i inne potencjalnie korzystne grupy stały się bardziej obfite. Równocześnie poprawiła się fizyczna bariera jelitowa. W preparatach mikroskopowych i skanach elektronowych zwierzęta poddane terapii wykazywały bardziej nienaruszone połączenia międzykomórkowe w nabłonku jelitowym oraz mniejsze poszerzenie przestrzeni, w których powstają przecieki. Poziomy iFABP we krwi, markera uszkodzenia i przepuszczalności jelit, spadły w kierunku wartości prawidłowych, co wskazuje na bardziej szczelne, selektywne ściany jelita.
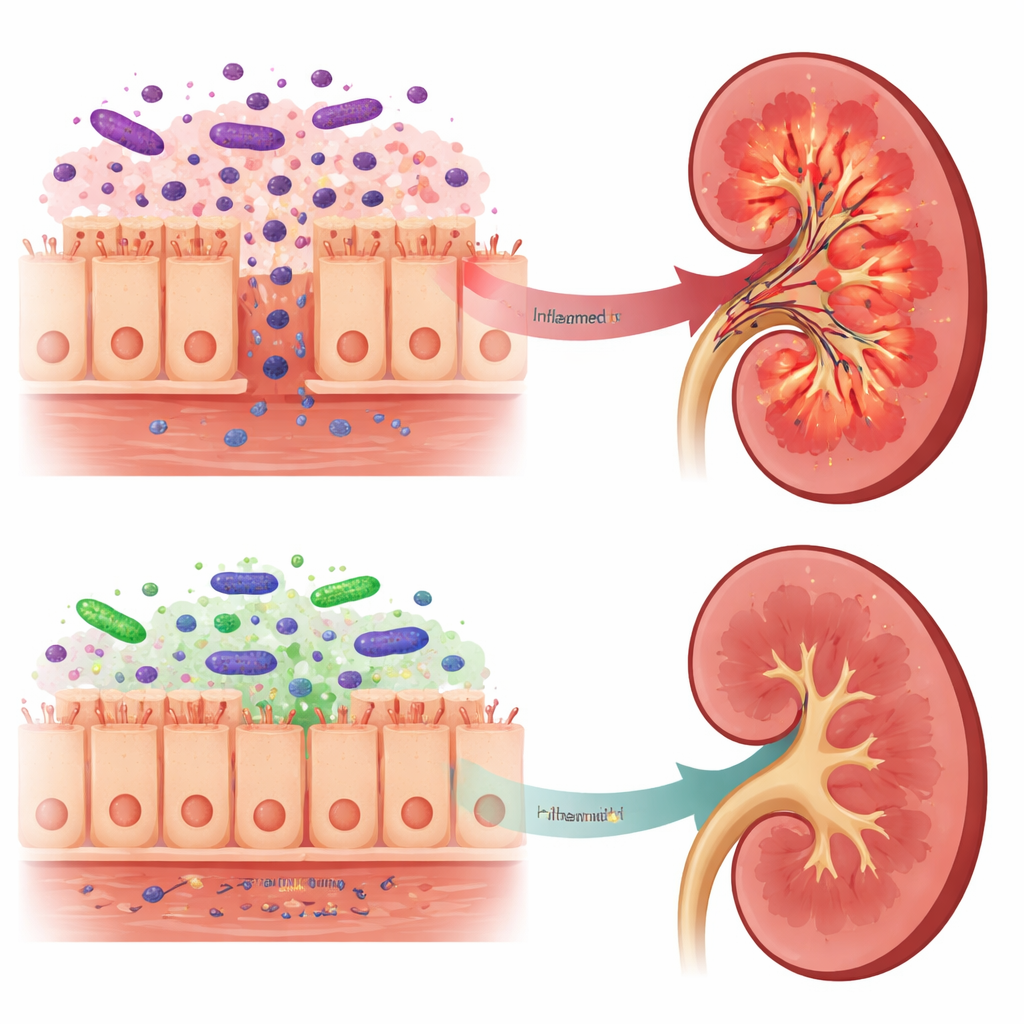
Z toksycznych sygnałów ku łagodniejszym komunikatom
Zmiany w jelitach znalazły odzwierciedlenie w tym, co docierało do nerek. U nieleczonych szczurów po śmierci mózgu tkanka nerek zawierała więcej LPS, wyższe poziomy TLR4 i jego białka pomocniczego LBP oraz silniejszą aktywację szlaku NF-kappaB — wszystkie te cechy świadczą o silnej odpowiedzi zapalnej. Natomiast szczury poddane wstępnej kuracji Lactobacillus reuteri miały niższe stężenie LPS w nerkach, słabsze sygnalizowanie przez TLR4 i zmniejszoną produkcję kilku mediatorów zapalnych, w tym IL-6 i IFN-gamma. Co ciekawe, całkowite LPS we krwi faktycznie wzrosło w grupie probiotycznej, ale analiza mikrobioty jelitowej sugerowała, że wiele z tego LPS pochodziło od Bacteroidota, których struktury LPS uważa się za znacznie mniej prozapalne i które mogą nawet działać jako częściowi blokery czujnika TLR4. Autorzy proponują, że ten „łagodniejszy” LPS konkuruje z formami bardziej szkodliwymi, zmniejszając ekspozycję nerek na najbardziej toksyczne sygnały.
Wyrównywanie odpowiedzi immunologicznej wzdłuż osi jelito–nerka
Probiotyk robił więcej niż tylko zmieniał mikroby i barierę; dostroił także układ odpornościowy po obu stronach połączenia jelito–nerka. W jelicie markery aktywacji komórek odpornościowych, takie jak CD4 i CD25, wzrastały po śmierci mózgu, co sugerowało nadmierną reakcję na powierzchni błony śluzowej. Lactobacillus reuteri ograniczył tę aktywację w samym nabłonku, ale zwiększył liczbę komórek CD25-dodatnich w leżących poniżej gruczołach, co sugeruje bardziej kontrolowaną i zlokalizowaną obronę. W nerkach probiotyk zmniejszył objawy nagromadzenia neutrofili i stresu oksydacyjnego, jednocześnie selektywnie zwiększając chemokinę CXCL2, która może pomagać w skoordynowaniu bardziej zrównoważonej reakcji naprawczej. Analizy korelacji powiązały konkretne członki Bacteroidota z tymi zmianami immunologicznymi, wspierając koncepcję sieci odporności sterowanej przez jelita, która pomaga chronić nerki.
Co to może znaczyć dla przyszłych przeszczepów
W sumie wyniki wskazują na podwójną ochronną rolę Lactobacillus reuteri u szczurów-dawców ze śmiercią mózgu: odbudowuje zdrowszą społeczność jelitową i barierę oraz przeobraża sygnały immunologiczne i zapalne docierające do nerek. W rezultacie komórki nerkowe są mniej narażone na silnie prozapalny LPS i wykazują lepszą funkcję oraz stan strukturalny. Chociaż prace te mają charakter przedkliniczny i opierają się na wstępnym leczeniu przed śmiercią mózgu, podkreślają jelito i jego mikroby jako obiecujące cele strategii poprawy jakości narządów przed przeszczepem, co potencjalnie daje przyszłym biorcom lepszy punkt wyjścia dla długoterminowej funkcji nerek.
Cytowanie: Liu, T., Zhu, G., Li, H. et al. Gut microbiota-dependent protection by Lactobacillus reuteri against renal injury in brain-dead rats. Sci Rep 16, 14709 (2026). https://doi.org/10.1038/s41598-026-47230-1
Słowa kluczowe: mikrobiota jelitowa, probiotyki, uszkodzenie nerek, dawcy ze śmiercią mózgową, Lactobacillus reuteri