Clear Sky Science · sv
Omplacering av FDA‑godkända läkemedel till multitarget neuroprotektiva medel för Alzheimers sjukdom via beräkningsbaserad screening och experimentell validering
Varför gamla mediciner kan hjälpa ett sviktande minne
Alzheimers sjukdom berövar miljontals människor deras minnen och självständighet, och dagens läkemedel lindrar endast symtomen under en begränsad tid. Att utveckla helt nya läkemedel är långsamt, kostsamt och riskfyllt. Denna studie ställer en enkel men kraftfull fråga: kan vi söka bland läkemedel som redan är godkända och säkerhetstestade för andra tillstånd och hitta sådana som tyst skyddar den åldrande hjärnan på flera fronter samtidigt?
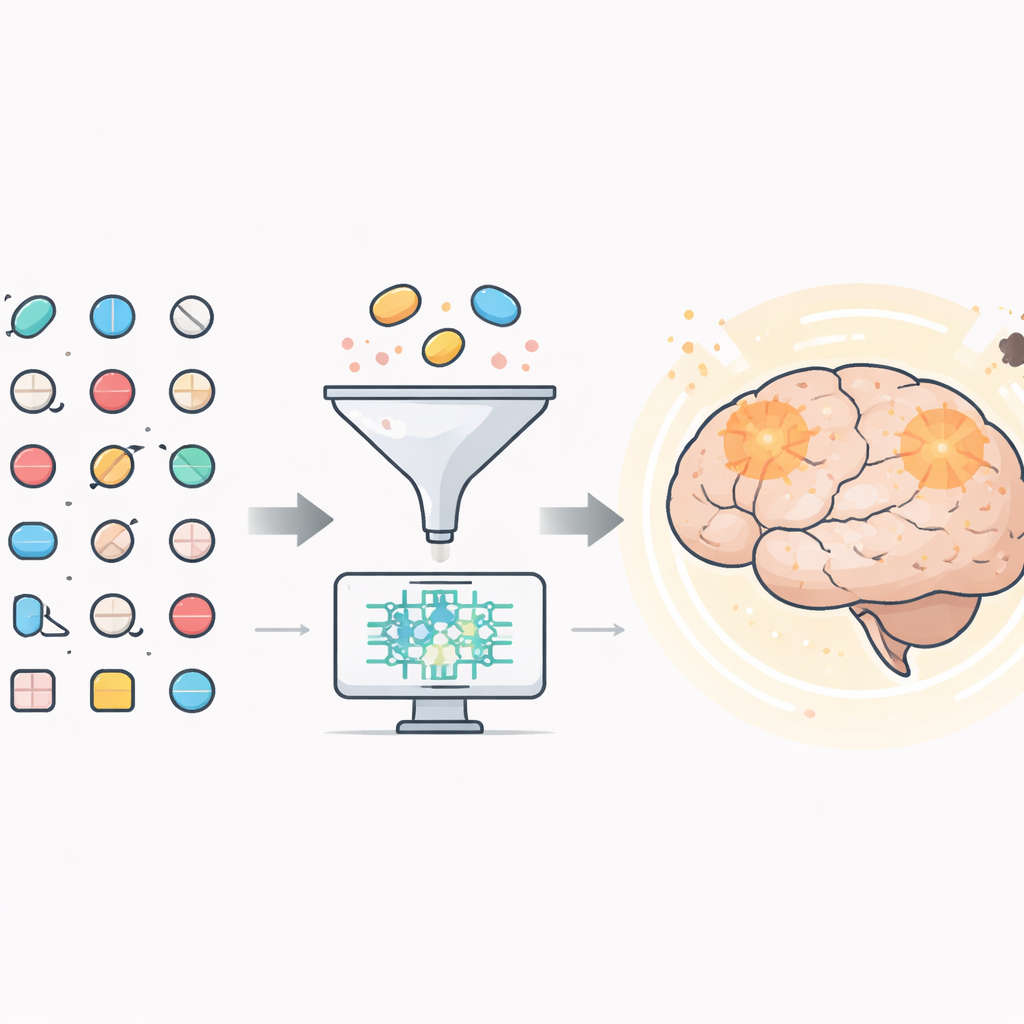
Letar efter dolda hjälpande krafter i befintliga läkemedel
Forskarna började med mer än 1 500 läkemedel som redan godkänts av den amerikanska läkemedelsmyndigheten FDA. Med hjälp av datorbaserade verktyg filtrerade de först bort föreningar som sannolikt inte når hjärnan, eftersom en behandling för Alzheimers måste passera blod‑hjärnbarriären. Omkring 600 kandidater klarade detta test. Därefter använde de detaljerade 3D‑modeller av ett viktigt hjärnenzym, kallat BACE1, för att se vilka läkemedel som skulle kunna fästa vid dess aktiva säte på ett stabilt och tätt sätt. BACE1 är betydelsefullt eftersom det hjälper till att klyva ett större protein till amyloid‑beta, den klibbiga fragmentet som klumpar ihop sig till plack i hjärnorna hos personer med Alzheimers.
Hittar en kandidat som kan flera uppgifter
Från denna virtuella screening identifierades 14 lovande träffar, och fyra valdes ut för närmare studier baserat på hur väl de passade enzymet, deras kemiska egenskaper och deras kända säkerhet vid långvarig användning. Teamet körde sedan långa datorbaserade simuleringar för att följa hur varje kandidat uppförde sig medan den var bunden till BACE1 över tid. Alla fyra höll sig stadigt i enzymets ficka, men en förening, märkt ZINC000019796155, utmärkte sig för sina gynnsamma interaktioner med de mest kritiska regionerna av BACE1. Dessa simuleringar antydde att läkemedlet skulle kunna minska enzymets förmåga att producera amyloid‑beta utan att destabilisera proteinet självt.
Testar hur läkemedlet skyddar hjärnans kemi
Datorprediktioner är bara ett första steg, så forskarna testade de fyra kandidaterna i laboratorieexperiment. Samtliga bromsade BACE1‑aktivitet, och ZINC000019796155 visade den starkaste effekten, om än fortfarande svagare än mycket potenta experimentella hämmare. Viktigt är att när de undersökte andra processer kopplade till Alzheimers fann de att samma förening hämmade ett annat enzym, butyrylkolinesteras, som blir mer aktivt ju längre sjukdomen fortskrider och bryter ner en minnesrelaterad kemisk budbärare. Den minskade också klumpningen av amyloid‑beta i ett provrörstest och visade stark antioxidantaktivitet, vilket innebär att den kan neutralisera skadliga fria radikaler som bidrar till celldöd i hjärnan.
Skyddar nervceller från skada
För att se hur dessa effekter översätts inne i levande celler exponerade teamet människoodlade, nervliknande celler för väteperoxid, en kemikalie som efterliknar den oxidativa stress som ses i Alzheimers hjärnor och som normalt dödar många celler. När cellerna förbehandlades med ZINC000019796155 överlevde betydligt fler. Vidare analys av cellproteiner visade att föreningen dämpade markörer för programmerad celldöd och sänkte nivåerna av nyckelspelare i plack‑ och trasselbildning, inklusive förstadiet till amyloid‑beta, själva BACE1‑enzymet och en modifierad form av tau‑proteinet som tenderar att bilda vridna fibrer inne i neuroner. Samtidigt förstärkte den signaler längs vägar som är kända för att hålla tau i ett friskare, mindre klibbigt tillstånd.
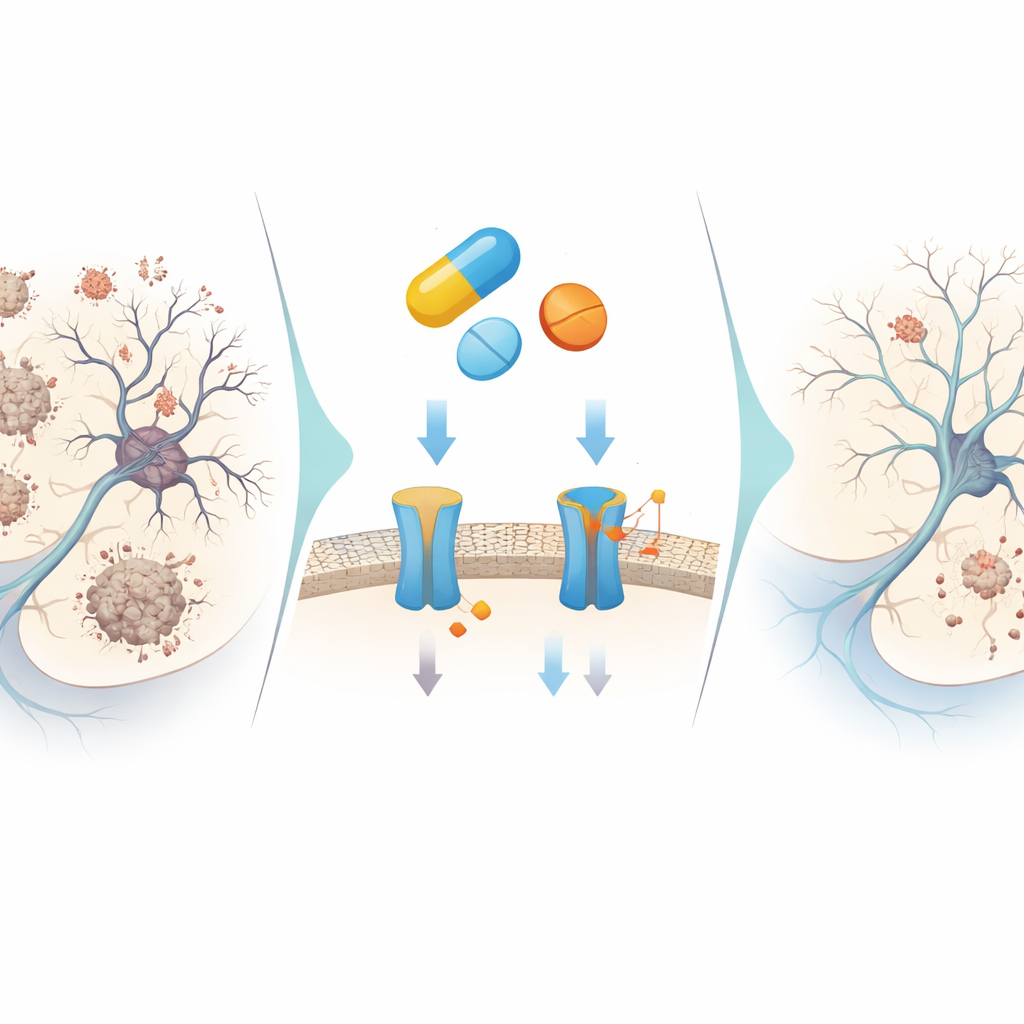
Vad detta kan betyda för framtida behandlingar
Tillsammans tyder resultaten på att ZINC000019796155, ett redan godkänt läkemedel, kan fungera som ett litet molekylärt multiverktyg: det blockerar delvis produktionen av amyloid‑beta, bromsar dess aggregering, begränsar nedbrytningen av en viktig minnesbudbärare, släcker skadliga oxidationsmedel och hjälper till att styra nervceller bort från självdestruktiva vägar och trasselbildning. Dess effekter är måttliga snarare än extrema, vilket faktiskt kan vara säkrare med tanke på tidigare misslyckanden med alltför starka BACE1‑hämmare. Även om föreningen kommer att behöva kemisk finjustering och noggrann testning i djur och så småningom människor, visar denna studie hur smart datorisk screening i kombination med riktade labbexperiment kan avslöja nya hjärnskyddande roller för välkända läkemedel och öppna en mer effektiv väg mot framtida Alzheimers‑terapier.
Citering: Phemphunananchai, K., Waiwut, P., Phetcharaburanin, J. et al. Repurposing FDA-approved drugs as multi-target neuroprotective agents for Alzheimer’s disease via computational screening and experimental validation. Sci Rep 16, 11688 (2026). https://doi.org/10.1038/s41598-026-46708-2
Nyckelord: Alzheimers sjukdom, läkemedelsomplacering, BACE1‑inhibering, multimålsbehandling, neuroprotektion