Clear Sky Science · nl
Herbestemming van door de FDA goedgekeurde medicijnen als multitarget-neuroprotectieve middelen voor de ziekte van Alzheimer via computationele screening en experimentele validatie
Waarom oude medicijnen een verzwakkend geheugen kunnen helpen
De ziekte van Alzheimer berooft miljoenen mensen van hun herinneringen en zelfstandigheid, en de huidige medicijnen verlichten de symptomen maar voor een beperkte tijd. Het ontwikkelen van gloednieuwe geneesmiddelen is traag, duur en riskant. Deze studie stelt een eenvoudige maar krachtige vraag: kunnen we zoeken onder medicijnen die al zijn goedgekeurd en op veiligheid zijn getest voor andere aandoeningen, en middelen vinden die het verouderende brein op meerdere fronten tegelijk stilletjes beschermen?
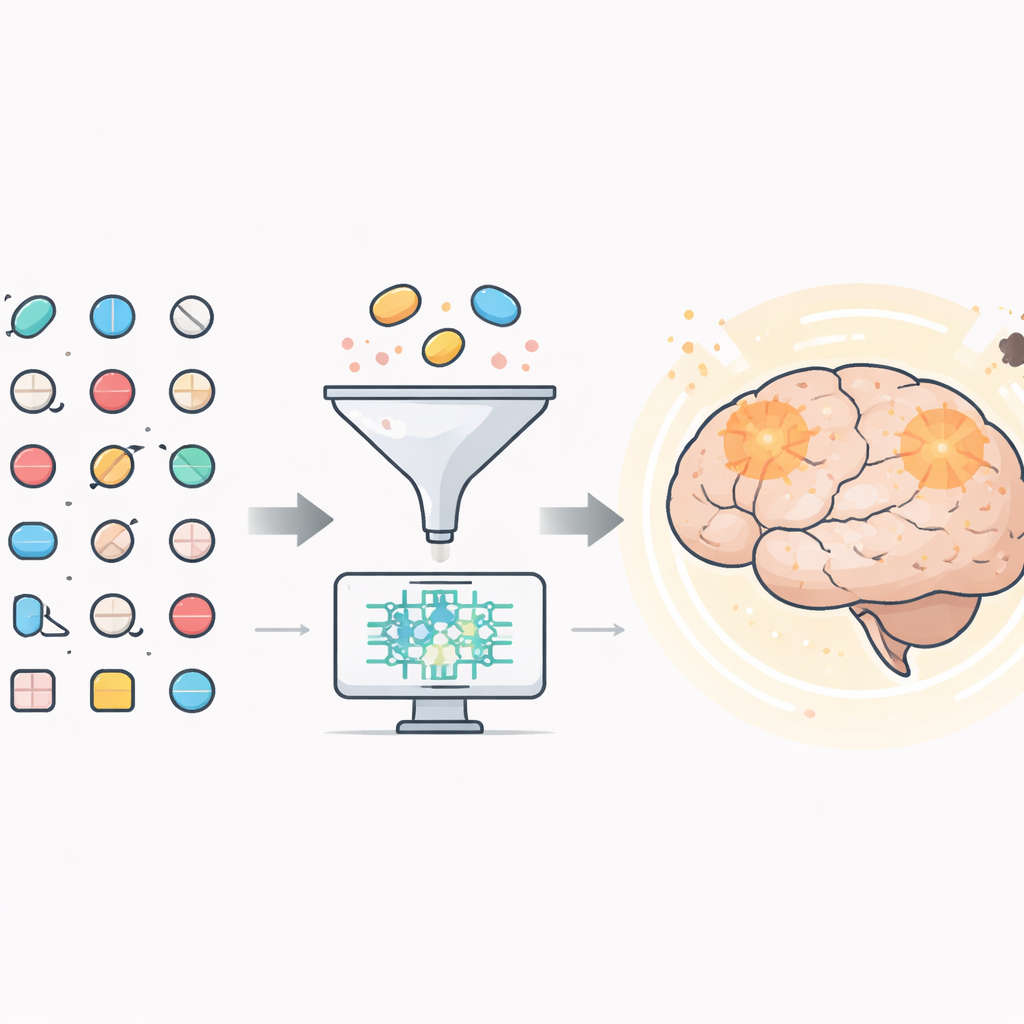
Op zoek naar verborgen helpers in bestaande medicijnen
De onderzoekers begonnen met meer dan 1.500 geneesmiddelen die al door de Amerikaanse Food and Drug Administration waren goedgekeurd. Met behulp van computertools filterden ze eerst verbindingen weg die waarschijnlijk niet het brein zouden bereiken, aangezien een behandeling voor Alzheimer de bloed‑hersenbarrière moet passeren. Ongeveer 600 kandidaten slaagden voor deze test. Vervolgens gebruikten ze gedetailleerde 3D‑modellen van een belangrijk hersenenzym, BACE1, om te zien welke geneesmiddelen zich op een stabiele en nauwsluitende manier aan het actieve centrum konden binden. BACE1 is belangrijk omdat het helpt een groter eiwit in stukken te knippen tot amyloïde‑bèta, het plakkerige fragment dat samenklontert tot plaques in de hersenen van mensen met Alzheimer.
Een multitaskend kandidaatgeneesmiddel vinden
Uit deze virtuele screening werden 14 veelbelovende hits geïdentificeerd, en vier werden geselecteerd voor nader onderzoek op basis van hoe goed ze in het enzym pasten, hun chemische eigenschappen en hun bekende veiligheid bij langdurig gebruik. Het team voerde vervolgens lange computersimulaties uit om te observeren hoe elke kandidaat zich gedroeg terwijl deze gebonden was aan BACE1 in de loop van de tijd. Alle vier bleven stabiel in het enzymenpoeltje, maar één verbinding, aangeduid als ZINC000019796155, onderscheidde zich door gunstige interacties met de meest kritische regio’s van BACE1. Deze simulaties suggereerden dat het geneesmiddel de capaciteit van het enzym om amyloïde‑bèta te produceren kon verminderen zonder het eiwit zelf te destabiliseren.
Testen hoe het geneesmiddel de hersenchemie beschermt
Computervoorspellingen zijn slechts een eerste stap, dus de wetenschappers testten de vier kandidaten in laboratoriumexperimenten. Al deze middelen vertraagden de activiteit van BACE1, en ZINC000019796155 toonde het sterkste effect, hoewel nog steeds zwakker dan zeer potente experimentele remmers. Belangrijk was dat, bij het onderzoeken van andere processen die met Alzheimer verbonden zijn, ze ontdekten dat diezelfde verbinding ook een ander enzym remde, butyrylcholinesterase, dat actiever wordt naarmate de ziekte vordert en een geheugen‑gerelateerde signaalstof afbreekt. Het verminderde ook de aggregatie van amyloïde‑bèta in een reageerbuis en toonde sterke antioxiderende activiteit, wat betekent dat het schadelijke vrije radicalen kon neutraliseren die bijdragen aan het afsterven van hersencellen.
Bescherming van zenuwcellen tegen schade
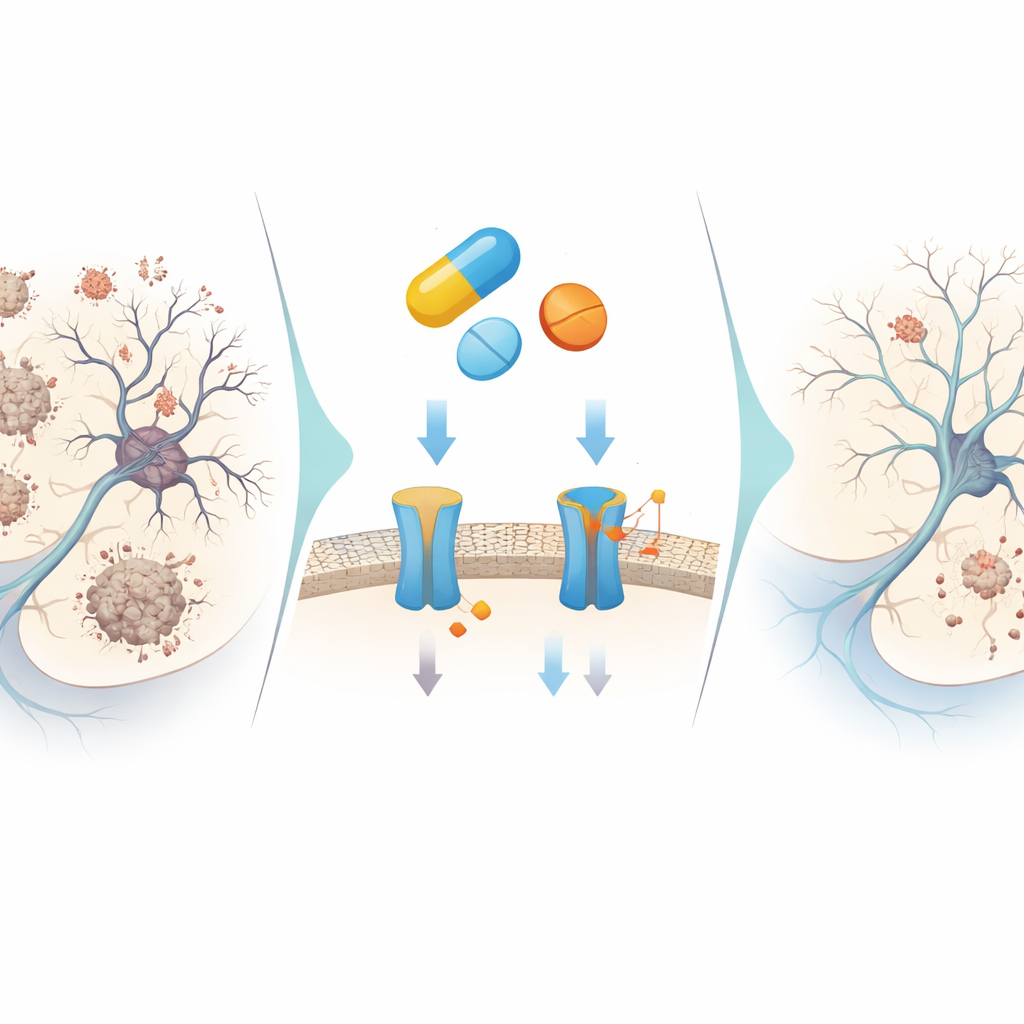
Om te zien hoe deze effecten zich vertalen in levende cellen, blootstelden de onderzoekers menselijk‑afgeleide zenuwachtige cellen aan waterstofperoxide, een stof die de oxidatieve stress nabootst die bij Alzheimer voorkomt en normaal veel cellen doet afsterven. Wanneer de cellen vooraf werden behandeld met ZINC000019796155, overleefden er veel meer. Verder eiwitanalyses van de cellen toonden aan dat de verbinding merkers van geprogrammeerde celdood dempte en de niveaus verlaagde van sleutelspelers bij plaque‑ en kluwenvorming, waaronder het voorstadium van amyloïde‑bèta, het BACE1‑enzym zelf en een gewijzigde vorm van het tau‑eiwit die de neiging heeft gedraaide vezels binnen neuronen te vormen. Tegelijkertijd versterkte het signalen langs routes die bekendstaan om tau in een gezondere, minder kleverige staat te houden.
Wat dit kan betekenen voor toekomstige behandeling
Samengevat suggereren de resultaten dat ZINC000019796155, een reeds goedgekeurd geneesmiddel, kan optreden als een klein moleculair multitool: het blokkeert gedeeltelijk de productie van amyloïde‑bèta, vertraagt de aggregatie ervan, beperkt de afbraak van een belangrijke geheugensignaalstof, dooft schadelijke oxidanten en helpt zenuwcellen weg te sturen van zelfvernietigingsroutes en kluwenvorming. De effecten zijn gematigd in plaats van extreem, wat juist veiliger kan zijn gezien eerdere mislukkingen met te sterke BACE1‑remmers. Hoewel de verbinding chemische bijstelling en zorgvuldige tests in dieren en uiteindelijk mensen nodig zal hebben, illustreert deze studie hoe slimme computergestuurde screening gecombineerd met gerichte labexperimenten nieuwe breinbeschermende rollen voor vertrouwde medicijnen kan onthullen, en zo een efficiëntere route naar toekomstige Alzheimer‑therapieën opent.
Bronvermelding: Phemphunananchai, K., Waiwut, P., Phetcharaburanin, J. et al. Repurposing FDA-approved drugs as multi-target neuroprotective agents for Alzheimer’s disease via computational screening and experimental validation. Sci Rep 16, 11688 (2026). https://doi.org/10.1038/s41598-026-46708-2
Trefwoorden: Ziekte van Alzheimer, herbestemming van geneesmiddelen, BACE1-remming, multitarget-therapie, neuroprotectie